Clear Sky Science · pt
Visualizando a progressão maligna: ensaio de imunofluorescência espacial in situ baseado em CD109 delineia a transformação de carcinoma papilífero para anaplásico de tireoide no microambiente tumoral
Por que este estudo sobre câncer de tireoide é importante
O carcinoma anaplásico da tireoide é um dos cânceres humanos mais letais, frequentemente transformando um tumor de tireoide que normalmente seria tratável em uma doença rapidamente fatal. Ainda assim, os médicos não compreendem totalmente como um carcinoma papilífero da tireoide, comum e de crescimento lento, pode de repente evoluir para essa forma agressiva. Este estudo acompanha essa transformação diretamente dentro do tumor de um paciente, usando uma nova técnica de imagem para observar como as células cancerosas e o tecido ao redor mudam etapa por etapa. O trabalho oferece uma imagem mais detalhada de como o ambiente local do tumor pode empurrar as células em direção a um estado mais letal, sugerindo novas formas de retardar ou prevenir essa transição.
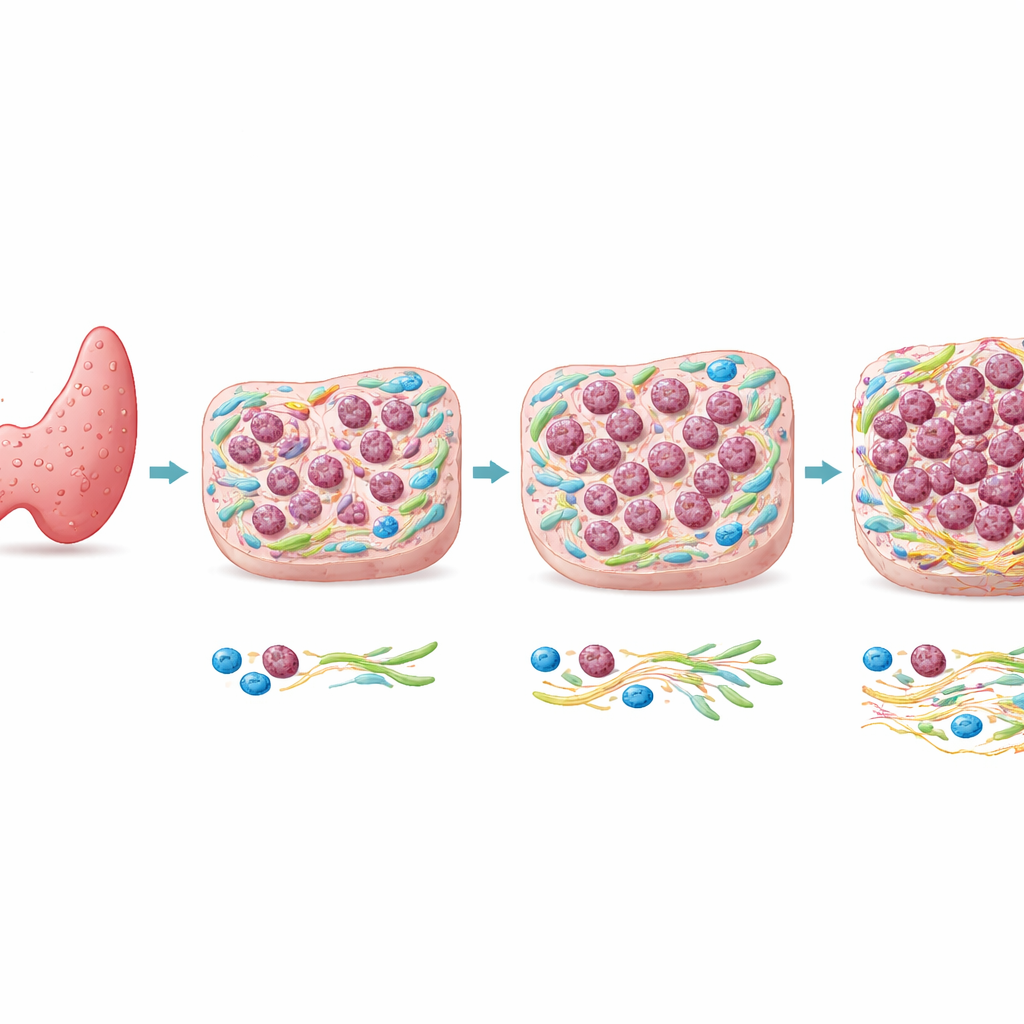
De um tumor comum a um raro assassino
A maioria dos cânceres de tireoide são carcinomas papilíferos da tireoide (CPT), que em geral crescem devagar e apresentam desfechos excelentes. O carcinoma anaplásico da tireoide (CAT), em contraste, é raro, mas frequentemente fatal em poucos meses. Estudos genéticos mostraram que CAT e áreas vizinhas de CPT no mesmo paciente frequentemente compartilham muitas das mesmas mutações no DNA, incluindo alterações em genes de câncer bem conhecidos. Essa semelhança sugere que apenas os genes podem não explicar por que apenas algumas regiões de um tumor tornam-se anaplásicas. Os autores, portanto, focaram no que acontece na paisagem tecidual ao redor das células — o microambiente tumoral — para ver se condições locais ajudam a impulsionar essa mudança perigosa.
Uma nova maneira de mapear o câncer no local
A equipe desenvolveu um ensaio de imunofluorescência espacial (SPI), um tipo de microscopia multicor que mede o brilho de proteínas específicas em pequenos mosaicos definidos por toda uma seção de tecido. Eles centraram esse método no CD109, uma proteína de superfície que identificaram como marcador de comportamento maligno no tecido tireoidiano, e em CK8/18, uma proteína característica das células tumorais papilíferas comuns. Calculando a razão entre CD109 e CK8/18 em centenas de pequenas regiões, eles geraram mapas codificados por cores que separaram áreas claramente CPT de áreas claramente CAT e, crucialmente, revelaram zonas intermediárias onde ambos os marcadores se sobrepunham. Em vez de uma fronteira nítida, a transição de câncer papilífero para anaplásico apareceu como um contínuo gradual e em manchas.
Cinco zonas ao longo de um caminho de mudança
Para entender melhor esse contínuo, os pesquisadores dividiram o tecido em cinco regiões, do CPT puro ao CAT totalmente desenvolvido. Em seguida, examinaram muitas proteínas adicionais que informam sobre identidade celular, crescimento, movimento e o tecido de suporte. Ao longo dessas regiões, características epiteliais clássicas, como E-caderina e CK8/18, declinaram de forma consistente, enquanto marcadores ligados à motilidade celular e mudança de forma, como vimentina, aumentaram. Proteínas que indicam divisão celular rápida cresceram nas zonas mais anaplásicas. Ao mesmo tempo, as células de suporte ao redor — fibroblastos associados ao câncer — e células imunes, especialmente certos macrófagos, tornaram-se mais numerosas e mais ativadas, e as proteínas que produziam aumentaram.
Quando o andaime tumoral vira hostil
Uma mudança marcante ocorreu no andaime do tumor, ou matriz extracelular. Nas regiões anaplásicas, células com aspecto de fibroblasto depositaram mais colágenos tipos III e VI e uma proteína de matriz chamada TGFBI, e essas fibras ficaram mais espessas, mais emaranhadas e orientadas em muitas direções em vez de linhas suaves e paralelas. Essa malha reorganizada provavelmente torna o tecido mecanicamente mais rígido. Nestas zonas mais rígidas, uma proteína de sinalização sensível à pressão chamada YAP estava mais ativa tanto em células cancerosas quanto nas células de suporte. As mesmas áreas mostraram mais sinais de dano ao DNA e de uma forma de morte celular inflamatória, junto com liberação de proteínas S100 que podem atuar como sinais de perigo e inflamar ainda mais o ambiente. Os autores propõem que essa combinação de compressão, morte celular e inflamação crônica favorece a sobrevivência e disseminação de células já mutadas que conseguem resistir ao estresse e passar por uma transição semelhante à epitélio–mesênquima.
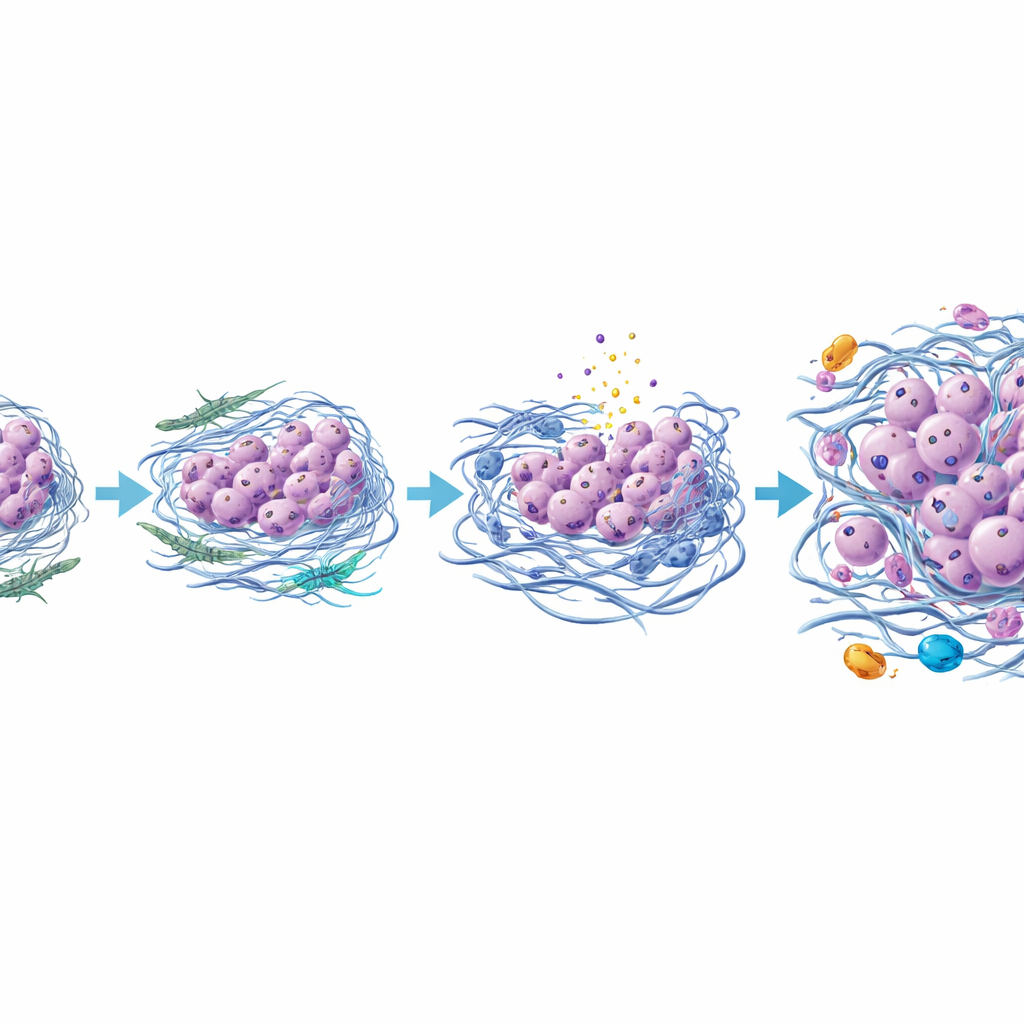
Uma nova imagem de como um tumor de tireoide se torna letal
Ao reunir essas descobertas, o estudo sugere que o câncer anaplásico da tireoide surge não apenas de mutações genéticas adicionais, mas de um bairro remodelado ao redor do tumor. À medida que as células tumorais papilíferas e as células de suporte próximas interagem, alguns fibroblastos evoluem para um tipo mais agressivo que espessa e endurece a matriz circundante, esmaga células vulneráveis até a morte e atrai células imunes inflamatórias. As células cancerosas sobreviventes, mais resilientes, gradualmente perdem suas características originais da tireoide e adotam uma identidade mais móvel e invasiva, eventualmente formando um tumor anaplásico. Embora esse trabalho se baseie em um único caso bem estudado e precise de confirmação em mais pacientes, ele introduz uma poderosa ferramenta de imagem e um modelo detalhado no qual mirar as células de suporte do tumor, a matriz ou sinais inflamatórios poderia ajudar a prevenir ou atrasar uma das transformações mais temidas no câncer de tireoide.
Citação: Cohen, T., Suzuki, K., Matsuda, K. et al. Visualizing malignant progression: in situ CD109-based spatial immunofluorescence assay delineates papillary to anaplastic thyroid carcinoma transformation within the tumor microenvironment. Sci Rep 16, 8682 (2026). https://doi.org/10.1038/s41598-026-41927-z
Palavras-chave: carcinoma anaplásico da tireoide, carcinoma papilífero da tireoide, microambiente tumoral, rigidez da matriz extracelular, imunofluorescência espacial