Clear Sky Science · pt
Análise de vesículas extracelulares derivadas de células epiteliais brônquicas usando citometria de fluxo convencional, de imagem e em nanoscale
Por que as bolhas minúsculas nos pulmões importam
Nossos pulmões são revestidos por células que estão constantemente se comunicando com o sistema imune, especialmente quando inalamos poeira, poluição ou germes. Grande parte dessa “conversa” ocorre por meio de bolhas microscópicas chamadas vesículas extracelulares — pacotes de lipídios e proteínas liberados pelas células. Essas vesículas podem agravar ou atenuar doenças pulmonares e, um dia, podem servir como sinais precoces para condições como asma, doença pulmonar obstrutiva crônica (DPOC) e fibrose. Este estudo explora a melhor forma de medir essas partículas elusivas usando diferentes tipos de instrumentos avançados baseados em laser, com vistas a tornar tais medições práticas para pesquisa e futuros testes clínicos.
Mensagens invisíveis das células das vias aéreas
Vesículas extracelulares (VEs) são minúsculos pacotes envoltos por membrana liberados por quase todas as células em fluidos como sangue, urina e o fino revestimento líquido das vias aéreas. VEs de células epiteliais brônquicas humanas — as células que revestem os tubos respiratórios — já foram associadas a vários processos pulmonares: podem influenciar o desenvolvimento de alergias, ajudar a combater infecções pulmonares, moldar a estrutura das vias aéreas na DPOC e até limitar a formação de cicatrizes no tecido pulmonar. Por carregarem fragmentos de proteínas, lipídios e material genético de suas células de origem, as VEs podem agir como impressões digitais da saúde ou da doença pulmonar e, eventualmente, serem usadas como tratamentos. O desafio é que elas são extremamente pequenas, altamente heterogêneas e estão em baixas quantidades, o que torna difícil vê‑las e contá‑las com precisão.
Avançando além de testes lentos e fragmentados
Tradicionalmente, cientistas têm se apoiado em vários métodos separados para estudar VEs. Ultracentrifugação ou cromatografia por exclusão de tamanho são usados para isolá‑las; análise de rastreamento de nanopartículas mede seu movimento para estimar tamanho e quantidade; e microscópios eletrônicos fornecem imagens detalhadas. Embora poderosos, esses métodos são lentos, trabalhosos e não ideais para uso rotineiro ou clínico. Fundamentalmente, eles têm dificuldade em identificar quais proteínas específicas cada vesícula carrega. A citometria de fluxo — uma tecnologia amplamente usada para analisar sangue e células imunes — oferece uma alternativa mais ágil. Ela faz as partículas passarem uma a uma por lasers, medindo a dispersão de luz (relacionada ao tamanho) e a fluorescência (proveniente de corantes ou anticorpos). Projetos recentes de instrumentos prometem empurrar a citometria de fluxo até a escala das menores vesículas, levantando a possibilidade de uma única máquina dimensionar, contar e caracterizar VEs em uma única corrida.
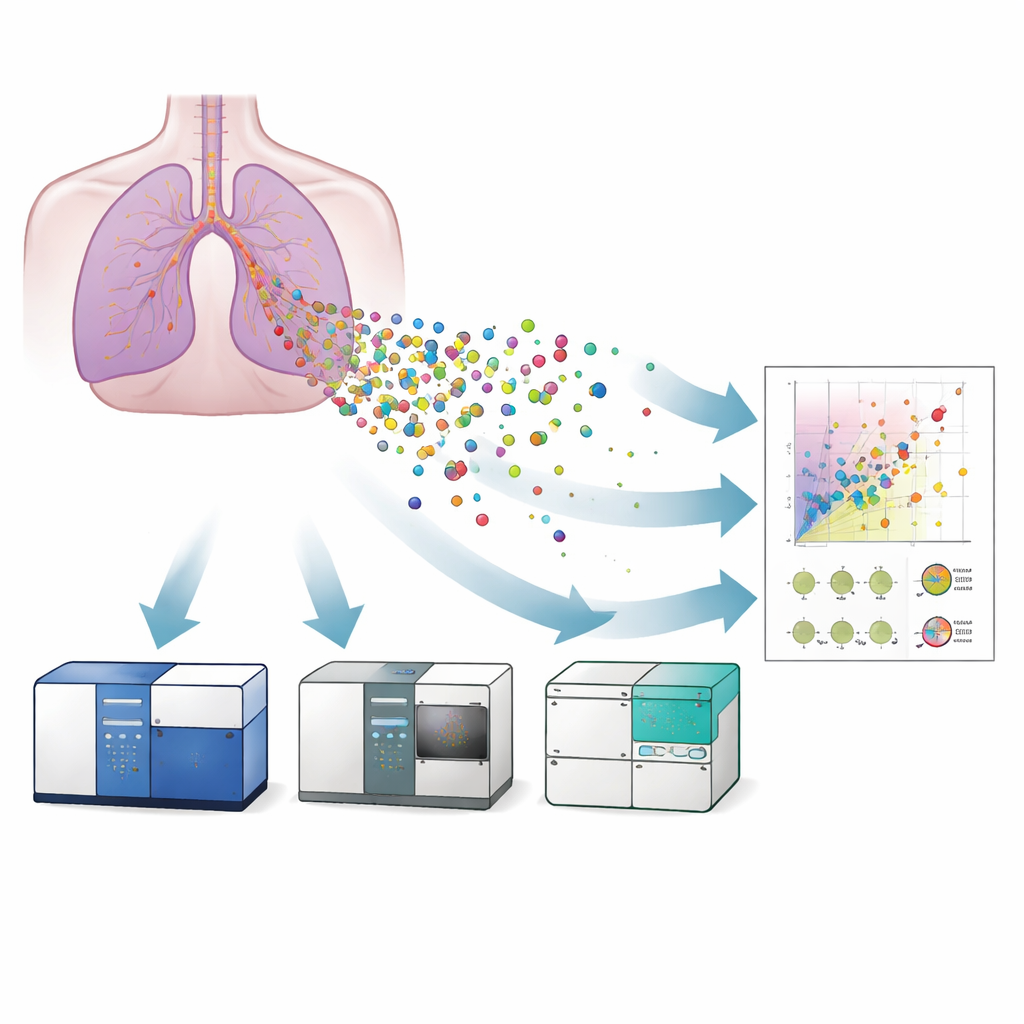
Três máquinas, um objetivo
Os pesquisadores compararam três variantes de citometria de fluxo para estudar VEs liberadas por um modelo cultivado em laboratório do epitélio brônquico humano: um citômetro de fluxo convencional, um citômetro de fluxo por imagem e um citômetro de fluxo em nanoscale. Primeiro, confirmaram a presença e a aparência típica das vesículas usando microscopia eletrônica e microscopia de super‑resolução, que também mostraram que as vesículas carregavam proteínas de superfície conhecidas como tetraspaninas (CD9, CD63, CD81) — marcadores padrão usados para identificar VEs. Em seguida, usaram esferas de referência cuidadosamente calibradas e padrões de lipossomos para traduzir os sinais de luz de cada instrumento em tamanhos aproximados de vesículas. O citômetro de fluxo nanoscale podia detectar vesículas de cerca de 40 nanômetros, o instrumento de imagem até cerca de 55 nanômetros, enquanto o equipamento convencional tinha dificuldade abaixo de aproximadamente 120 nanômetros. Isso significou que apenas os sistemas mais sensíveis conseguiam captar totalmente as vesículas menores e, potencialmente, as mais relevantes clinicamente.
Marcar e contar as vesículas
Para garantir que estavam medindo vesículas intactas e biologicamente ativas em vez de detritos, a equipe usou um corante chamado calceína‑AM. Esse corante só fluoresce depois de atravessar uma membrana intacta e ser processado por enzimas dentro da vesícula. Eles ajustaram cuidadosamente a concentração do corante para que marcasse as vesículas fortemente enquanto minimizava o sinal de fundo, escolhendo uma concentração que produziu respostas claras e lineares através de diluições das amostras. A calceína foi então combinada com anticorpos fluorescentes que se ligam às tetraspaninas na superfície das vesículas, permitindo que os instrumentos separassem vesículas que carregavam diferentes combinações desses marcadores. O grupo também mediu a sensibilidade de cada máquina a essas marcas fluorescentes — quantas moléculas de anticorpo precisavam estar presentes em uma vesícula para que ela pudesse ser detectada de forma confiável. A citometria de fluxo por imagem geralmente ofereceu limites de detecção menores do que o citômetro convencional, sendo mais adequada para partículas com apenas um pequeno número de proteínas marcadoras.
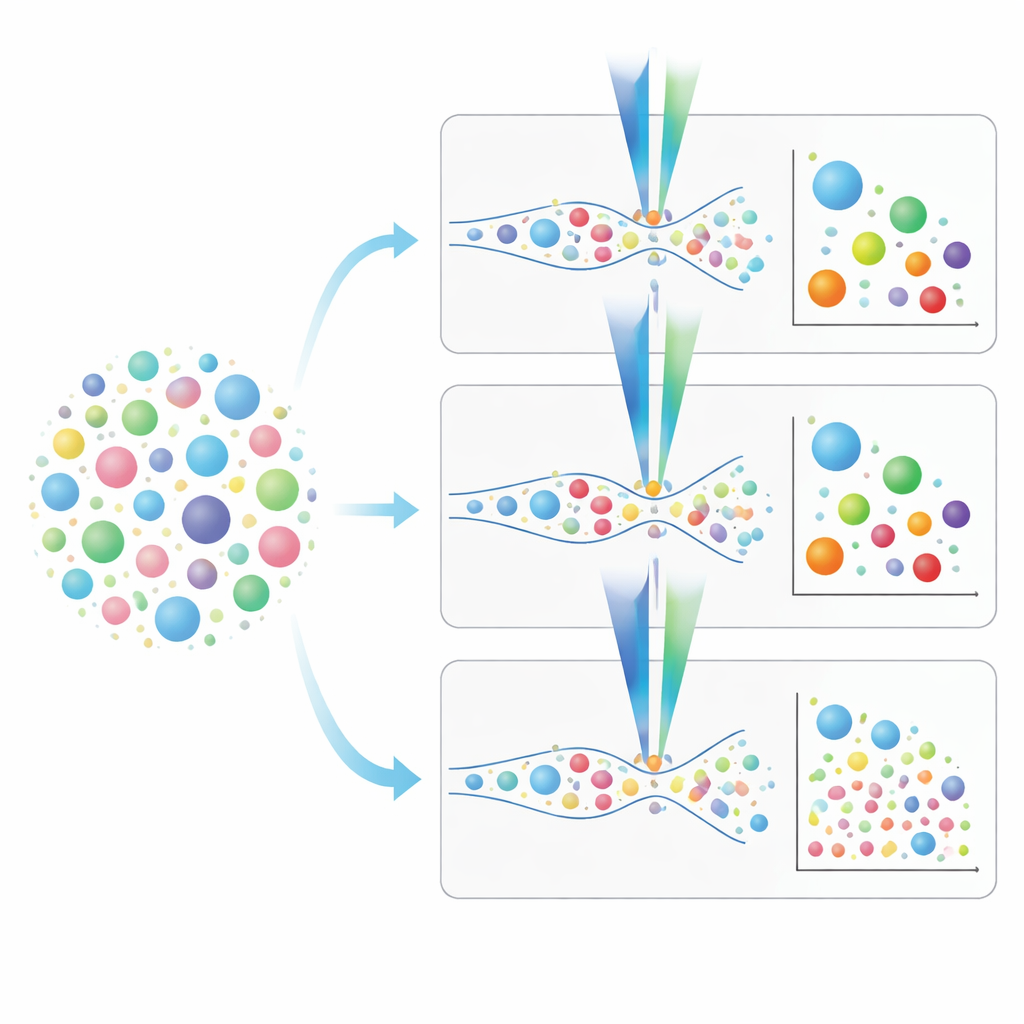
Escolhendo a ferramenta certa para estudos de vesículas pulmonares
Dessa comparação direta surge um quadro prático. Citômetros de fluxo convencionais são mais rápidos e podem analisar amostras sem isolamento prévio, mas perdem muitas das vesículas menores que podem portar sinais cruciais de doença. Citômetros de fluxo por imagem e em nanoscale, embora mais lentos e, no caso do instrumento nanoscale, mais dependentes de limpeza prévia da amostra, conseguem ver tamanhos muito menores e possibilitam uma caracterização mais rica dos marcadores de superfície das vesículas. Os autores descrevem estratégias passo a passo de coloração e calibração, enfatizam a importância de conhecer o limite de detecção de cada marca fluorescente e mostram como evitar sinais enganosos de corantes que também marcam fragmentos ou partículas não vesiculares. Em termos simples, eles fornecem um roteiro para os pesquisadores decidirem qual instrumento e protocolo melhor se ajustam às questões sobre VEs pulmonares, ajudando a aproximar o campo do uso desses mensageiros microscópicos como ferramentas práticas para entender, diagnosticar e, eventualmente, tratar doenças respiratórias.
Citação: Hopkins, G., Browne, W., Tucis, D. et al. Bronchial epithelial cell-derived extracellular vesicle analysis using conventional, imaging, and nanoscale flow cytometry technologies. Sci Rep 16, 11162 (2026). https://doi.org/10.1038/s41598-026-41848-x
Palavras-chave: vesículas extracelulares, epitélio pulmonar, citometria de fluxo, doença respiratória, análise de biomarcadores