Clear Sky Science · pt
Efeitos antagônicos de aminoácidos sustentam nano-ambientes abióticos em argila
Como bolsões minúsculos na argila podem nutrir a primeira química da vida
A vida pode não ter começado nos mares abertos, mas dentro de espaços inimaginavelmente pequenos entre camadas de minerais argilosos comuns. Este estudo explora como moléculas simples relacionadas aos aminoácidos atuais podem remodelar a argila em escala nanométrica, esculpindo compartimentos aconchegantes que aprisionam e organizam a química. Ao mostrar como diferentes aminoácidos ora fortalecem, ora desestruturam as camadas de argila, o trabalho sugere um modo natural pelo qual a Terra primitiva — ou outros mundos rochosos — poderia ter criado “laboratórios” em miniatura onde os blocos de construção da vida poderiam se montar.
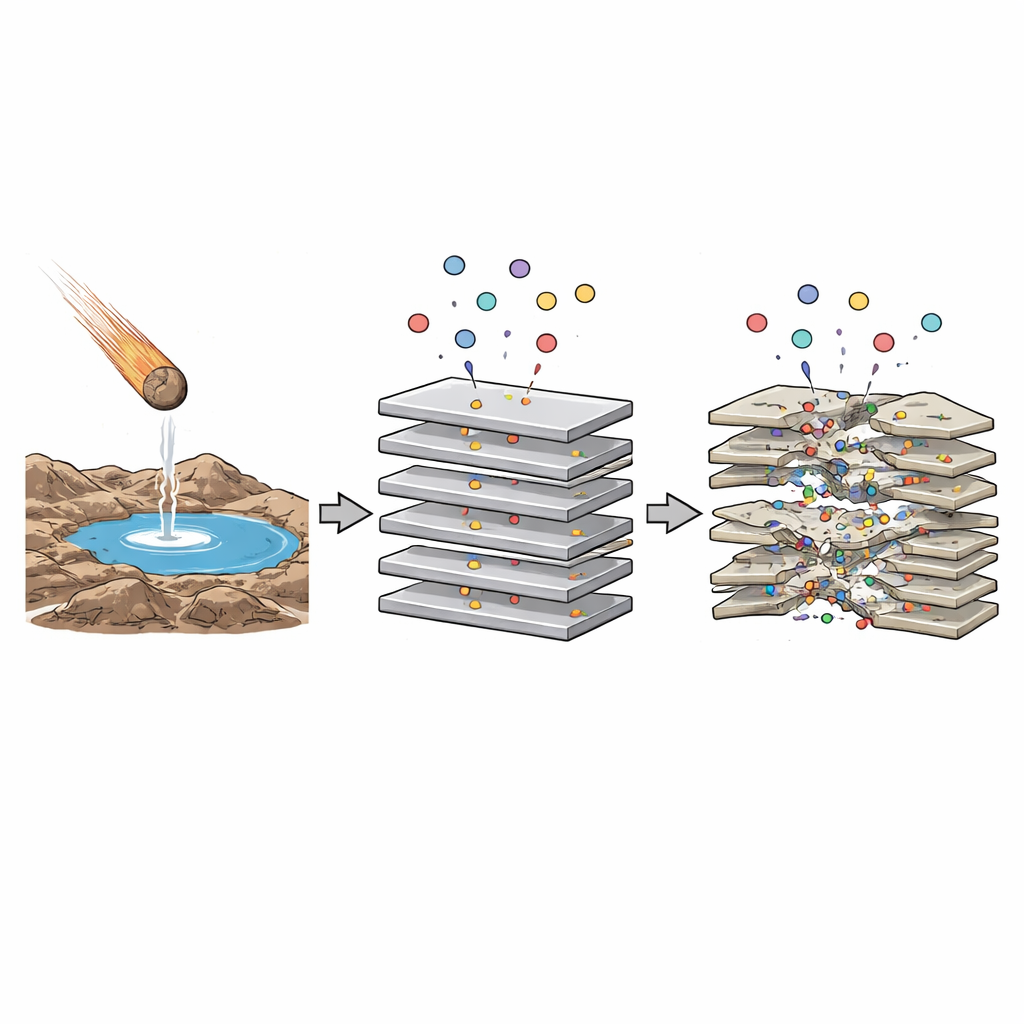
A promessa dos espaços ocultos
Cientistas suspeitam há muito que os minerais fizeram mais do que apenas ficar sob oceanos e lagoas primordiais: eles podem ter ajudado a montar as primeiras cadeias de moléculas. Em particular, argilas como a montmorilonita podem inchar e encolher conforme água e pequenas moléculas se inserem entre suas folhas empilhadas. Dentro dessas fendas estreitas, a água se comporta de forma diferente, forças elétricas são mais intensas, e reações difíceis na água comum podem tornar-se mais fáceis. Esses espaços confinados podem ajudar a ligar blocos simples — como aminoácidos e nucleotídeos — em cadeias mais longas, um passo-chave rumo à vida. Mas ambientes prebióticos reais eram caldeirões químicos com muitas moléculas orgânicas diferentes presentes ao mesmo tempo. Surge então uma pergunta: quando vários tipos de aminoácidos interagem com a argila juntos, eles se anulam entre si ou seus efeitos concorrentes podem, na verdade, criar ambientes mais ricos para a química?
Construtores amistosos e desestabilizadores travessos
Os pesquisadores focaram em uma forma de montmorilonita rica em cálcio e três aminoácidos. Dois, lisina e arginina, são aminoácidos usados em proteínas e familiares dos livros de biologia. O terceiro, ácido gama-aminobutírico (GABA), não é incorporado em proteínas modernas, mas é comum em meteoritos e, portanto, provavelmente foi entregue à Terra primitiva. Trabalhos anteriores mostraram que lisina e arginina se acomodam nos espaços entre as camadas de argila e se ligam firmemente, ajudando a manter as camadas ordenadas e relativamente planas. O GABA, por contraste, praticamente não adere — ainda que tenha um efeito desproporcional: ele curva e parcialmente descola as lâminas de argila, criando cavidades em escala nanométrica. Este estudo investigou o que acontece quando uma pequena quantidade de aminoácido do tipo proteico é misturada com um grande excesso de GABA, simulando uma lagoa fortemente semeada com orgânicos extraterrenos.
Observando as transformações das camadas de argila
Para rastrear essas mudanças, a equipe combinou várias técnicas que revelam diferentes aspectos da argila. A espectroscopia infravermelha sondou como as partes silício–oxigênio da estrutura vibram, o que muda quando camadas são distorcidas, separadas ou preenchidas por espécies diferentes. A difração de raios X mediu o espaçamento e a ordenação das folhas empilhadas, tanto em amostras secas quanto após reidratação com vapor d’água. A análise termogravimétrica monitorou quão fortemente as moléculas orgânicas e a água eram retidas na argila. Finalmente, a microscopia eletrônica de alta resolução forneceu imagens diretas das estruturas em camadas e de quaisquer cavidades minúsculas entre elas. Juntas, essas ferramentas permitiram aos autores separar as ações estabilizadoras da lisina e da arginina da influência disruptiva do GABA, mesmo quando todos estavam presentes na mesma mistura.
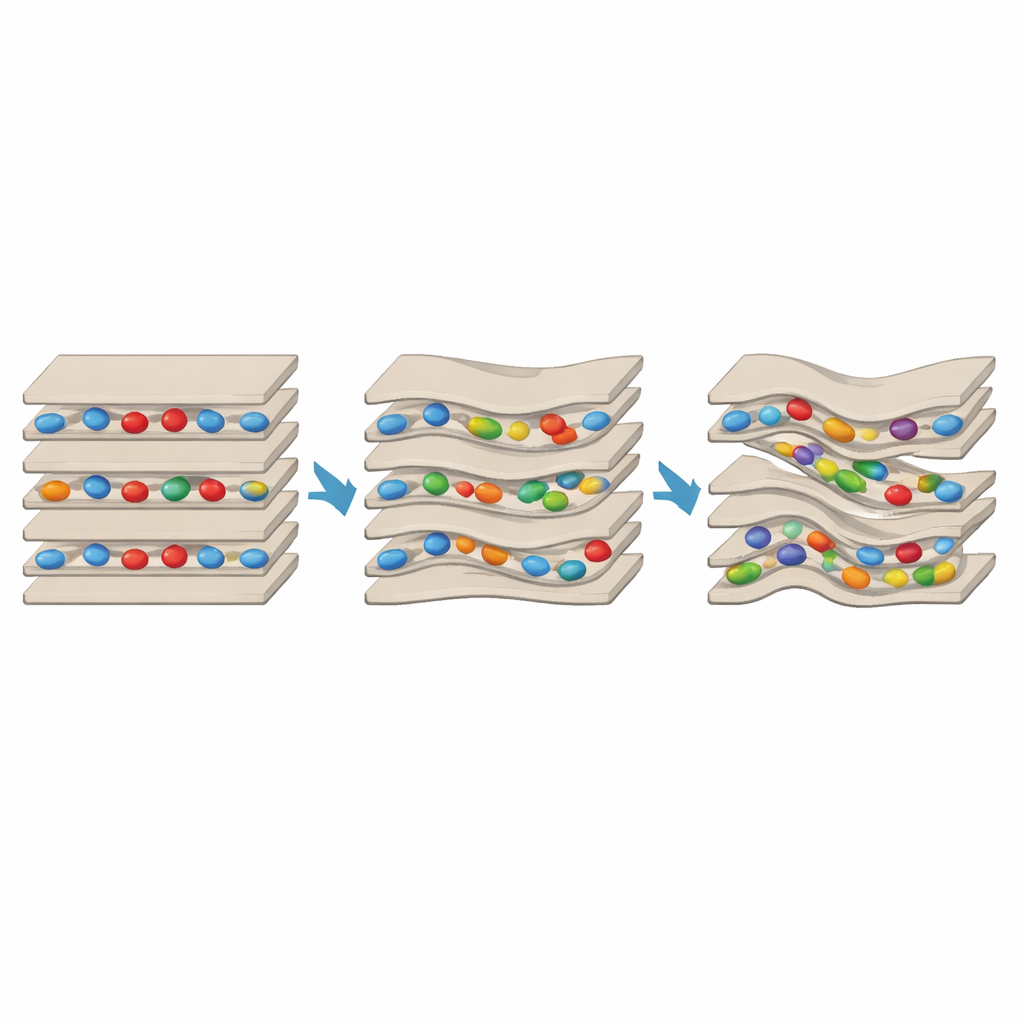
Um yin–yang nanométrico na argila
Os resultados revelam um empurra-e-puxa marcante. Quando apenas lisina ou arginina estavam presentes, elas se alojavam nos espaços intercamadas, agindo como travessas que unem uma folha à seguinte. Isso reduziu a capacidade da argila de inchar com água e tornou a estrutura mais ordenada e resistente ao descolamento. Mas quando GABA foi adicionado em grande excesso, ele superou esse efeito estabilizador em muitas regiões. Assinaturas espectroscópicas mostraram a presença de domínios parcialmente esfoliados, e padrões de raios X indicaram mais desordem e alinhamento reduzido das camadas. A microscopia eletrônica foi além, revelando pilhas altamente distorcidas com claras nanocavidades embutidas no meio das camadas — pequenos bolsões de alguns nanômetros que não apareciam no controle ou nas amostras apenas com aminoácidos proteicos. Importante: regiões com camadas pontes, fortemente mantidas, coexistiam ao lado de regiões com camadas distorcidas e ricas em cavidades no mesmo grão de argila, demonstrando que ambos os efeitos podem operar lado a lado.
Nano-compartimentos naturais para a química primordial
Para um público não especializado, a mensagem principal é que misturas simples de aminoácidos podem esculpir a argila em um mosaico de pequenos compartimentos com propriedades distintas. Aminoácidos usados em proteínas ajudam a manter as camadas juntas, enquanto o GABA de origem meteórica as separa sutilmente e esculpe nanocavidades. Esses bolsões confinados provavelmente abrigam água e moléculas dissolvidas em condições distintas do ambiente circundante, potencialmente favorecendo reações como a formação de polímeros, centrais para a origem da vida. Como meteoritos entregam abundantes aminoácidos não proteicos a mundos ricos em argila, esse “yin–yang” antagônico entre moléculas estabilizadoras e disruptivas pode ser um caminho comum para planetas rochosos e asteroides gerarem e sustentarem nano-ambientes diversos onde uma bioquímica primitiva poderia começar.
Citação: Bezaly, O.R., King, H.E. & Petrignani, A. Antagonistic effects of amino acids support abiotic nano-environments in clay. Sci Rep 16, 8959 (2026). https://doi.org/10.1038/s41598-026-41502-6
Palavras-chave: origens da vida, química prebiótica, minerais de argila, aminoácidos, nanoconfinamento