Clear Sky Science · pt
Classificação pan‑câncer de lâminas congeladas usando um vision transformer com mistura suave de especialistas sob supervisão fraca
Por que isso importa na sala de cirurgia
Quando cirurgiões removem um tumor suspeito, frequentemente têm apenas minutos para descobrir se todo o câncer foi retirado. Patologistas se apressam para examinar uma fatia de tecido rapidamente congelada e dar uma resposta enquanto o paciente ainda está na mesa. Esse processo sob alta pressão pode ser prejudicado por lâminas borradas, tumores sutis e limites de tempo. O estudo descrito aqui investiga como um sistema de inteligência artificial (IA) pode ajudar patologistas a distinguir rápida e confiavelmente tecido inofensivo de perigoso em muitos órgãos diferentes, usando equipamentos realistas para hospitais do dia a dia.
Um teste rápido com desafios embutidos
A análise de lâminas congeladas é um pilar da cirurgia moderna: um pedaço fino de tecido é congelado, fatiado, corado e observado ao microscópio para julgar se é benigno ou maligno e se a margem cirúrgica está limpa. Ao contrário das lâminas permanentes de laboratório, as lâminas congeladas frequentemente apresentam fissuras, dobras e coloração desigual. Diferentes patologistas podem discordar em casos limítrofes, e o relógio está sempre correndo. Esses problemas são especialmente graves em hospitais menores ou sobrecarregados, onde apenas alguns especialistas cobrem muitos tipos de câncer. Os autores argumentam que um assistente computacional robusto poderia tornar as decisões sobre lâminas congeladas mais consistentes, rápidas e amplamente disponíveis.
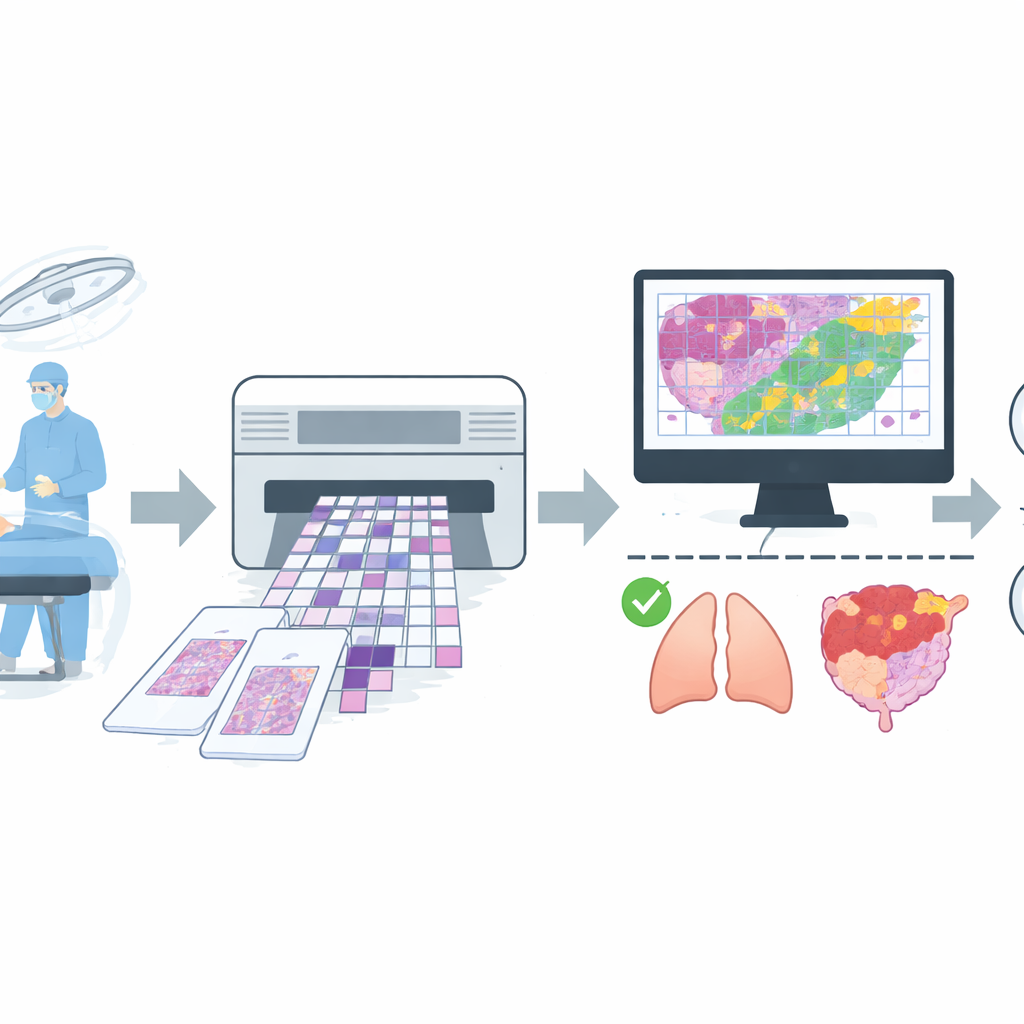
Construindo um conjunto de imagens amplo e realista
Para treinar esse assistente, a equipe reuniu uma grande coleção de imagens digitais de operações de rotina em um hospital importante. Eles coletaram 4.754 imagens de lâminas inteiras de tecido congelado de mais de 2.600 pacientes e então aplicaram regras rígidas de qualidade para remover lâminas com artefatos severos ou diagnósticos incertos. O conjunto de dados final continha 4.667 lâminas, cada uma rotulada simplesmente como benigna ou maligna com base no acordo entre a leitura rápida da lâmina congelada e o relatório posterior e mais cuidadoso da lâmina permanente. As lâminas cobriram sítios comuns como pulmão, mama, tireoide, linfonodos e órgãos reprodutores femininos, além de um grupo misto de locais menos frequentes como estômago, fígado e pele. Os dados foram divididos em grupos separados para treino, ajuste fino e teste final, com cuidado para que imagens do mesmo paciente nunca aparecessem em mais de um grupo.
Como a IA aprende a partir de pistas fracas
Os pesquisadores construíram seu modelo sobre uma classe de rede neural chamada Vision Transformer, que se destaca em encontrar padrões em imagens grandes. Cada imagem gigante de tecido foi automaticamente cortada em muitos blocos menores e patches para que pudesse ser processada em hardware gráfico padrão. Uma inovação chave foi substituir parte da rede por uma “mistura suave de especialistas”, um conjunto de muitos ramos especializados pequenos que focam em diferentes padrões visuais. Em vez de ligar e desligar especialistas, o sistema mistura suas contribuições de forma contínua, o que estabiliza o treinamento e aproveita melhor os dados limitados. Como os patologistas não desenharam contornos ao redor dos tumores, o modelo teve de aprender com supervisão fraca: ele sabia apenas se uma lâmina inteira era benigna ou maligna. Uma estratégia de aprendizado por múltiplas instâncias promoveu os patches mais suspeitos dentro de uma lâmina maligna para servir como exemplos positivos, permitindo que a rede gradualmente se concentrasse nas regiões mais informativas.
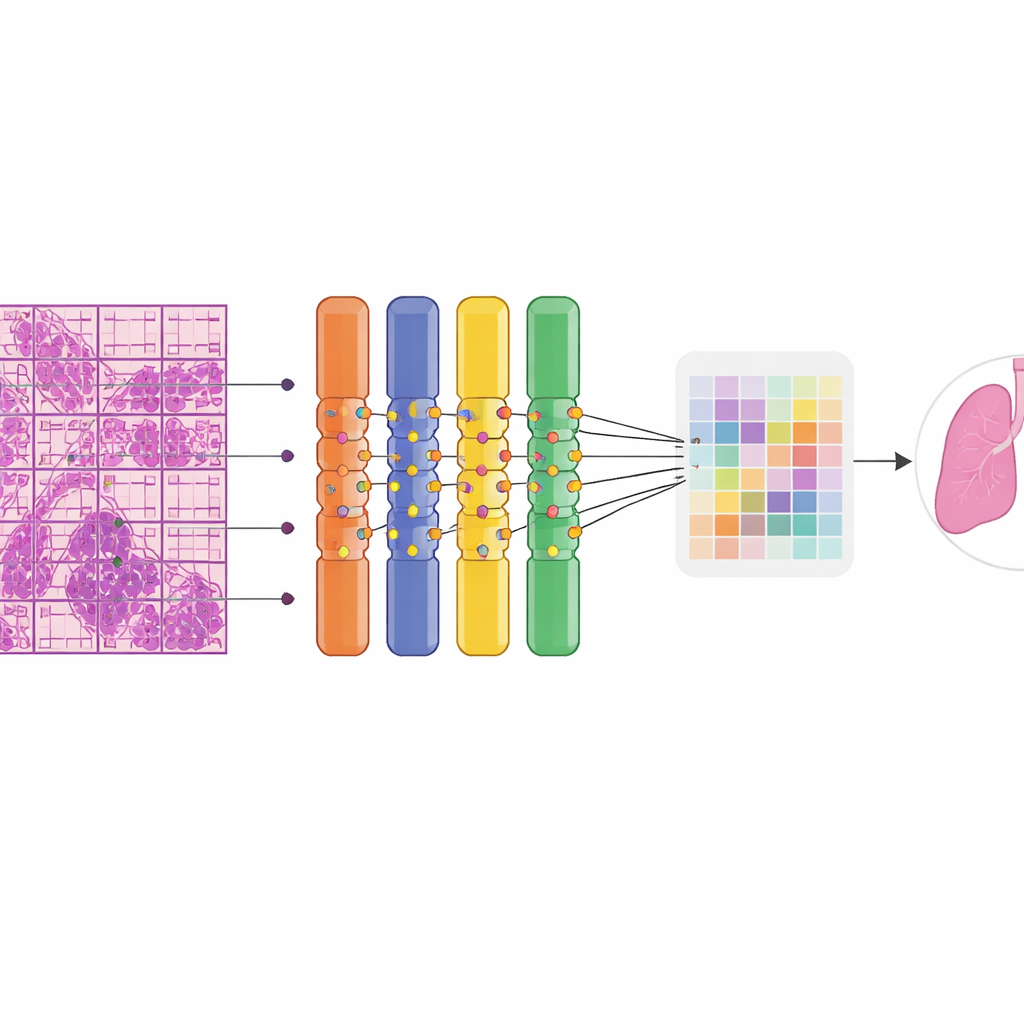
Qual o desempenho do sistema na prática
Ao ser testada em 669 lâminas inéditas, a IA distinguiu tecido benigno de maligno com alta acurácia. Ela classificou corretamente cerca de 90% dos casos no geral e mostrou excelente capacidade de separar os dois grupos através de limiares de probabilidade. Sensibilidade, a chance de sinalizar corretamente uma lâmina realmente maligna, ficou em torno de quatro em cada cinco, enquanto especificidade, a chance de tranquilamente declarar uma lâmina benigna como benigna, foi ainda maior. Importante, o desempenho permaneceu forte entre órgãos: detectou perfeitamente todos os casos malignos de pulmão e mama no conjunto de teste e teve bom desempenho em grupos mais raros, como tumores anexiais femininos e órgãos mistos “outros”. Mapas de calor coloridos sobrepostos às lâminas mostraram que a atenção do modelo se concentrava em regiões que patologistas especialistas reconheceram como tumor, incluindo focos metastáticos em linfonodos, enquanto em grande parte ignorava estruturas normais. O sistema rodou de forma eficiente, necessitando de menos de 5 GB de memória, tornando‑o adequado para uso em placas gráficas comumente disponíveis em vez de clusters caros.
Limites, tropeços e espaço para melhorar
Os autores também examinaram onde a IA falhou. Resultados falso‑negativos frequentemente envolviam células cancerosas extremamente esparsas, áreas de digitalização borradas ou inflamação intensa que disfarçava ninhos malignos. Falsos positivos tendiam a surgir em condições benignas que imitam câncer ao microscópio, como proliferações reativas ou tecido congelado distorcido. Como os fluxos de trabalho cirúrgicos de rotina não incluem contornos detalhados das regiões tumorais, a equipe não pôde quantificar exatamente o quanto os mapas de calor correspondiam às marcações de especialistas, baseando‑se em revisão qualitativa. Alguns tipos de órgão, como língua ou certos tumores de tecido mole, continuaram subrepresentados, indicando que coleções maiores e multicêntricas serão necessárias para estender o alcance do sistema.
O que isso pode significar para pacientes e hospitais
No geral, o estudo demonstra que um sistema de IA cuidadosamente projetado pode auxiliar com precisão e interpretabilidade em uma tarefa central da patologia cirúrgica: decidir, em tempo real, se o tecido é benigno ou maligno em muitos tipos de órgãos. Ao operar com apenas rótulos em nível de lâmina, rodar em hardware amplamente disponível e destacar áreas suspeitas para revisão humana, o modelo oferece um caminho prático rumo a decisões de lâminas congeladas mais consistentes. Para pacientes, isso pode se traduzir em cirurgias melhor informadas em uma única operação; para hospitais, especialmente os com número limitado de especialistas, aponta para um futuro em que ferramentas digitais avançadas ajudam a oferecer cuidado oncológico de alta qualidade de forma mais equitativa.
Citação: Wu, J., Yang, M., Li, J. et al. Pan-cancer frozen section classification using a soft mixture of experts vision transformer under weak supervision. Sci Rep 16, 10297 (2026). https://doi.org/10.1038/s41598-026-40924-6
Palavras-chave: lâmina congelada, patologia digital, diagnóstico de câncer, vision transformer, aprendizado fraco supervisionado