Clear Sky Science · pt
ABE9 fundido à Cas9 nickase SpRY permite geração precisa de modelos murinos sem alterações colaterais
Ferramentas mais afiadas para construir modelos de doença melhores
Muitas doenças graves são causadas por “typos” de uma única letra no nosso DNA. Para entender e, eventualmente, tratar essas condições, pesquisadores frequentemente criam camundongos que carregam as mesmas mutações que pacientes humanos. Mas reescrever o DNA de forma tão precisa é surpreendentemente difícil: métodos mais antigos podem deixar cicatrizes no genoma, introduzir mutações extras e confundir os resultados experimentais. Este estudo apresenta uma ferramenta de edição gênica refinada, chamada ABE9-SpRY, projetada para trocar uma letra específica do DNA deixando as letras vizinhas — e o restante do genoma — em grande parte intactos.
De cortes pesados a ajustes sutis no DNA
A edição CRISPR-Cas9 tradicional funciona como uma tesoura molecular, cortando ambas as fitas do DNA. As células reparam essas quebras de forma imperfeita, frequentemente deixando pequenas inserções ou deleções que interrompem genes de maneiras imprevisíveis. Isso é útil para desligar genes, mas não para reproduzir uma mutação causadora de doença com precisão. Editores de base, por outro lado, não cortam o DNA. Em vez disso, eles empurram quimicamente uma letra do DNA para outra — aqui, mudando A para G — mantendo a dupla hélice intacta. Essa abordagem reduz dramaticamente grandes deleções e rearranjos, mas editores de adenina anteriores ainda sofriam de três problemas principais: às vezes editavam letras vizinhas “bystander”, só podiam alcançar locais de DNA próximos a tags de sequência específicas curtas e, ocasionalmente, causavam edições em locais não intencionais do genoma.
Projetando um lápis molecular mais seletivo
Os pesquisadores se propuseram a enfrentar as três limitações simultaneamente. Começaram com o ABE9, uma variante mais nova de editor de base que concentra sua atividade em uma faixa muito estreita do DNA, reduzindo tanto a “janela de edição” que bem menos letras vizinhas são alteradas acidentalmente. Em seguida, fundiram o ABE9 a uma Cas9 nickase engenheirada chamada SpRY. Ao contrário da Cas9 padrão, que requer uma tag rígida “NGG” ao lado do sítio alvo, o SpRY pode reconhecer um conjunto muito mais amplo de sequências de DNA. Isso torna possível alcançar posições relacionadas a doenças no genoma que antes eram inacessíveis. A ferramenta resultante, ABE9-SpRY, foi projetada para ser tanto altamente precisa quanto muito mais flexível quanto aos locais onde pode atuar.
Testando o novo editor em células e embriões
Para verificar se o ABE9-SpRY correspondia ao projeto, a equipe o comparou com um editor mais agressivo e amplamente usado chamado ABE8e-SpRY. Eles miraram quatro posições relevantes para doenças em genes que codificam canais iônicos (TPC1, TPC2 e TRPM4), que desempenham papéis importantes nas funções cardíaca e hepática. Em células nervosas de camundongo cultivadas em laboratório, o ABE8e-SpRY editou a letra alvo com mais eficiência, mas também alterou muitas bases próximas. O ABE9-SpRY, em contraste, produziu menos edições no total, mas uma fração muito maior de resultados “limpos” — leituras nas quais apenas a letra pretendida foi alterada, sem mutações extras na região local. O mesmo padrão foi observado em embriões de camundongo. Quando os pesquisadores injetaram os componentes de edição em óvulos fertilizados, o ABE8e-SpRY frequentemente converteu quase todas as cópias do gene alvo, porém com muitas alterações colaterais. O ABE9-SpRY editou menos cópias no total, mas onde atuou, a sequência de DNA foi tipicamente corrigida exatamente como planejado.
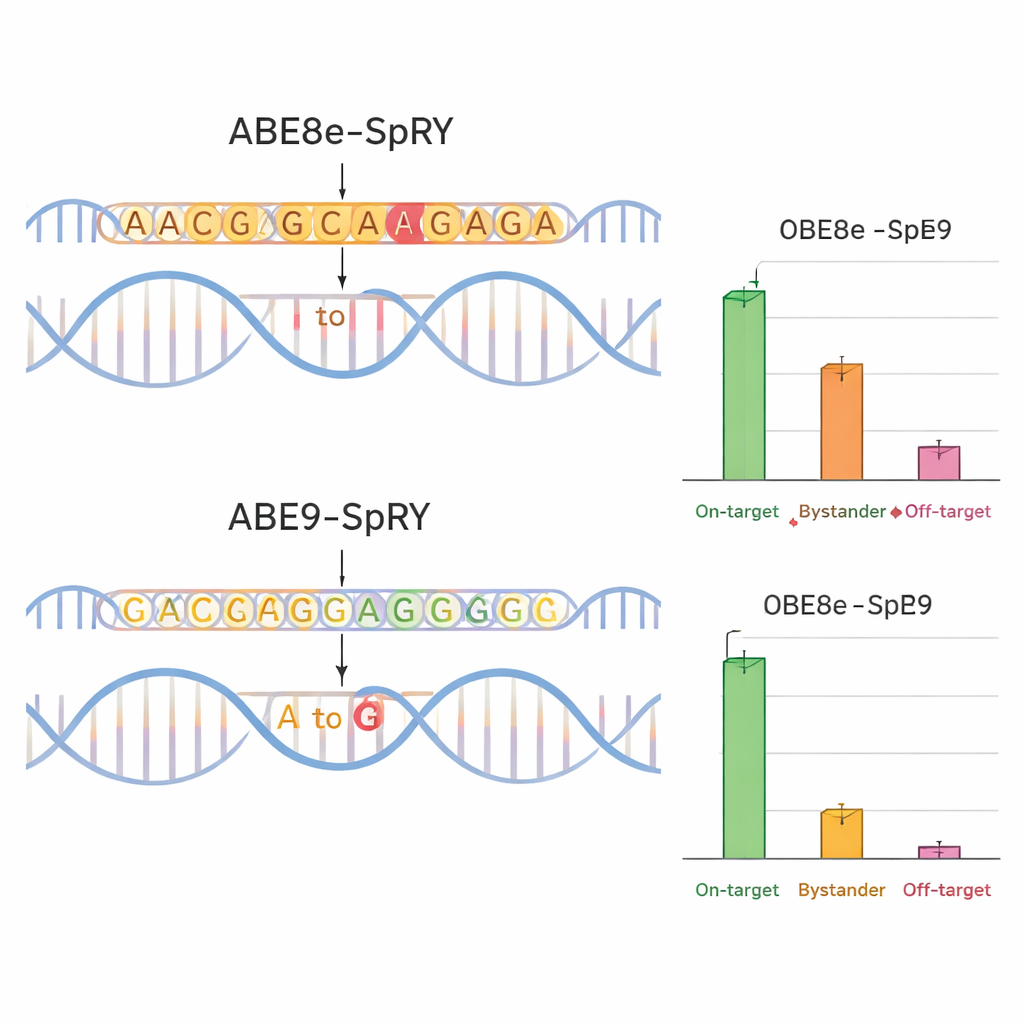
Edições mais limpas, menos efeitos colaterais
Precisão não é apenas sobre o bairro local do DNA. A equipe também examinou se o editor alterava regiões distantes do genoma. Usando previsões computacionais e sequenciamento direcionado, mediram mudanças fora do alvo em sítios prováveis de semelhança em embriões de camundongo. O ABE8e-SpRY frequentemente introduziu mudanças não intencionais de A para G nesses locais, às vezes em níveis surpreendentemente altos. O ABE9-SpRY mostrou muito menos desses eventos, com apenas raras edições fora do alvo e nenhuma atividade detectável em um teste especializado para danos ao DNA independentes de Cas9. Importante, quando o ABE9-SpRY foi usado isoladamente — não em testes agrupados — para introduzir duas mutações específicas em camundongos, ele gerou muitos animais fundadores nos quais a edição desejada estava presente em altos níveis e foi transmitida de forma confiável para a prole, novamente com mínimas alterações colaterais ou pequenas inserções e deleções.
Estendendo a edição precisa a células-tronco humanas
Como células-tronco específicas de pacientes são cada vez mais usadas para estudar doenças e testar fármacos, os pesquisadores também testaram o ABE9-SpRY em células-tronco pluripotentes induzidas humanas. Eles miraram a versão humana do gene TPC1 em uma posição equivalente a um dos sítios murinos. Usando um repórter fluorescente para enriquecer células editadas, constataram que o ABE8e-SpRY produziu taxas brutas de edição mais altas, mas novamente modificou várias bases vizinhas. O ABE9-SpRY editou menos alelos no total, mas a proporção de sequências perfeitamente editadas — uma mudança pretendida e nada mais — foi marcadamente maior, com menos inserções ou deleções disruptivas. Em trabalhos com células-tronco, onde clones individuais são expandidos para estudo detalhado, esse tipo de edição “limpa” costuma ser mais valioso que eficiência bruta.
Por que isso importa para pesquisas futuras sobre doenças
Para cientistas que buscam entender como a mudança de uma única letra do DNA leva à doença, mutações não intencionais extras podem ser profundamente enganosas. Este estudo mostra que o ABE9-SpRY, embora um pouco menos poderoso em termos de rapidez bruta de edição, pode escrever mudanças de uma única letra nos genomas de camundongos e em células-tronco humanas com precisão notável e ampla flexibilidade de alvo. Isso o torna um candidato promissor para construir modelos animais e celulares fiéis de distúrbios genéticos humanos, especialmente em situações nas quais até uma única mutação indesejada poderia confundir a biologia ou atrapalhar uma potencial terapia.
Citação: Ong, J.K., Bhunia, S., Hilbert, B. et al. ABE9 fused to SpRY Cas9 nickase enables precise generation of bystander free mouse models. Sci Rep 16, 7463 (2026). https://doi.org/10.1038/s41598-026-40642-z
Palavras-chave: edição de bases de adenina, modelos de doenças por CRISPR, genética de camundongos, efeitos fora do alvo, edição gênica em hiPSC