Clear Sky Science · pt
Ligação de baixa afinidade do anti-B7-H3 clone MJ18 ao B7-H3 murino não consegue induzir regressão tumoral
Por que isso importa para a pesquisa do câncer
A imunoterapia contra o câncer frequentemente depende de anticorpos — proteínas produzidas em laboratório projetadas para se ligar às células tumorais e ajudar o sistema imune a destruí-las. Um alvo promissor é uma molécula chamada B7-H3, abundante em muitos cânceres humanos e escassa em tecidos saudáveis. Este artigo examina de forma crítica um anticorpo de pesquisa amplamente usado, MJ18, que supostamente bloqueava B7-H3 em estudos com camundongos. Os autores constatam que o MJ18 mal se liga ao seu alvo pretendido e não retarda o crescimento tumoral, levantando dúvidas sobre como interpretar experimentos animais anteriores que usaram essa ferramenta.
A promessa de uma “bandeira” no câncer
O B7-H3 atraiu grande interesse porque age como um escudo molecular: tumores ricos nessa proteína tendem a ter menos células imunes agressivas em seu interior e estão associados a piores desfechos para pacientes. Em vários modelos de camundongo, a deleção do gene B7-H3 nas células tumorais libera um ataque imune mais forte e pode fazer os tumores encolherem ou desaparecerem. Essas observações impulsionaram esforços para desenvolver drogas, células imunes modificadas e conjugados anticorpo-droga que miram B7-H3 em cânceres humanos. No entanto, o modo exato como B7-H3 reduz a imunidade — e até qual receptor ele usa nas células imunes — continua incerto, especialmente porque as versões murina e humana de B7-H3 diferem estruturalmente.
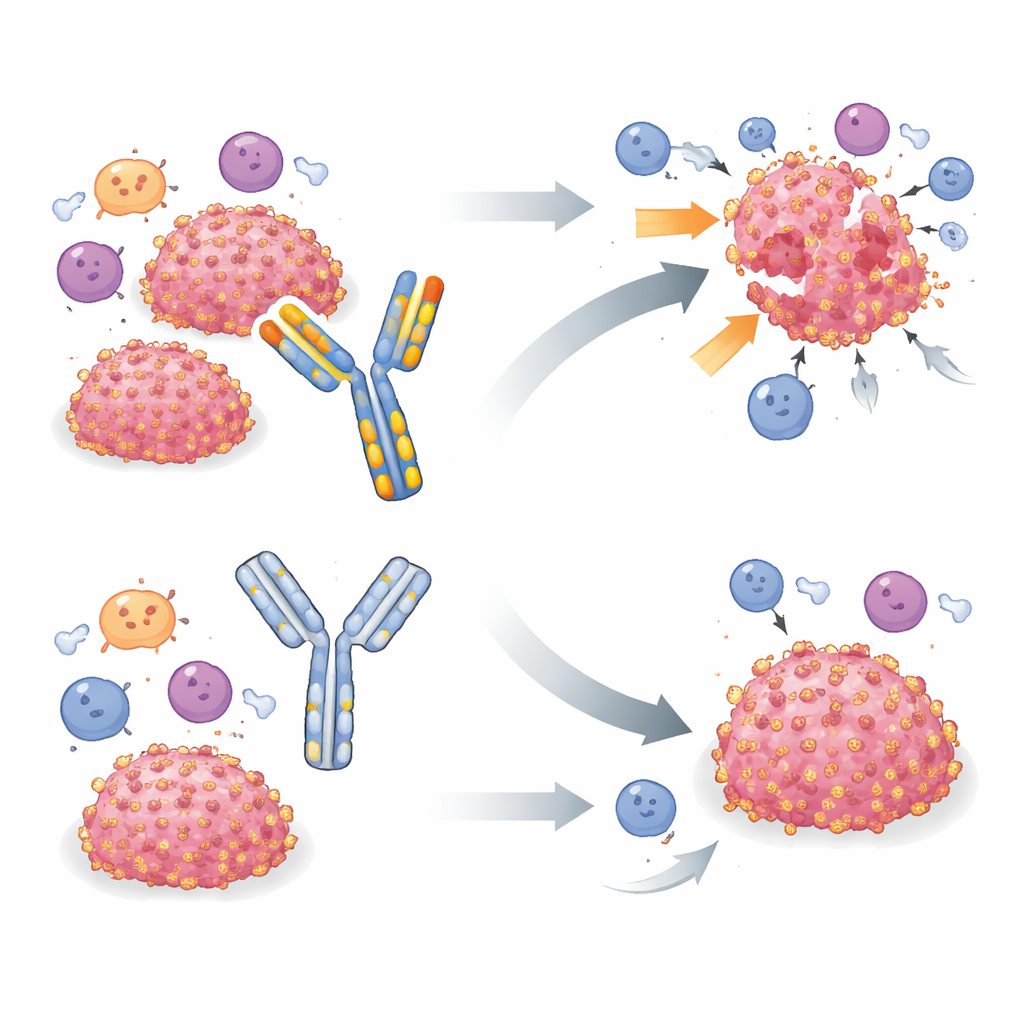
Uma ferramenta amplamente usada sob o microscópio
Para estudar B7-H3 em camundongos vivos, muitos grupos confiaram em um único anticorpo derivado de rato chamado MJ18, relatado como capaz de reconhecer o B7-H3 murino e bloquear sua atividade imunossupressora. Estudos anteriores usando MJ18 em vários modelos de doença, incluindo cânceres, frequentemente relataram crescimento tumoral mais lento e melhor sobrevida. A equipe atual inicialmente testou MJ18 em um modelo murino de rabdomiossarcoma, um câncer de tecido mole infantil onde B7-H3 já havia sido apontado como um importante mecanismo de escape. Quando o MJ18 não melhorou o controle tumoral, os pesquisadores ampliaram os testes para outros dois tipos de tumores B7-H3 positivos — cânceres pancreático e mamário — que são claramente sensíveis à deleção do gene B7-H3. Em todos os três modelos, eliminar B7-H3 nas células tumorais retardou ou eliminou os tumores de forma robusta, mas tratar os camundongos com MJ18 em doses e cronogramas semelhantes aos da literatura não teve impacto detectável no crescimento tumoral nem na sobrevida.
Testando se o MJ18 realmente acerta seu alvo
Os autores então fizeram uma pergunta básica que, surpreendentemente, nunca havia sido abordada de forma rigorosa: o MJ18 realmente se liga ao B7-H3 murino, e com que força? Usando citometria de fluxo, compararam MJ18 com outro anticorpo, EPNCIR122, conhecido por detectar B7-H3. Em várias linhagens de células tumorais murinas, EPNCIR122 produziu um sinal claro que desapareceu quando o gene B7-H3 foi deletado, confirmando sua especificidade. MJ18, em contraste, não mostrou ligação convincente mesmo em alta concentração. Ao examinar células imunes do baço, MJ18 ligou-se, mas o padrão não correspondia ao do B7-H3, e EPNCIR122 não detectou B7-H3 nessas células, sugerindo que MJ18 estava se ligando a outra coisa.
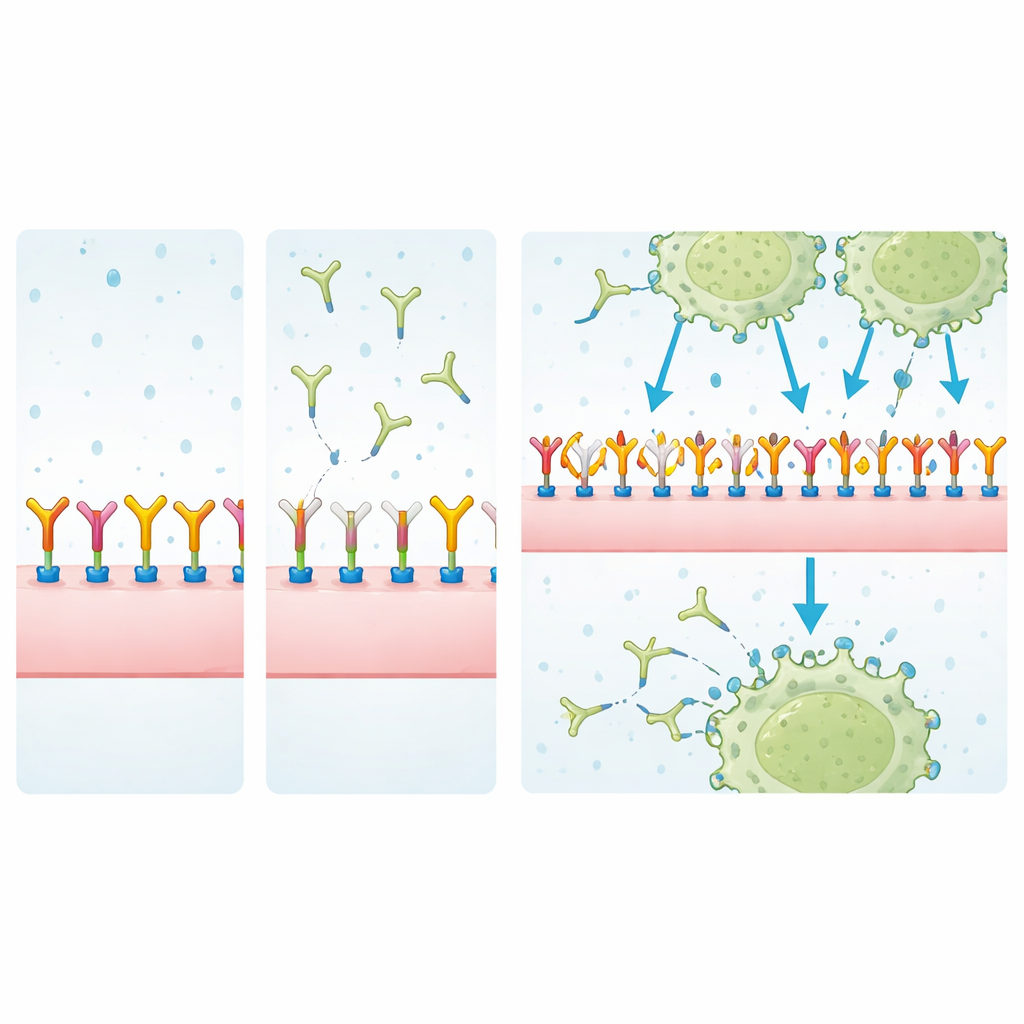
Investigando os parceiros de ligação
Para identificar o que o MJ18 poderia realmente reconhecer, os pesquisadores precipitaram proteínas da superfície celular usando MJ18 ou EPNCIR122 e as analisaram por espectrometria de massa, filtrando contaminantes comuns de fundo. Em células tumorais, EPNCIR122 enriqueceu fortemente B7-H3 em relação a outras proteínas, confirmando que é um reagente altamente específico. MJ18, porém, puxou uma mistura de proteínas na qual B7-H3 apareceu apenas fracamente e em níveis semelhantes aos de ligantes inespecíficos. Medições por ressonância plasmónica de superfície, uma técnica sensível para quantificar interações moleculares, reforçaram a conclusão: a afinidade do MJ18 pelo B7-H3 murino foi aproximadamente 7.000 vezes mais fraca que a de EPNCIR122 — muito abaixo do que é típico para anticorpos terapêuticos.
Quando anticorpos são agarrados pelas células erradas
A história não terminou com a ligação fraca. Em células do baço, testes adicionais mostraram que MJ18 e anticorpos de rato semelhantes eram reconhecidos por receptores Fc de camundongo — moléculas em células imunes que normalmente se ligam à cauda dos anticorpos. Bloquear esses receptores reduziu drasticamente o sinal de MJ18, implicando que grande parte de sua aparente ligação vinha das células imunes agarrando o próprio anticorpo, em vez de MJ18 direcionar uma proteína de superfície específica. Tentativas de identificar um parceiro proteico único para MJ18 em células imunes encontraram apenas candidatos em níveis indistinguíveis do ruído de fundo. No conjunto, os dados sugerem que MJ18 se comporta amplamente como um anticorpo de baixa afinidade e não específico, cujas interações são dominadas pelo engajamento de receptores Fc em vez do reconhecimento preciso do B7-H3.
O que isso significa para o futuro
Para não especialistas, a mensagem é direta: embora B7-H3 continue sendo um alvo atraente em muitos cânceres, o anticorpo MJ18 não é um dardo confiável. Ele se liga ao B7-H3 em camundongos apenas de forma fraca e não reproduz o controle tumoral robusto observado quando o gene B7-H3 é removido. Estudos anteriores em camundongos que relataram benefícios dramáticos com MJ18 podem, portanto, refletir outros efeitos — como o modo como a região Fc do anticorpo interage com receptores de células imunes — em vez de um bloqueio real de B7-H3. Os autores defendem que o campo precisa urgentemente de anticorpos bem validados e de alta afinidade contra o B7-H3 murino, e que os pesquisadores devem confirmar rotineiramente a especificidade e a força dessas ferramentas. Só com reagentes confiáveis as informações obtidas em modelos animais poderão guiar com segurança o desenvolvimento de terapias de próxima geração direcionadas a B7-H3 para pacientes.
Citação: Gulyás, D., Nammor, T., Frizzell, J. et al. Low-affinity binding of anti-B7-H3 clone MJ18 to murine B7-H3 fails to induce tumor regression. Sci Rep 16, 9519 (2026). https://doi.org/10.1038/s41598-026-40628-x
Palavras-chave: B7-H3, imunoterapia do câncer, validação de anticorpos, pontos de verificação imune, modelos tumorais