Clear Sky Science · pt
Grandes variações na expressão total e alelo‑específica de transcritos de maneira independente da mutação causal da doença
Por que isso importa para pessoas com fibrose cística
A fibrose cística (FC) costuma ser descrita como uma doença “de gene único” nos livros, ainda que pessoas com exatamente a mesma mutação possam apresentar sintomas e trajetórias de vida muito diferentes. Este estudo faz uma pergunta aparentemente simples, com consequências amplas: mesmo quando o gene defeituoso é o mesmo, os pacientes produzem quantidades diferentes da mensagem gênica, e isso poderia ajudar a explicar por que a doença se manifesta de modos tão distintos — e como eles respondem aos medicamentos modernos?
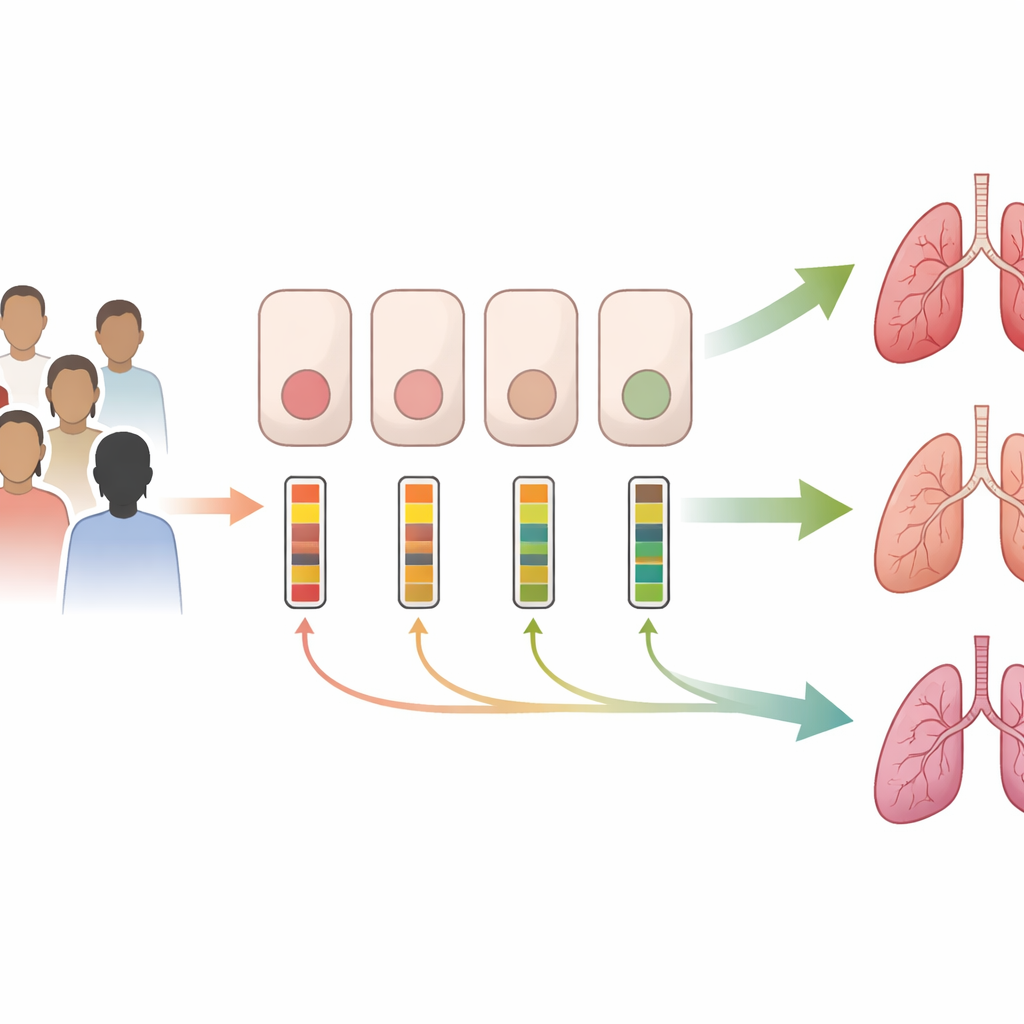
Pacientes diferentes, mesma mutação, atividade gênica muito diferente
Os pesquisadores focaram no gene CFTR, cujas versões defeituosas causam FC. Em vez de olharem só para mudanças no DNA, mediram quanto RNA mensageiro (mRNA) do CFTR — o “roteiro” do gene para produzir proteína — estava presente em células das vias aéreas coletadas por raspagens nasais suaves. Ao longo de cinco anos reuniram amostras de crianças e adultos com FC, além de um pequeno grupo sem FC. Muitos pacientes carregavam a mutação comum F508del, seja em ambas as cópias do gene ou em uma cópia combinada com outra variante. Mesmo dentro desses grupos, os níveis de mRNA do CFTR variaram amplamente — diferindo vários vezes de uma pessoa para outra. Voluntários saudáveis também mostraram grande variação, sugerindo que a expressão do CFTR difere naturalmente entre indivíduos, e que essa variabilidade intrínseca se reflete na FC.
Quando as duas cópias do gene não contribuem igualmente
Para pacientes que carregavam duas mutações diferentes no CFTR — uma F508del e outra variante — a equipe foi além. Usando testes moleculares altamente específicos, contaram quanto mRNA vinha de cada cópia do gene separadamente. Em vez de cada alelo contribuir com cerca de metade do total, frequentemente encontraram um forte desequilíbrio, ou “viés”: o alelo não‑F508del tipicamente produzia muito mais mRNA do que o alelo F508del. Em alguns pacientes, a cópia F508del contribuía com apenas uma fração pequena da mensagem total do CFTR. Essa produção desigual apareceu mesmo entre pessoas que compartilhavam o mesmo par de mutações, sugerindo que mudanças adicionais no DNA próximas ao gene, ou mecanismos regulatórios mais amplos, influenciam quanto mensagem cada cópia produz.
Estudos em células confirmam a variabilidade intrínseca
Para remover algumas das complicações do mundo real, como infecções e inflamação nas vias aéreas, os cientistas também cultivaram células nasais e brônquicas de pacientes em laboratório. Ali também detectaram grandes diferenças nos níveis totais de mRNA do CFTR entre pessoas com o mesmo perfil genético. Em um subconjunto de células cultivadas de pacientes heterozigotos compostos, a expressão dos dois alelos estava mais próxima do equilíbrio do que nas amostras nasais frescas, ressaltando como as condições do cultivo celular e o ambiente do corpo podem alterar a atividade gênica. Em conjunto, essas observações apoiam a ideia de que tanto a produção total de CFTR quanto a contribuição relativa de cada alelo são características flexíveis, não fixadas apenas pela sequência de DNA das mutações principais.
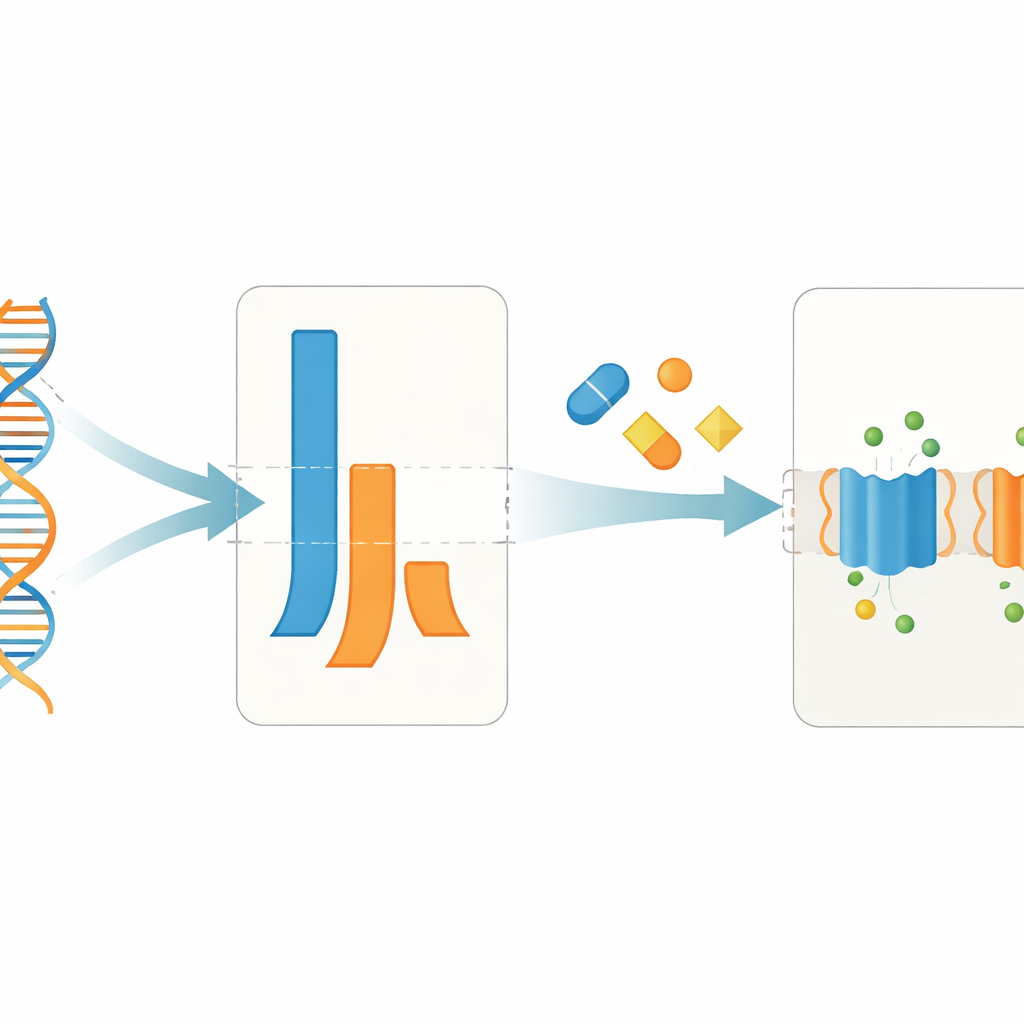
Medicamentos modernos para FC alteram o equilíbrio entre as cópias do gene
O estudo também examinou um pequeno grupo de pacientes antes e depois de iniciar terapias moduladoras de CFTR amplamente usadas, incluindo a combinação tripla elexacaftor–tezacaftor–ivacaftor e um regime com dois fármacos. Surpreendentemente, esses medicamentos não aumentaram nem diminuíram de forma consistente a quantidade total de mRNA do CFTR em células nasais. Em vez disso, deslocaram qual alelo contribuía mais. Após o tratamento, o alelo F508del frequentemente passou a produzir uma parcela maior da mensagem total do CFTR, em alguns casos tornando‑se a fonte dominante. Essa mudança no balanço alélico ocorreu acompanhada das melhorias clínicas esperadas, como melhor função pulmonar e níveis de sal no suor mais baixos, sugerindo que aumentar a produção de mensagem de uma proteína mutante parcialmente resgatada pode complementar os efeitos conhecidos desses fármacos sobre o dobramento e a função proteica.
O que isso significa para o tratamento personalizado
Para pessoas que vivem com fibrose cística, esses achados ressaltam que mutações no DNA são apenas parte da história. Quanto mRNA do CFTR uma pessoa produz — e como essa produção é dividida entre suas duas cópias do gene — pode variar amplamente e de formas não previstas apenas pelo tipo de mutação. Essa variação pode ajudar a explicar por que pacientes com o mesmo genótipo apresentam gravidade da doença e respostas ao tratamento diferentes. Também sugere que abordagens personalizadas futuras podem precisar medir não apenas quais mutações do CFTR um indivíduo carrega, mas quão ativamente cada cópia do gene está sendo utilizada, tanto antes quanto durante o tratamento. Entender e, eventualmente, controlar essa camada oculta de atividade gênica pode ajudar a afinar terapias para FC e outras doenças de gene único.
Citação: Freyberg, M., Bewig, M., Bampi, G.B. et al. Large variations in total and allele-specific transcript expression in a disease mutation-independent manner. Sci Rep 16, 7831 (2026). https://doi.org/10.1038/s41598-026-40624-1
Palavras-chave: fibrose cística, CFTR, expressão gênica, desequilíbrio alélico, moduladores de CFTR