Clear Sky Science · pt
Análise teórica da supressão optogenética de potenciais de ação em cardiomiócitos ventriculares humanos expressando canalorodopsinas seletivas para potássio com baixo consumo de energia
Uma maneira mais suave, à base de luz, de acalmar um coração acelerado
Ritmos cardíacos rápidos e caóticos podem causar desmaios, AVC ou morte súbita. Os tratamentos atuais — drogas potentes, desfibriladores implantados ou choques de alta energia — podem salvar vidas, mas também são dolorosos e imprecisos. Este estudo explora uma ideia bem diferente: usar flashes tênues de luz e proteínas especialmente projetadas para empurrar discretamente as células cardíacas de volta a um ritmo seguro e regular, usando muito menos energia do que as abordagens atuais.
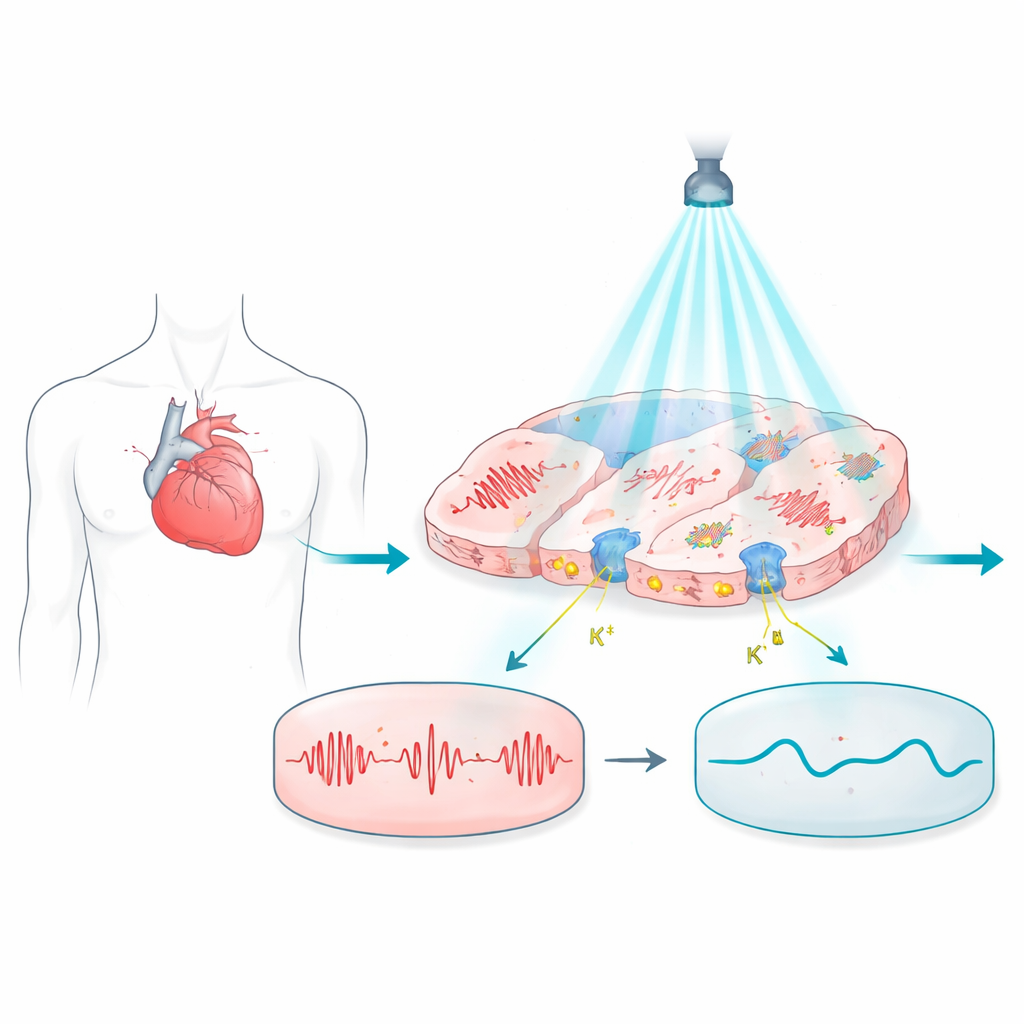
Iluminando batimentos problemáticos
O trabalho baseia-se na optogenética, uma técnica em que células são equipadas com proteínas sensíveis à luz para que sua atividade elétrica possa ser controlada por flashes luminosos. No coração, essas proteínas podem em princípio substituir eletrodos de metal, oferecendo controle sem contato e indolor. Mas a maioria das proteínas sensíveis à luz usadas até agora tende a elevar a voltagem da célula, em direção a um estado excitado, o que dificulta manter as células silenciosas em repouso ou ajustar finamente a duração de cada batida. Isso limita sua utilidade para desligar com segurança ritmos perigosos ou corrigir distúrbios elétricos que dependem de temporizações sutis.
Novos interruptores de luz ajustados ao “ajuste de repouso” do coração
Proteínas recentemente descobertas, chamadas canalorodopsinas seletivas para potássio, incluindo WiChR e HcKCR1, prometem corrigir esse desalinhamento. Ao contrário de proteínas mais antigas que deixam passar uma mistura de íons, esses canais preferem fortemente o potássio e naturalmente puxam a voltagem da célula para o mesmo nível negativo que ela adotaria em repouso. Os autores construíram modelos computacionais detalhados de células ventriculares humanas que expressam esses canais mais novos e os compararam com duas opsinas mais conhecidas e mais excitatórias, ChR2(H134R) e ChRmine. Ao simular como essas células respondem a diferentes cores e intensidades de luz, puderam explorar com segurança condições que seriam difíceis ou demoradas de testar em corações reais.
Luz suave, controle forte
As simulações mostram que canais seletivos para potássio fornecem controle muito mais econômico e estável. A WiChR, em particular, poderia interromper completamente potenciais de ação — os breves picos elétricos que disparam cada batida — usando intensidades de luz centenas a milhares de vezes menores do que as necessárias para muitas ferramentas anteriores. Com luz contínua, WiChR e HcKCR1 mantiveram a voltagem da célula próxima ao seu nível normal de repouso, efetivamente segurando a célula em um estado calmo e seguro. Em contraste, ChR2 e ChRmine tendiam a empurrar a voltagem para valores mais positivos, às vezes bloqueando a atividade, mas apenas após forçar a célula a um estado estressado e superexcitável. A WiChR também funcionou bem com pulsos breves de luz, impedindo de forma confiável os picos das células cardíacas batida após batida, o que sugere que poderia acompanhar ritmos cardíacos rápidos sem superaquecer o tecido ou desperdiçar energia.
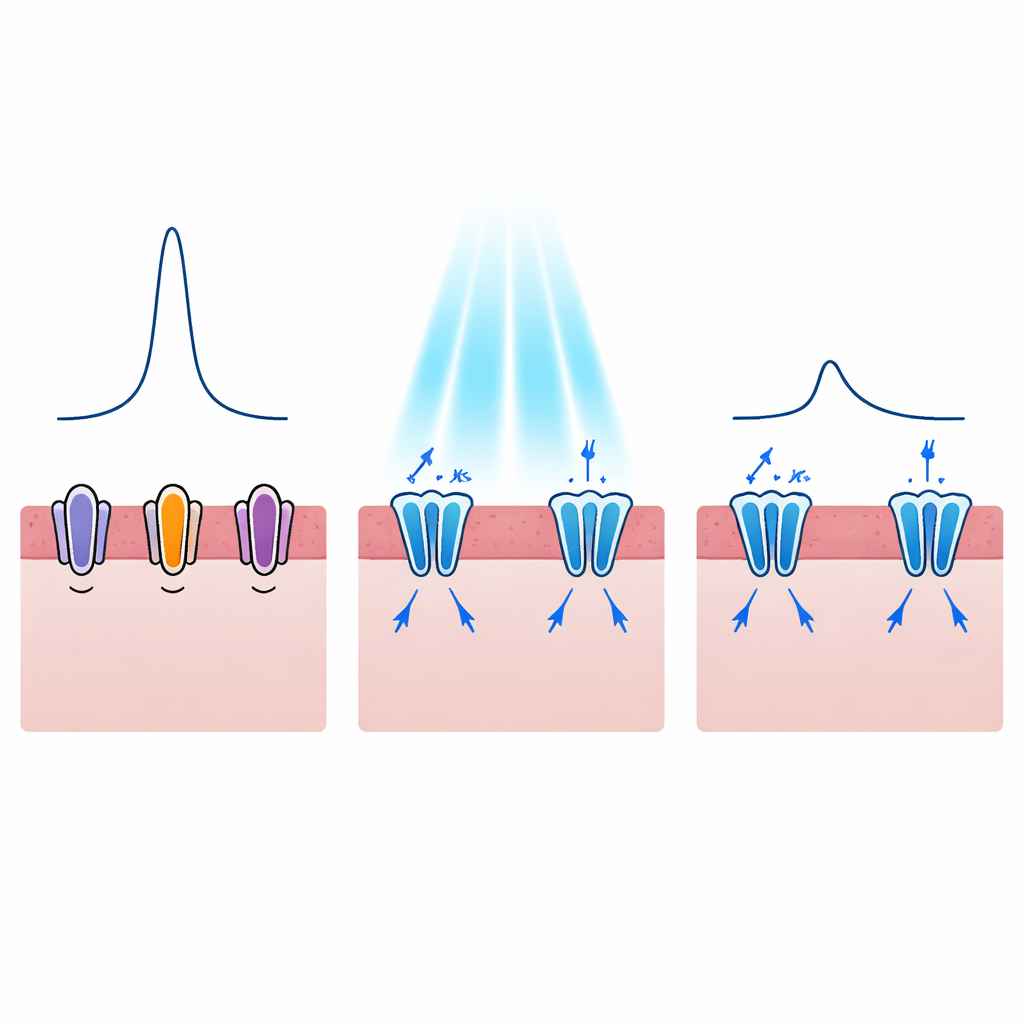
Reconfigurando cada batida, não apenas parando-a
Arritmias perigosas estão frequentemente ligadas não só ao fato de uma célula cardíaca disparar, mas também a quanto tempo ela permanece excitada. Em distúrbios como a síndrome do QT longo, o pulso elétrico de cada batida é prolongado, aumentando a chance de evoluir para ritmos fatais. Os autores, portanto, perguntaram se canais de potássio ativados por luz poderiam encurtar esse pulso de maneira controlada. Seus modelos mostraram que ativar WiChR ou HcKCR1 durante a fase de platô do potencial de ação gerou correntes de potássio fortes e de saída que puxaram a voltagem de volta mais cedo. À medida que os níveis de luz aumentavam, a duração do pulso elétrico caiu de cerca de 300 milissegundos para aproximadamente metade desse valor, e esse efeito podia ser alcançado mesmo com flashes de luz muito curtos. A WiChR tendia a produzir períodos de silêncio mais duradouros, enquanto HcKCR1 oferecia recuperação mais rápida assim que a luz era desligada, sugerindo diferentes usos clínicos potenciais.
De modelos computacionais a terapias futuras
No conjunto, o estudo conclui que canais sensíveis à luz seletivos para potássio, especialmente a WiChR, são ferramentas promissoras para um controle cardíaco suave e de baixo consumo. Eles podem tanto silenciar a atividade elétrica descontrolada quanto reduzir batimentos excessivamente longos, tudo mantendo a voltagem da célula próxima ao seu estado natural de repouso. Embora os resultados provenham de simulações detalhadas em célula única em vez de experimentos em coração inteiro, eles fornecem orientação quantitativa sobre quanta luz pode ser necessária, quando ela deveria ser aplicada e quais variantes proteicas são mais adequadas para diferentes objetivos. A longo prazo, essa linha de trabalho aponta para um futuro em que cardiologistas possam usar feixes de luz finamente ajustados, em vez de choques dolorosos, para prevenir ou interromper arritmias potencialmente fatais.
Citação: Dixit, N., Pyari, G. & Roy, S. Theoretical analysis of low-power optogenetic suppression of action potentials in human ventricular cardiomyocytes expressed with potassium-selective channelrhodopsins. Sci Rep 16, 9765 (2026). https://doi.org/10.1038/s41598-026-40578-4
Palavras-chave: optogenética cardíaca, supressão de arritmia, canalorodopsinas de potássio, duração do potencial de ação, síndrome do QT longo