Clear Sky Science · pt
Sexagem in ovo e genotipagem usando técnicas de PCR: uma contribuição aos princípios 3R na criação de galinhas
Por que o que acontece dentro do ovo importa
Todo ano, milhões de pintinhos machos são eliminados pouco depois da eclosão porque não são úteis para a produção de ovos. Ao mesmo tempo, laboratórios de pesquisa no mundo inteiro incubam mais animais do que realmente precisam, simplesmente porque não conseguem identificar o sexo ou o perfil genético de um embrião cedo o suficiente. Este estudo apresenta um modo prático de “ler” o sexo e os genes de um pintinho enquanto ele ainda se desenvolve dentro do ovo, usando testes de DNA padrão. Ao fazer isso de forma precoce e suave, o método busca evitar a eclosão de animais excedentes e reduzir o sofrimento, sem exigir equipamento industrial caro.
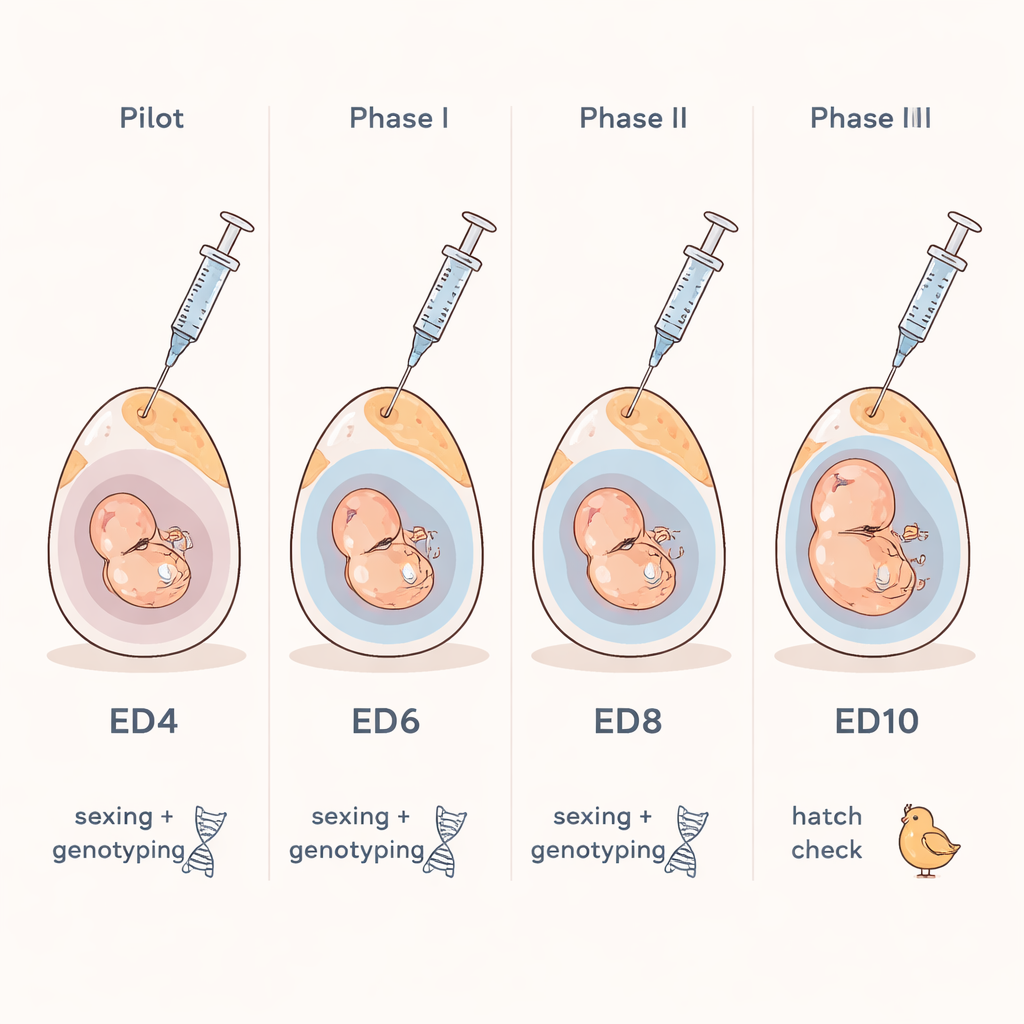
Olhando dentro do ovo sem abri‑lo
Os pesquisadores concentraram‑se em uma pergunta simples: podemos, de forma segura, retirar uma pequena amostra de fluido de um ovo de galinha fertilizado e usá‑la para identificar o sexo do embrião e traços genéticos importantes? Eles se apoiaram em um conceito familiar da medicina humana, em que médicos analisam fluidos ao redor do feto para detectar condições genéticas. Nas galinhas, uma fina bolsa preenchida por fluido chamada alantoide se forma ao redor do embrião conforme ele cresce. Ao sétimo dia de incubação, essa bolsa contém fluido suficiente para que uma agulha fina o alcance sem tocar o embrião. A equipe utilizou uma luz forte para localizar a câmara de ar na extremidade romba do ovo, fez um furo do tamanho de um alfinete na casca e retirou apenas algumas gotas de fluido com uma seringa minúscula.
De algumas gotas a uma impressão genética
O fluido coletado de ovos no início do desenvolvimento contém apenas quantidades minúsculas de DNA. Para contornar isso, os cientistas primeiro amplificaram todo o material genético em cada amostra, criando muitas cópias sem alterar seu conteúdo. Em seguida aplicaram dois testes laboratoriais de rotina: a reação em cadeia da polimerase (PCR) padrão e uma variante chamada KASP (Kompetitive Allele Specific PCR). Ambos os testes podem distinguir entre os cromossomos sexuais de pintos machos e fêmeas e também detectar marcadores genéticos específicos, como a mutação que causa casca azul ou a presença de um gene inserido em linhas de pesquisa. Em mais de 800 ovos de várias raças — incluindo poedeiras comerciais, cruzamentos Araucana coloridos e uma linha de pesquisa geneticamente modificada — esses métodos produziram identificações corretas em cerca de 92–100% dos casos.
Encontrando o momento mais seguro para a amostragem
A amostragem muito precoce corre o risco de danificar estruturas frágeis vitais para o embrião, enquanto amostrar tardiamente deixa pouco tempo para agir a partir dos resultados. Para definir a janela ideal, a equipe primeiro cultivou embriões sem a casca para observar como as membranas e os espaços de fluido se expandem ao longo do tempo. Depois conduziram uma série de testes em ovos intactos em estágios definidos. Foi possível coletar fluido a partir do quarto dia, mas as taxas de sucesso para testes de DNA eram menores nesses dias iniciais, e o procedimento era tecnicamente mais difícil. Ao comparar as taxas de eclosão entre ovos perfurados e ovos‑controle intactos, verificaram que o sétimo dia oferecia o melhor equilíbrio: havia alantoide clara em quantidade suficiente, os testes de DNA funcionavam de forma confiável e a maioria dos embriões sobrevivia até a eclosão. Nesse ponto ainda há vários dias antes do provável início da percepção de dor no embrião, oferecendo uma margem ética para decisões.
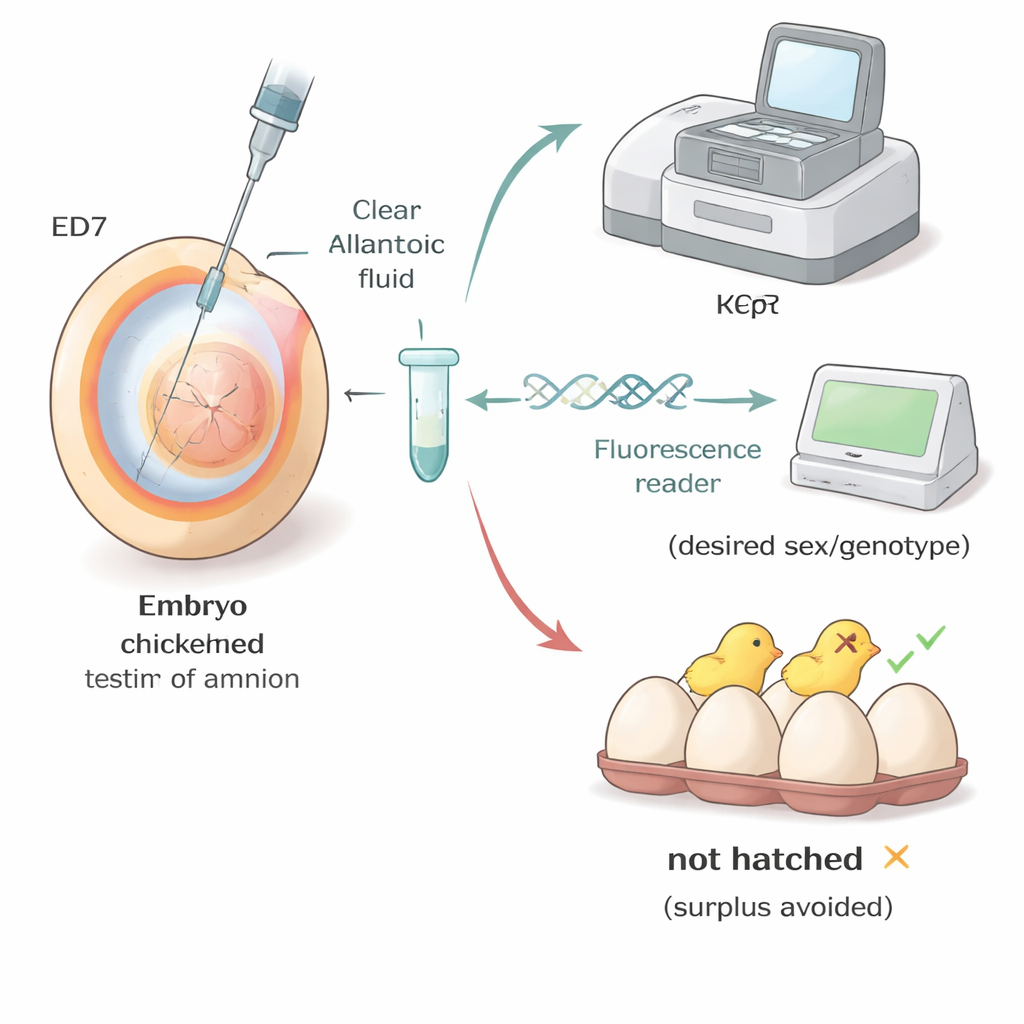
Aplicando o método em bandos reais
Os pesquisadores testaram seu fluxo de trabalho em condições semelhantes às de granjas de reprodução e laboratórios universitários. Em linhas comerciais de poedeiras marrons e brancas, ovos amostrados entre os dias quatro e sete mostraram que a eclodibilidade geralmente melhorava quando a amostragem era feita mais tarde, com os melhores resultados novamente no sétimo dia. Em uma linha especializada “hospedeira substituta” usada para genética avançada, a equipe foi além: sexou e genotipou embriões no sétimo dia e, em seguida, escolheu apenas aqueles com a combinação de sexo e genética desejada para continuar até a eclosão. Quase todos os embriões selecionados eclodiram em pintos saudáveis que cresceram conforme esperado, mostrando que a seleção precoce pode reduzir drasticamente o número de animais indesejados sem comprometer a qualidade dos pintos.
O que isso significa para o bem‑estar animal e a pesquisa
Para um não‑especialista, a mensagem central é direta: com um furo do tamanho de um alfinete e ferramentas de laboratório de rotina, agora é possível saber, enquanto o pintinho ainda está seguramente dentro do ovo, se ele é macho ou fêmea e se carrega determinados traços genéticos. O estudo mostra que fazer isso por volta do sétimo dia de incubação é tecnicamente confiável e suave o bastante para que a maioria dos embriões sobreviva. Ao permitir que embriões indesejados sejam removidos antes de provavelmente serem capazes de sentir dor, a abordagem apoia os amplamente aceitos princípios 3R: substituir, reduzir e refinar o uso de animais na ciência. Para incubatórios e laboratórios de pesquisa, essa técnica oferece um caminho realista para menos animais excedentes, melhor aproveitamento de recursos e padrões de bem‑estar mais elevados — sem necessidade de máquinas industriais complexas.
Citação: Dierks, C., Förster, A., Meunier, D. et al. In ovo sexing and genotyping using PCR techniques: a contribution to the 3R principles in chicken breeding. Sci Rep 16, 7464 (2026). https://doi.org/10.1038/s41598-026-40562-y
Palavras-chave: embrião de galinha, sexagem in ovo, genotipagem por PCR, bem‑estar animal, princípios 3R