Clear Sky Science · pt
Descoberta da hidroxitrazol como potencial inibidor da glicoxalase‑I utilizando técnicas de desenho de fármacos assistido por computador
Por que atrapalhar um pequeno limpador celular pode combater o câncer
As células cancerosas frequentemente crescem tão rápido que se afogam em seus próprios resíduos. Um dos truques de sobrevivência é uma equipe de limpeza interna que desintoxica subprodutos nocivos da queima de açúcar. Este estudo explora como desligar um membro-chave dessa equipe, uma enzima chamada glicoxalase‑I, usando computadores para vasculhar dezenas de milhares de moléculas e experimentos para testar os melhores candidatos. O objetivo é descobrir novos “pontos de partida” para fármacos que possam, um dia, ajudar médicos a envenenar seletivamente as células cancerosas por dentro.
Um sistema oculto de remoção de resíduos dentro de nossas células
Cada célula quebra constantemente açúcar para produzir energia, e esse processo gera um químico reativo de resíduos chamado metilgloxal. Em quantidades normais, nosso corpo converte o metilgloxal em ácido lático inofensivo por meio do sistema glicoxalase, uma via em duas etapas que depende da molécula auxiliar glutationa. A glicoxalase‑I é a primeira e mais crucial etapa dessa cadeia. Células cancerosas, que consomem açúcar em ritmo frenético, dependem fortemente da glicoxalase‑I para evitar que o metilgloxal atinja níveis tóxicos. Se essa enzima for bloqueada, o metilgloxal se acumula e pode levar células danificadas à morte programada. Isso torna a glicoxalase‑I um alvo atraente para medicamentos anticâncer que atacam uma vulnerabilidade básica do metabolismo tumoral.
Buscando o espaço químico com silício e estatística
Em vez de testar substâncias aleatórias no laboratório, os pesquisadores utilizaram o desenho de fármacos assistido por computador para vasculhar uma grande coleção comercial de mais de 50.000 pequenas moléculas. Um software especializado primeiro limpou e padronizou cada molécula, depois previu sua forma 3D e comportamento em pH semelhante ao corporal. Uma triagem virtual rápida pontuou quão bem cada candidato poderia encaixar‑se no sítio ativo da glicoxalase‑I. A equipe então aplicou regras simples sobre tamanho, solubilidade e outras propriedades de “semelhança a fármaco” para descartar moléculas pouco prováveis de funcionar no organismo. Um programa de acoplamento mais detalhado examinou como as moléculas mais promissoras poderiam se orientar dentro da enzima, especialmente como poderiam alcançar e agarrar o átomo de zinco que fica no coração da química da glicoxalase‑I.
Uma nova maneira de agarrar o núcleo metálico da enzima
Esforços anteriores para bloquear a glicoxalase‑I focaram em grupos químicos bem conhecidos, como ácidos carboxílicos e ácidos hidroxâmicos, que são bons em se ligar a metais, mas frequentemente sofrem de baixa estabilidade ou efeitos colaterais indesejados. O presente estudo, em vez disso, revelou um tipo diferente de unidade “agarra‑metal”: um anel de hidroxitrazol. Entre dezesseis moléculas melhor ranqueadas escolhidas para compra e testes em laboratório, uma contendo esse anel — codificada SPB07393SC — destacou‑se. No acoplamento virtual, seu grupo hidroxitrazol alcançou o átomo de zinco, enquanto seus dois anéis aromáticos se encaixaram em bolsões oleosos próximos da enzima. Simulações computacionais do complexo ao longo de dezenas de nanosegundos sugeriram que a molécula permaneceu firmemente ligada, com distâncias estáveis, forma compacta da proteína e uma rede persistente de ligações de hidrogênio.
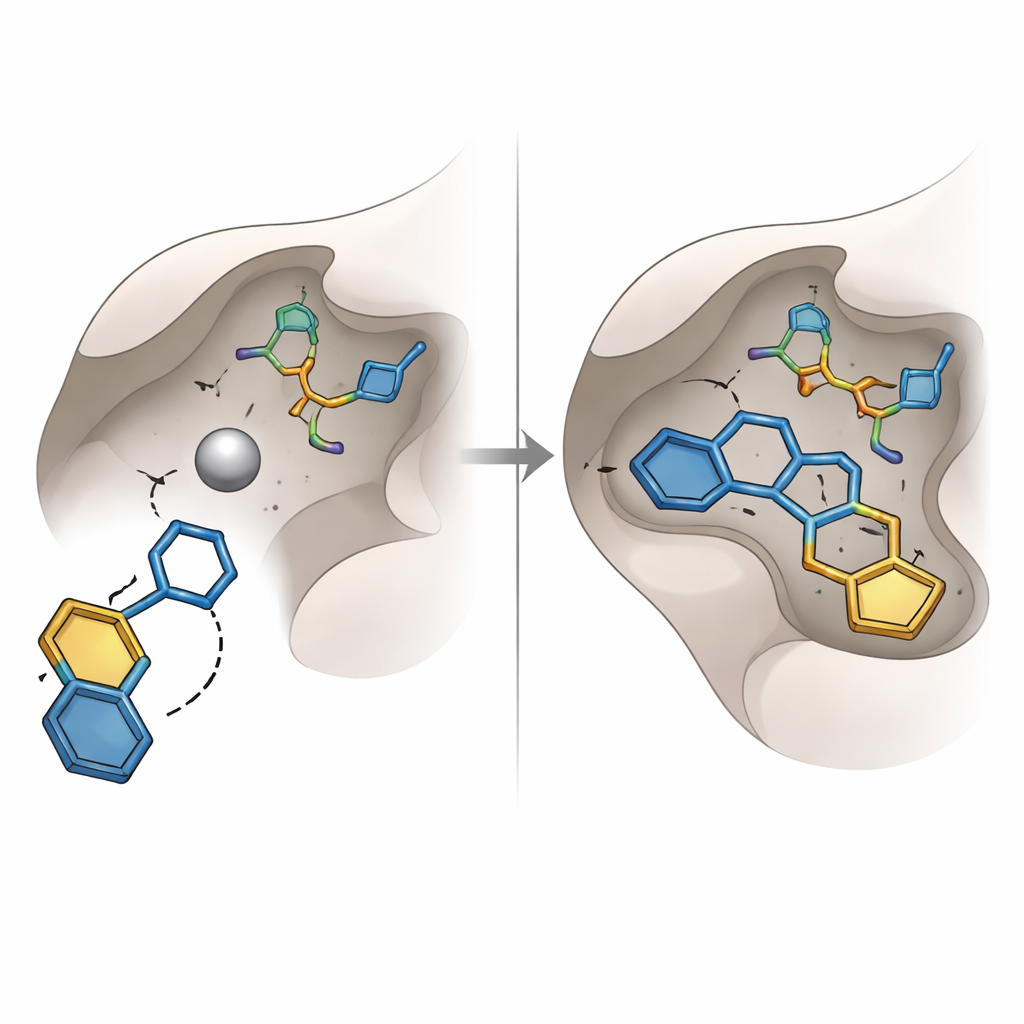
Colocando as previsões à prova
Para verificar se os modelos computacionais se traduziriam em efeitos no mundo real, a equipe mediu o quanto as moléculas selecionadas retardaram a atividade da glicoxalase‑I humana purificada em um ensaio em placa. Quinze das dezesseis candidatas mostraram apenas inibição fraca ou negligenciável nas condições testadas, destacando as armadilhas de confiar apenas em pontuações de acoplamento estático. Em contraste, a SPB07393SC inibiu fortemente a enzima, com uma potência na faixa de micromolar médio que a torna um “hit” inicial sólido, e não um fármaco acabado. Ferramentas de software adicionais previram que essa molécula deve ter solubilidade aceitável, boa absorção, capacidade de atingir o cérebro se necessário, e baixa probabilidade de causar certas toxicidades genéticas ou relacionadas ao fígado, embora essas previsões de segurança ainda exijam confirmação experimental.
O que isso significa para futuros medicamentos contra o câncer
O trabalho introduz o hidroxitrazol como uma forma nova de ancorar candidatos a fármacos ao átomo de zinco no centro da glicoxalase‑I, expandindo o cardápio de truques químicos disponíveis aos projetistas de fármacos. Embora a SPB07393SC em si seja apenas um ponto de partida, sua combinação de poder de bloqueio enzimático, comportamento previsto semelhante a fármaco e ligação estável em simulações dinâmicas a marca como um arcabouço promissor para refinamentos futuros. Mais amplamente, o estudo demonstra tanto as forças quanto os limites da triagem guiada por computador: ela pode reduzir rapidamente vastas bibliotecas químicas a alguns concorrentes realistas, mas experimentos laboratoriais cuidadosos ainda são essenciais para revelar quais moléculas realmente desativam a enzima da qual as células cancerosas dependem para gerenciar seus resíduos tóxicos.
Citação: Al-Qazzan, M., Al-Balas, Q., Alnajjar, B. et al. Discovery of hydroxytriazole as a potential glyoxalase-I inhibitor utilizing computer-aided drug design techniques. Sci Rep 16, 9945 (2026). https://doi.org/10.1038/s41598-026-40497-4
Palavras-chave: glicoxalase I, metabolismo do câncer, desenho de fármacos assistido por computador, inibidores ligantes de zinco, acoplamento molecular