Clear Sky Science · pt
Comportamento dependente da temperatura de líquidos ligados por ligações de hidrogênio: conectando experimentos com dinâmica molecular e DFT
Por que líquidos quentes e frios se comportam tão diferente
Qualquer pessoa que já tentou despejar xarope frio ou misturar óleos resfriados sabe que a temperatura pode mudar dramaticamente como líquidos fluem e se misturam. Este estudo investiga por que isso acontece em uma família específica de líquidos de importância industrial: misturas de um aldeído chamado heptanal com vários álcoois estreitamente relacionados. Ao observar essas misturas tanto no laboratório quanto em nível molecular, os autores mostram como um aquecimento suave rearranja silenciosamente a rede invisível de atrações entre moléculas, com grandes consequências para densidade, viscosidade e facilidade de escoamento. 
Soluventes do cotidiano com um aperto de mão escondido
Os líquidos examinados aqui estão longe de ser exóticos. Aldeídos e álcoois são comuns em combustíveis, fragrâncias, cosméticos e formulações farmacêuticas. Quando misturados, suas moléculas “se apertam a mão” por meio de atrações direcionais entre o grupo OH do álcool e o grupo carbonila do aldeído, formando o que os químicos chamam de ligações de hidrogênio. Essas ligações aproximam as moléculas mais do que uma mistura simples preveria, fazendo com que a mistura fique ligeiramente mais compacta e mais espessa do que uma mistura ideal sem interação. Os pesquisadores se concentraram no heptanal combinado com álcoois de cadeia linear de 1‑propanol a 1‑heptanol, perguntando-se duas questões-chave: como a temperatura altera esses apertos de mão moleculares e como o comprimento da “cauda” do álcool influencia o resultado?
Medindo como líquidos se compactam e fluem
No laboratório, a equipe mediu cuidadosamente a densidade e a viscosidade de cada mistura em uma faixa de temperaturas próximas à ambiente e superiores. Eles descobriram que todas as misturas exibem volume “extra” negativo ao serem combinadas, o que significa que o líquido misto ocupa menos espaço do que os ingredientes separados. Ao mesmo tempo, as misturas são mais viscosas do que uma regra prática simples sugeriria. Ambos os efeitos são mais fortes em baixa temperatura e para o álcool mais curto, 1‑propanol, e diminuem gradualmente à medida que os líquidos são aquecidos ou conforme as cadeias de álcool ficam mais longas. Esse padrão indica atrações fortes e eficientes entre heptanal e álcoois curtos que aproximam as moléculas e resistem ao fluxo, e interações mais fracas e mais obstruídas quando a cauda do álcool é mais volumosa.
Observando o movimento e o agrupamento molecular
Para ver a história microscópica por trás dessas medições, os autores recorreram a simulações de dinâmica molecular e cálculos quânticos. Modelos computacionais de milhares de moléculas revelaram com que frequência e quão de perto heptanal e moléculas de álcool se agrupam umas às outras. Em baixas temperaturas, as simulações mostram muitas ligações de hidrogênio curtas e bem definidas e uma estrutura densamente empacotada com apenas pequenas cavidades vazias entre as moléculas. À medida que a temperatura aumenta, essas ligações se tornam menos frequentes e um pouco mais longas, as moléculas se movem com mais liberdade e as cavidades vazias crescem e se conectam mais — evidência direta de aumento do espaço livre e de difusão mais rápida. Para álcoois curtos, o entorno ao redor do heptanal é relativamente uniforme, enquanto álcoois mais longos criam uma primeira camada mais irregular, pois suas caudas volumosas bloqueiam parcialmente o acesso aos sítios de ligação chave. 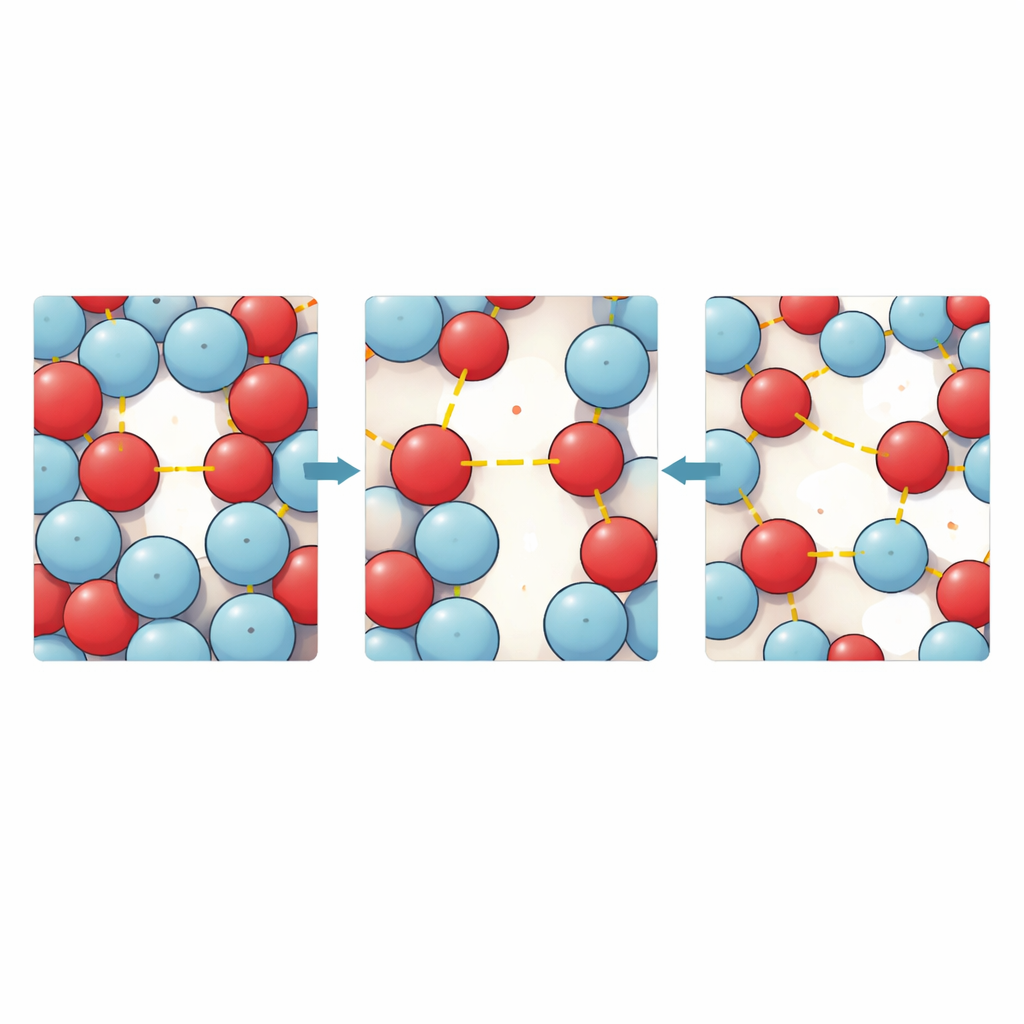
Balanceando energia, ordem e aglomeração molecular
Ao analisar como os arranjos moleculares mudam com a temperatura, a equipe conseguiu separar os papéis da estabilização energética e da desordem. Formar contatos próximos entre moléculas libera uma pequena quantidade de energia, tornando essas interações favoráveis, mas também restringe sua liberdade de mover-se e girar. Os cálculos mostram que, para essas misturas, o ganho energético da ligação de hidrogênio supera ligeiramente a perda de liberdade, de modo que os contatos locais são impulsionados principalmente pela energia atrativa com uma penalidade modesta em termos de desordem. Modelos quânticos de pares simples de moléculas confirmam que pares heptanal–álcool são, em geral, mais fortemente ligados do que pares álcool–álcool para cadeias mais curtas, reforçando a ligação mista e o empacotamento compacto. Para o álcool mais longo estudado, essa vantagem quase desaparece, e o álcool prefere ligar-se a si mesmo tanto quanto ao heptanal, enfraquecendo a contração e o espessamento especiais observados em misturas de cadeias mais curtas.
O que isso significa para líquidos do mundo real
Em termos simples, o artigo mostra que em baixas temperaturas o heptanal e álcoois de cadeia curta se entrelaçam por meio de muitas atrações direcionais, puxando‑se para uma fase intimamente compactada e relativamente lenta. Aquecer a mistura solta essas conexões, abrindo mais espaço vazio, permitindo que as moléculas deslizem umas pelas outras com mais facilidade e aproximando o comportamento daquele de líquidos comuns, menos interativos. À medida que as cadeias de álcool se alongam, suas caudas volumosas atrapalham esse entrelaçamento, de modo que a temperatura tem um efeito mais suave e as misturas se tornam, no geral, menos compactas e menos viscosas. Ao reunir medições, simulações e cálculos detalhados, o estudo oferece uma imagem clara e multinível de como a variação de temperatura e o tamanho molecular ajustam a rede oculta de ligações que governa como líquidos ligados por hidrogênio do cotidiano se compactam, fluem e respondem em processos industriais.
Citação: Almasi, M., Vatanparast, M. Temperature dependent behavior of hydrogen-bonded liquids: bridging experiments with molecular dynamics and DFT. Sci Rep 16, 9185 (2026). https://doi.org/10.1038/s41598-026-40428-3
Palavras-chave: líquidos ligados por ligação de hidrogênio, efeitos da temperatura, misturas aldeído–álcool, dinâmica molecular, viscosidade e densidade