Clear Sky Science · pt
MOV10, uma nova imunoterapia e biomarcador prognóstico, contribui para o desenvolvimento do glioma ao regular a autofagia
Por que este estudo sobre câncer cerebral importa
O glioblastoma, uma forma agressiva de câncer cerebral, é notoriamente difícil de tratar. A maioria dos pacientes sobrevive apenas alguns meses após o diagnóstico, mesmo com cirurgia, radioterapia e quimioterapia. Este estudo foca em uma única molécula chamada MOV10, que está incomumente ativa nesses tumores. Ao mostrar como o MOV10 ajuda as células cancerosas a crescer, evadir o sistema imunológico e resistir à morte, os pesquisadores identificam um novo alvo potencial para terapias mais eficazes — e um possível marcador para prever o prognóstico dos pacientes.
Um ajudante oculto dos tumores cerebrais mortais
A equipe começou vasculhando grandes bancos de dados públicos de câncer que contêm informações genéticas e clínicas de centenas de pessoas com glioma, um grupo amplo de tumores cerebrais que inclui o glioblastoma. Eles descobriram que MOV10, uma proteína envolvida no processamento de RNA dentro das células, está ativada em níveis mais altos nos tecidos de glioma do que no cérebro normal. Pacientes cujos tumores produziam mais MOV10 tendiam a viver menos tempo, e essa associação permaneceu mesmo após ajustar por idade, grau do tumor e características genéticas importantes. Usando esses fatores, os pesquisadores construíram um modelo matemático mostrando que os níveis de MOV10 podem ajudar a prever as chances de sobrevida de um paciente, sugerindo que MOV10 pode servir como biomarcador prognóstico.
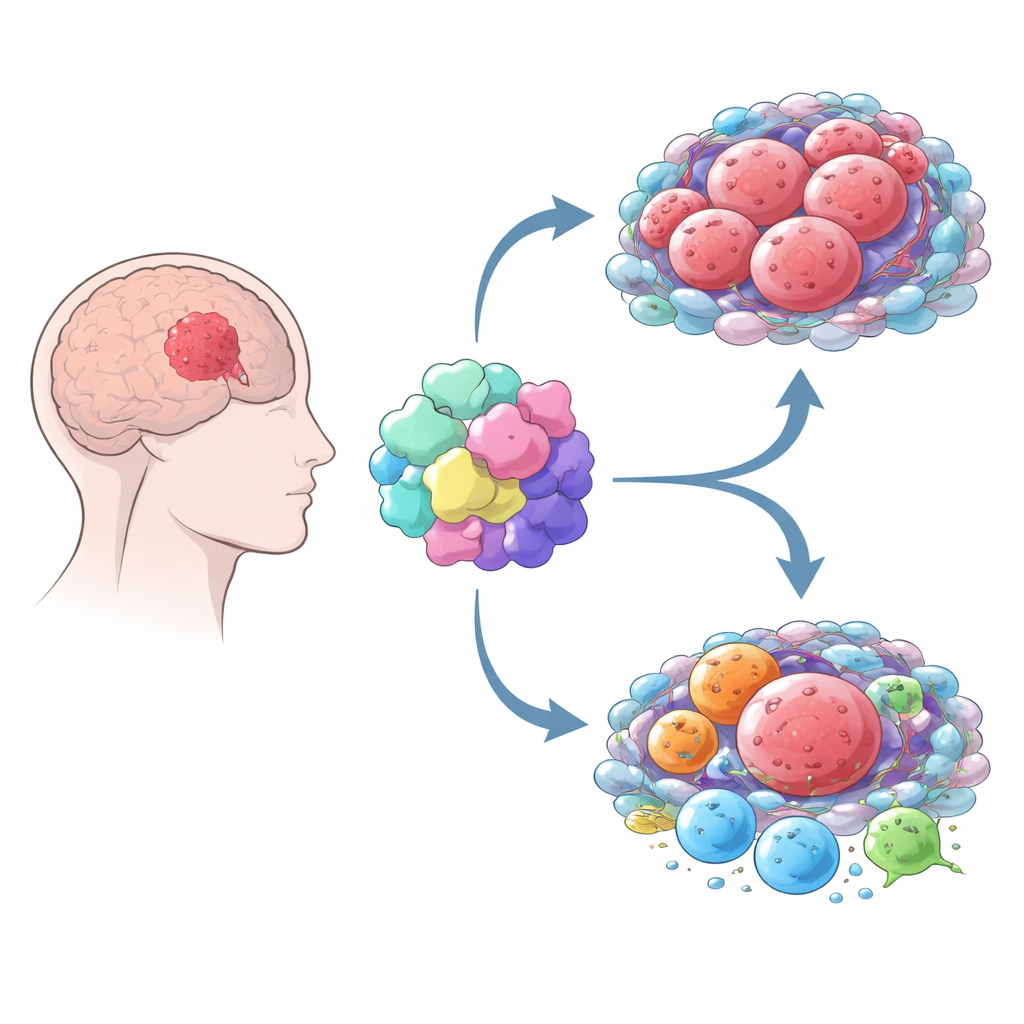
Como o MOV10 remodela o entorno tumoral
O câncer não cresce isoladamente — ele apropria-se do “vizinhança” ao redor composta por células imunes e de suporte. Ao combinar várias ferramentas computacionais, os autores mostraram que gliomas com alto MOV10 são rodeados por uma mistura mais rica de células imunes e estromais do que tumores com baixo MOV10. Mas isso não representa um ataque imunológico saudável. Em vez disso, tumores com alto MOV10 contêm mais macrófagos, especialmente um subtipo frequentemente chamado M2, que tipicamente apoia o crescimento tumoral e acalma as respostas imunes. Esses tumores também exibem assinaturas mais fortes de células T exauridas e maior atividade de “freios” imunológicos que são alvos de drogas imunoterápicas populares, como PD-1 e CTLA-4. No conjunto, o padrão sugere que o MOV10 está ligado a um ambiente imuno-supressor no qual as defesas do organismo ficam atenuadas.
Do big data às células no laboratório
Para ir além das correlações, os pesquisadores examinaram o MOV10 diretamente em amostras de pacientes e em células cultivadas. Eles confirmaram que o MOV10 é mais abundante em tecidos de glioma do que no cérebro normal, e que várias linhas celulares de glioma amplamente usadas também exibem níveis altos. Quando usaram pequenos RNAs interferentes para reduzir o MOV10 em células de glioma cultivadas em placas, as células se dividiram mais lentamente, formaram menos colônias e perderam parte da habilidade de se mover e invadir através de membranas artificiais. Proteínas que promovem a progressão do ciclo celular e a invasão diminuíram em abundância, sustentando a ideia de que o MOV10 promove ativamente o comportamento agressivo em vez de ser um observador passivo.
Ligando o MOV10 às células imunes e às vias de auto-limpeza
O estudo também investigou como o MOV10 interage com dois processos-chave: o comportamento dos macrófagos associados ao tumor e o sistema de “auto-limpeza” da célula conhecido como autofagia. Em amostras tumorais humanas, o MOV10 foi encontrado nas mesmas regiões que macrófagos do tipo M2. Em um sistema de co-cultura, quando células de glioma foram geneticamente alteradas para produzir menos MOV10, menos macrófagos tipo M2 migraram através de uma barreira em direção a elas, implicando que o MOV10 nas células tumorais ajuda a atrair ou sustentar essas células imunes pró-tumorais. Ao mesmo tempo, análises genéticas ligaram o MOV10 a vários genes envolvidos na autofagia. Usando marcadores fluorescentes que iluminam estruturas de reciclagem celular, a equipe mostrou que reduzir o MOV10 aumentou a atividade autofágica nas células de glioma e desencadeou mais morte celular programada. Alterações em proteínas marcadoras de autofagia e apoptose corroboraram essas observações.
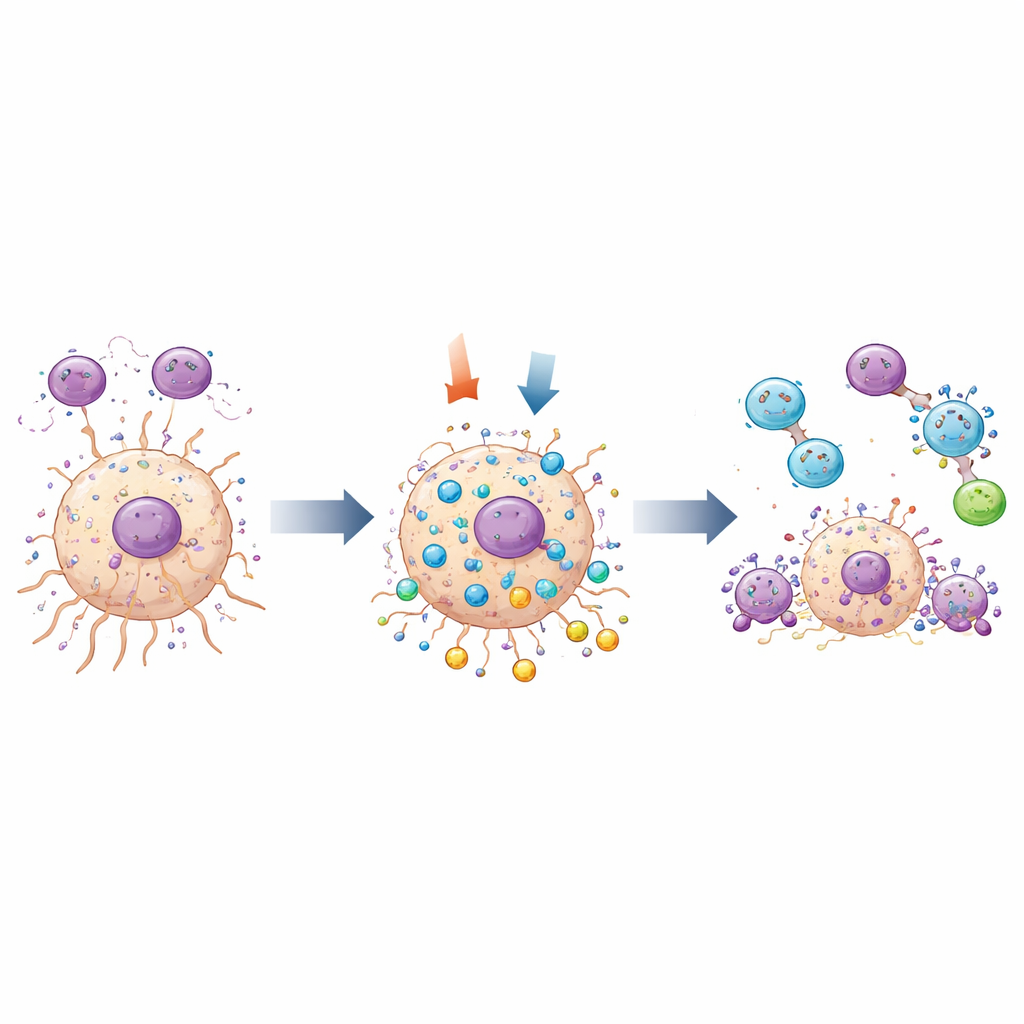
O que isso significa para tratamentos futuros
Em conjunto, os achados desenham o MOV10 como um aliado multifacetado do glioma: ele impulsiona o crescimento e a invasão das células tumorais, ajuda a construir um microambiente imuno-supressor rico em macrófagos que suportam o tumor, e mantém os sistemas de reciclagem e autodestruição celular sob controle. Quando o MOV10 é silenciado, as células de glioma crescem menos, morrem com mais facilidade e parecem menos capazes de recrutar tipos de células imunes prejudiciais. Para não especialistas, a mensagem-chave é que o MOV10 é tanto um “termômetro” quanto um “interruptor”: seu nível nos tumores pode ajudar a prever o prognóstico dos pacientes, e reduzi-lo poderia, em princípio, tornar os tumores cerebrais mais vulneráveis ao tratamento. Embora sejam necessários mais estudos em animais e, eventualmente, ensaios clínicos, o MOV10 agora se destaca como um alvo promissor na busca por terapias melhores contra um dos cânceres cerebrais mais letais.
Citação: Wang, F., Ruan, L., Yang, W. et al. MOV10, a novel immunotherapy and prognostic biomarker, contributes to glioma development by regulating autophagy. Sci Rep 16, 9501 (2026). https://doi.org/10.1038/s41598-026-40396-8
Palavras-chave: glioblastoma, imunoterapia de tumores cerebrais, proteína MOV10, microambiente tumoral, autofagia e apoptose