Clear Sky Science · pt
Splicing alternativo e expressão gênica diferencial durante mudanças na receptividade endometrial em pacientes com falha recorrente de implantação
Por que alguns embriões não se implantam
Muitos casais submetidos à fertilização in vitro enfrentam um mistério frustrante: mesmo quando embriões de alta qualidade são transferidos, a gravidez pode não ocorrer. Este estudo examina de perto o revestimento do útero — o endométrio — para entender por que algumas mulheres apresentam falhas repetidas de implantação. Ao investigar como genes são ativados e desativados, como suas mensagens são cortadas e reorganizadas, e como as células imunes se comportam durante a breve janela em que o útero está pronto para receber um embrião, a pesquisa revela novas pistas moleculares que, no futuro, podem orientar testes e tratamentos mais precisos.
A breve janela de acolhimento do útero
A implantação só pode ocorrer durante um curto período de cada ciclo, quando o revestimento uterino se torna "receptivo." Os pesquisadores compararam amostras de tecido de 90 mulheres férteis e 73 mulheres com falha recorrente de implantação, todas coletadas em três momentos-chave: pouco antes de o endométrio se tornar receptivo, durante a janela receptiva e logo após seu fechamento. Usando sequenciamento de RNA em alta vazão, mediram quais genes estavam ativos e como as mensagens de RNA eram processadas. Esse desenho permitiu acompanhar como um endométrio saudável se prepara para um embrião e como essa preparação falha em mulheres que repetidamente não conseguem implantar, apesar de embriões de boa qualidade. 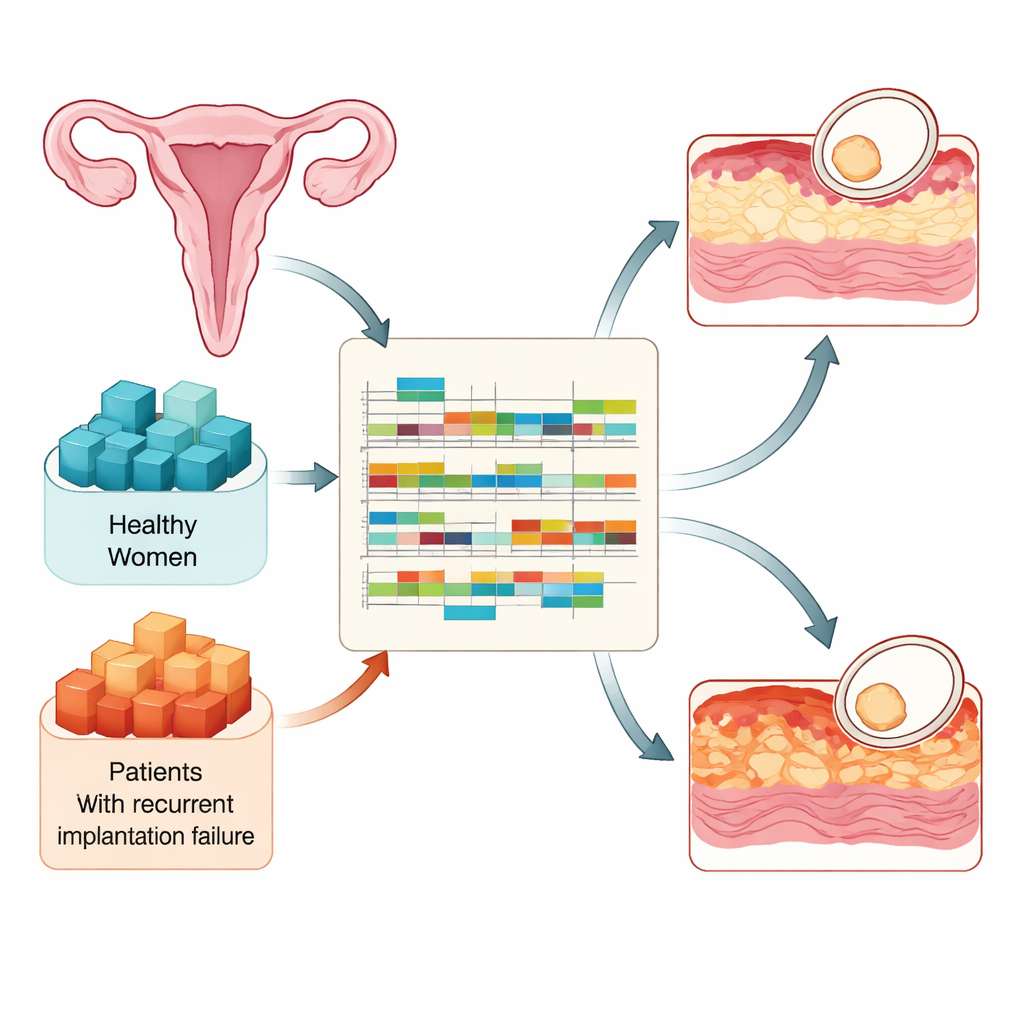
Mensagens gênicas cortadas e reorganizadas
Além de simplesmente contar a atividade de cada gene, a equipe focou no splicing alternativo — o processo pelo qual um único gene pode ser cortado em variantes de mensagem diferentes, levando a formas proteicas distintas. Eles encontraram mais de um milhão de eventos de splicing nas comparações, com dois tipos — pular segmentos inteiros e escolher entre segmentos mutuamente exclusivos — sendo especialmente comuns. Quando analisaram apenas mudanças que eram ao mesmo tempo frequentes e estatisticamente robustas, observaram centenas a milhares de alterações de splicing à medida que o endométrio passava da fase não receptiva para a receptiva, particularmente da fase inicial (pré‑receptiva) para a janela de implantação. Muitas dessas mudanças ocorreram mesmo quando a quantidade total do gene permaneceu a mesma, o que significa que a forma da proteína mudou sem alteração na atividade gênica global.
Células aderindo, se remodelando e comunicando-se com o sistema imune
Genes afetados por splicing alterado e por mudanças de atividade estavam fortemente envolvidos em como as células se aderem umas às outras, como seu arcabouço interno é reorganizado e como elas enviam e recebem sinais imunes. Essas funções são cruciais enquanto o endométrio se transforma de uma barreira simples em uma superfície capaz de acolher e ancorar um embrião, ao mesmo tempo em que remodela vasos sanguíneos. Tanto em mulheres férteis quanto nas com falha de implantação, a fase receptiva foi marcada por forte remodelamento nessas vias, mas mulheres com falha recorrente tendiam a mostrar alterações de splicing mais frequentes ou padronizadas de forma diferente. Alguns dos genes envolvidos já foram sugeridos como marcadores da janela ideal de implantação, reforçando a ideia de que não apenas a atividade gênica, mas a forma exata de seus produtos, ajuda a definir quando o endométrio está realmente pronto.
Células imunes e um regulador chave do splicing
A equipe também estimou os tipos de células imunes presentes no tecido a partir dos mesmos dados de RNA. Em mulheres com falha de implantação, a fase receptiva mostrou menos células T citotóxicas e células natural killer em repouso, mas mais monócitos e certos macrófagos em comparação com fases anteriores. Mais tarde, após o fechamento da janela, os padrões mudaram novamente, com alterações em células natural killer ativadas e subtipos de macrófagos. Várias dessas mudanças nas células imunes acompanharam de perto eventos específicos de splicing, sugerindo que a remodelação das mensagens gênicas e o equilíbrio imune estão ligados. Entre as proteínas que controlam o splicing, uma chamada KHDRBS3 destacou‑se como um hub central conectado a muitos dos eventos alterados e consistentemente diminuiu de nível quando o endométrio se tornava receptivo, tanto em mulheres férteis quanto nas afetadas. Isso sugere que ela pode ajudar a promover a troca nos padrões de splicing que acompanha a abertura da janela de implantação. 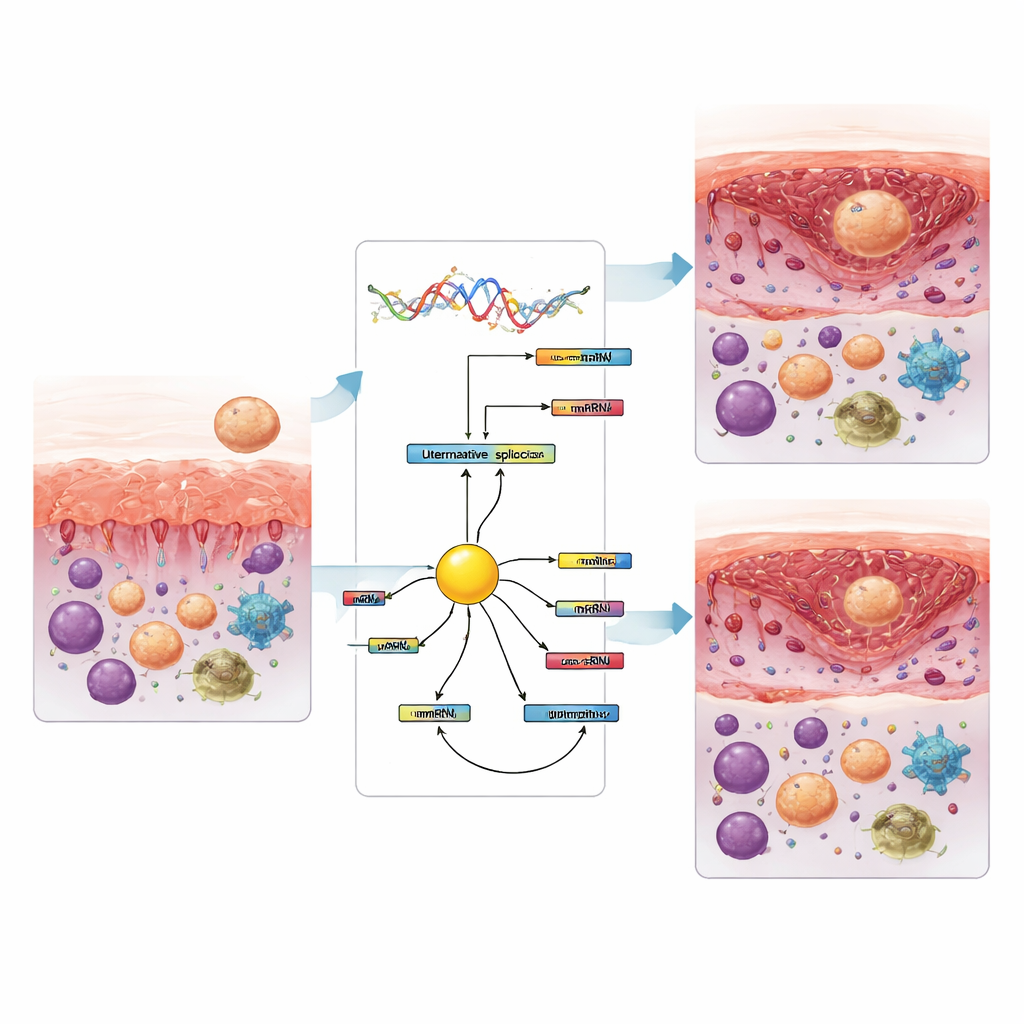
Apontando para futuros testes e tratamentos
Para traduzir esses padrões moleculares em possíveis terapias, os pesquisadores investigaram se pequenas moléculas já existentes poderiam contrariar as assinaturas de splicing anormais observadas. Ao comparar suas listas de genes com grandes bancos de dados de resposta a fármacos, identificaram vários compostos aprovados ou experimentais que miram genes ligados à implantação, incluindo agentes que influenciam respostas imunes ou vias relacionadas a hormônios. Embora esses estejam longe de prontos para uso clínico nesse contexto, oferecem um mapa inicial para testes em laboratório.
O que isso significa para pacientes
De modo geral, o estudo mostra que a falha de implantação não é simplesmente uma questão de ter os "genes errados", mas de como esses genes são editados em mensagens diferentes e de como o ambiente imune do útero é ajustado ao longo do tempo. O trabalho destaca KHDRBS3 e fatores relacionados como reguladores promissores desse processo e revela mudanças coordenadas em células imunes que podem apoiar ou dificultar a tentativa de um embrião de se instalar. A longo prazo, tais insights poderiam levar a testes mais refinados que determinem o tempo e a qualidade reais da janela receptiva de uma mulher, assim como a tratamentos direcionados que ajustem suavemente a mensageria gênica ou o equilíbrio imune para dar aos embriões uma melhor chance de implantação.
Citação: Wang, Ml., Lu, Bj., Lu, X. et al. Alternative splicing and differential gene expression during changes in endometrial receptivity in patients with recurrent implantation failure. Sci Rep 16, 9754 (2026). https://doi.org/10.1038/s41598-026-40386-w
Palavras-chave: receptividade endometrial, falha recorrente de implantação, splicing alternativo, células imunes uterinas, reprodução assistida