Clear Sky Science · pt
Seleção adaptativa de exemplos para detecção explicável de mitoses baseada em protótipos em patologia digital
Por que isso importa para o cuidado do câncer
Quando patologistas examinam amostras de câncer ao microscópio, contar quantas células tumorais estão ativamente se dividindo ajuda a determinar quão agressivo é o tumor e quais tratamentos escolher. A inteligência artificial agora pode identificar rapidamente essas células em lâminas digitais, mas suas decisões frequentemente são um mistério até para especialistas. Este artigo apresenta um método chamado Seleção Adaptativa de Exemplos (AES) que permite que um sistema de IA “mostre seu raciocínio” apontando para casos reais anteriores que suportam ou contradizem cada decisão, tornando a detecção automatizada de mitoses mais transparente e confiável clinicamente.
O desafio de identificar células em divisão
As células tumorais em divisão, conhecidas como figuras mitóticas, são pequenas, raras e visualmente diversas. Sob a coloração típica rosa e roxa, elas podem se assemelhar muito a estruturas inofensivas, como células em morte ou certos tipos de células imunes. Especialistas humanos precisam vasculhar lâminas digitais enormes para encontrá‑las, um processo lento, cansativo e suscetível a discordâncias. Sistemas modernos de deep learning podem igualar ou superar o desempenho de especialistas nessa tarefa, mas funcionam como caixas‑pretas: produzem um escore para cada célula suspeita sem explicar claramente o porquê. Na medicina, onde decisões de tratamento podem mudar vidas, essa falta de clareza é um obstáculo sério para o uso rotineiro de IA.
Construindo um detector poderoso, porém opaco
Os autores primeiro treinam uma rede de detecção de objetos de última geração, baseada na arquitetura Faster R-CNN, para localizar figuras mitóticas em um grande e diversificado conjunto de dados chamado MIDOG++. Essas imagens vêm tanto de tumores humanos quanto caninos, abrangendo vários tipos de câncer e laboratórios, e incluem mais de onze mil células em divisão cuidadosamente anotadas. Para preservar detalhes finos, as lâminas são cortadas em pequenos blocos e fortemente aumentadas para imitar variações reais na coloração e na aquisição das imagens. O detector resultante alcança desempenho sólido entre os tipos tumorais, com F1‑scores de até 0,84, confirmando que é preciso, mas complexo — justamente o tipo de sistema que precisa de explicações melhores antes que clínicos possam confiar nele na prática.
Ensinando a IA a se explicar com exemplos
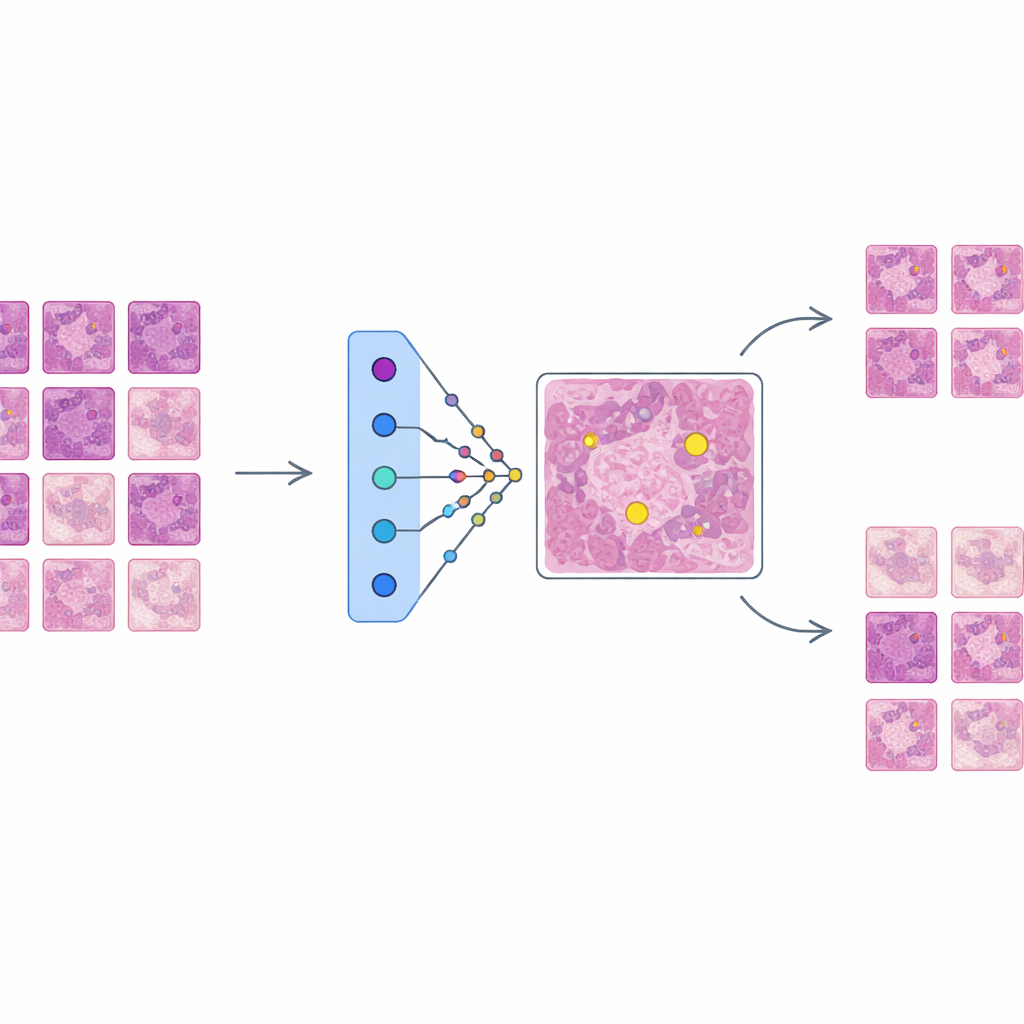
O AES atua sobre esse detector treinado como uma camada de interpretabilidade, em vez de alterar o funcionamento do detector. Para cada região candidata que o detector marca como possivelmente mitótica, o AES consulta uma biblioteca de fragmentos de tecido reais extraídos dos dados de treinamento. Dessa biblioteca, seleciona um pequeno conjunto de exemplos “de apoio” que se assemelham a mitoses verdadeiras e um conjunto de exemplos “contraditórios” que se parecem mais com células não mitóticas. Nos bastidores, o AES trata os escores de confiança do detector como uma superfície contínua e usa uma ferramenta matemática chamada funções de base radial para aproximar como essa confiança varia perto de cada caso. Apenas protótipos que influenciam de forma significativa a confiança local são mantidos, de modo que a explicação para uma decisão costuma envolver cerca de dez exemplos cuidadosamente escolhidos em vez de centenas de exemplos pouco relevantes.
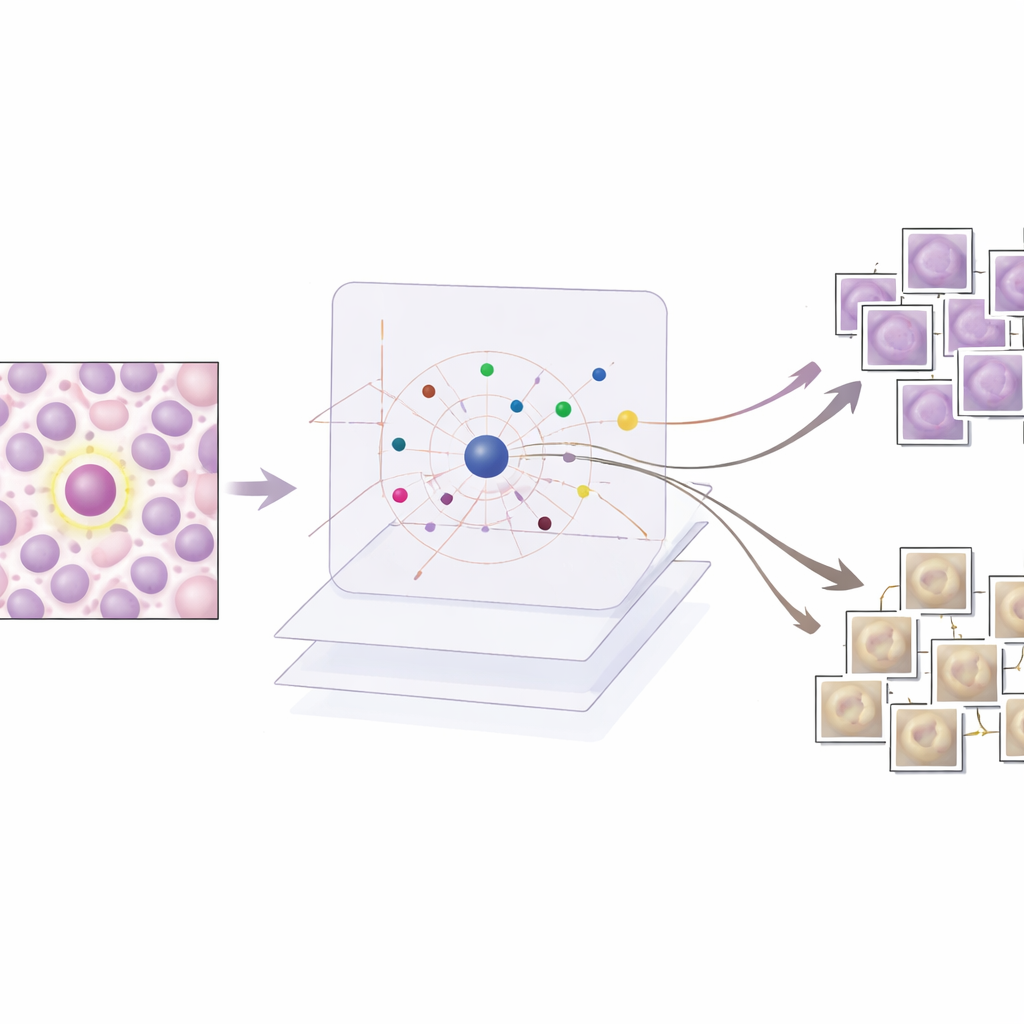
O que os exemplos revelam sobre as decisões da IA
Os pesquisadores avaliam o AES tanto quantitativamente quanto qualitativamente. Em termos numéricos, mostram que um dicionário compacto de cerca de 190 imagens‑protótipo pode reproduzir os escores de confiança do detector com alta acurácia, mantendo o número de exemplos apresentados por caso baixo o suficiente para revisão humana. Em termos qualitativos, examinam três cenários comuns. Quando o detector está claramente correto, o AES retorna apenas protótipos mitóticos que suportam fortemente a decisão, o que traz segurança aos clínicos. Para alarmes falsos, o método destaca protótipos mitóticos semelhantes que mostram por que o detector foi enganado por texturas ou padrões de cromatina parecidos, frequentemente junto com protótipos não mitóticos mais fracos que indicam incerteza. Para mitoses perdidas, o AES tende a retornar principalmente protótipos não mitóticos ou exemplos ambíguos, apontando para pontos cegos nos dados de treinamento e sugerindo onde são necessários exemplos novos ou melhor rotulados.
De caixa‑preta a ferramenta colaborativa
Ao fundamentar cada predição em um punhado de fragmentos de tecido reais e rotulados, o AES faz um detector de IA complexo comportar‑se mais como um colega humano que justifica decisões lembrando casos passados. O sistema não apenas informa se uma célula provavelmente está em divisão, mas também mostra por que e com que confiança, por meio da combinação e da influência de protótipos que apoiam ou contradizem a decisão. Esse desenho permite que patologistas confirmem rapidamente predições fortes, concentrem atenção em regiões limítrofes ou confusas e identifiquem padrões sistemáticos de erro que podem orientar novos treinamentos. Embora desenvolvido para detecção de mitoses, a mesma abordagem pode ser estendida a outras tarefas em patologia digital, ajudando a mover a IA de uma automação opaca para um assistente interpretável baseado em casos, que clínicos possam questionar, confiar e aprimorar.
Citação: Banik, M., Kreutz-Delgado, K., Mohanty, I. et al. Adaptive example selection for prototype based explainable mitosis detection in digital pathology. Sci Rep 16, 9481 (2026). https://doi.org/10.1038/s41598-026-40283-2
Palavras-chave: IA explicável, patologia digital, detecção de mitoses, modelos baseados em protótipos, diagnóstico de câncer