Clear Sky Science · pt
Fonte pulsada ultra-intensa de radiação ionizante baseada em aceleração direta de elétrons por laser para estudar o efeito FLASH
Por que pulsos de radiação ultrarrápidos importam
A radioterapia contra o câncer anda na corda bamba: dar radiação suficiente para eliminar tumores sem causar danos duradouros ao tecido saudável. Uma ideia recente e empolgante, chamada efeito FLASH, sugere que administrar a radiação em um pulso ultracurto e ultra-intenso pode poupar o tecido normal enquanto ainda ataca o câncer. Este estudo apresenta um novo tipo de fonte experimental de radiação baseada em um laser de alta potência que cria explosões extremamente breves de elétrons de alta energia, e a usa para observar como o oxigênio em água e líquidos biológicos é subitamente consumido durante a irradiação — um processo considerado central para o efeito FLASH. 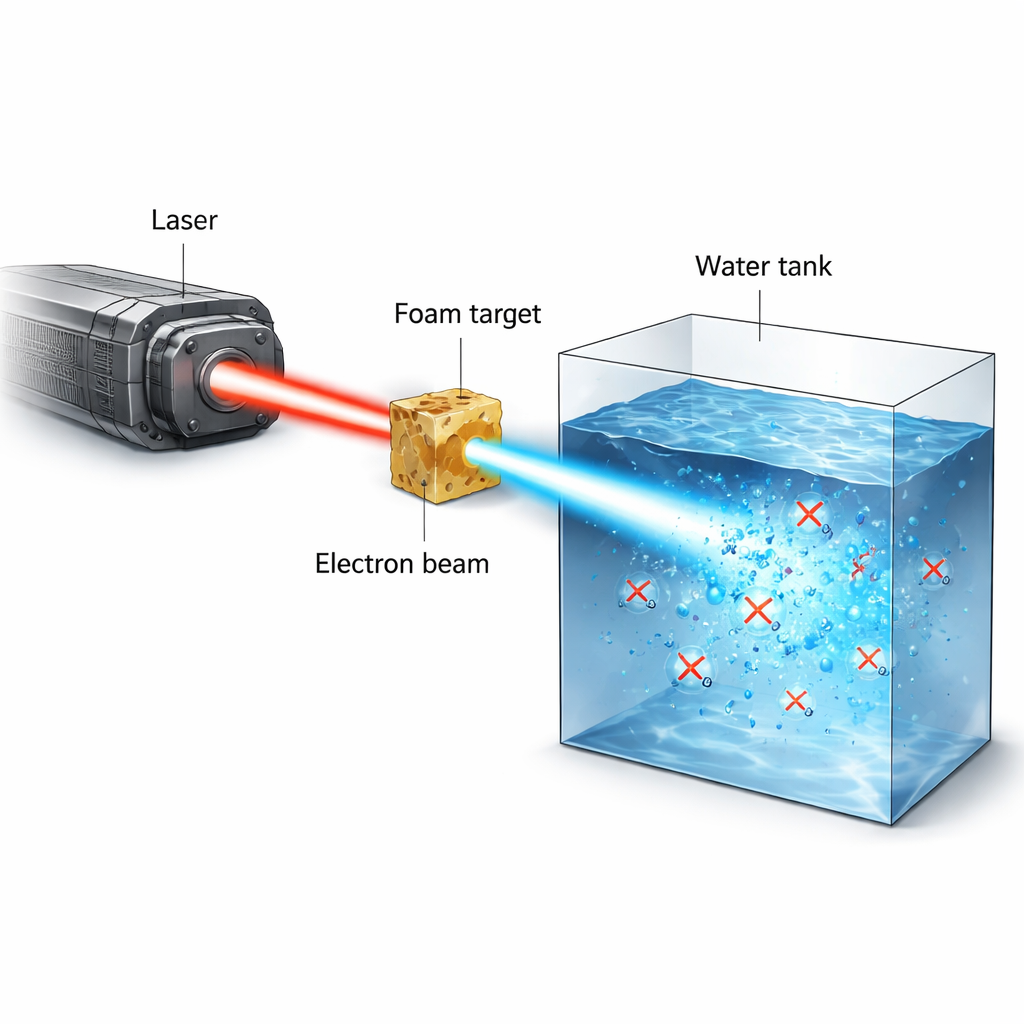
Das máquinas hospitalares para feixes gerados por laser
A radioterapia convencional usa raios X, elétrons ou prótons vindos de grandes aceleradores. Essas máquinas normalmente entregam dose ao longo de milissegundos a segundos e, embora sejam muito precisas, ainda danificam o tecido normal porque a radiação quebra o DNA de forma indireta ao partir moléculas de água e gerar espécies reativas de oxigênio. O oxigênio em tecido saudável e bem vascularizado na verdade agrava esse dano — o chamado efeito do oxigênio. A radioterapia FLASH pretende inverter esse cenário ao entregar a dose terapêutica completa em uma fração de segundo a taxas de dose ultra-altas, o que parece proteger temporariamente o tecido normal em estudos com animais sem proteger os tumores. Contudo, aceleradores médicos padrão têm dificuldade em alcançar essas taxas extremas, o que motiva a busca por fontes alternativas, como lasers de alta potência.
Transformando espuma e luz em um pulso potente de elétrons
Os pesquisadores usaram o laser de alta potência PHELIX para criar feixes estreitos e de alta corrente de elétrons com energias de vários milhões de elétron-volts (MeV). O laser primeiro ioniza uma espuma polimérica de baixa densidade em um plasma quase-crítico. Em um segundo pulso ultracurto, com duração menor que um trilionésimo de segundo, o laser empurra e aprisiona elétrons dentro de um canal de plasma, acelerando-os diretamente até energias elevadas. Esse processo, chamado aceleração direta por laser, produz um feixe fortemente colimado que pode transportar dezenas de nanocoulombs de carga em um pulso de escala de picosegundos. Quando esse feixe incide sobre água ou material semelhante à água, pode depositar 20–50 gray de dose de radiação em um único disparo, com taxas de dose instantâneas acima de 10¹³ gray por segundo — muito além do que máquinas convencionais conseguem alcançar.
Observando o oxigênio desaparecer em um flash
Para sondar como tais explosões intensas afetam a química em condições semelhantes a tecidos, a equipe construiu tanques selados de água que podiam operar em vácuo e ser preenchidos com água pura, meio de cultura ou células lisadas, todos previamente totalmente oxigenados. O feixe de elétrons foi moldado e filtrado de modo que elétrons de alta energia dominassem a dose dentro do tanque, enquanto prótons e raios X eram amplamente suprimidos ou cuidadosamente contabilizados usando camadas de blindagem e filmes radiocrômicos. Um sensor óptico colocado na parede interna do tanque monitorava o oxigênio dissolvido medindo como as moléculas de oxigênio abafavam a luminescência de uma mancha de corante. Após cada irradiação de pulso único, o sensor registrou uma queda súbita na concentração de oxigênio que então relaxava lentamente conforme o oxigênio difundia-se na região do sensor. Combinando dados dos filmes, simulações e o poder de parada conhecido dos elétrons, os autores reconstruíram a dose entregue ao volume irradiado e a vincularam diretamente à perda de oxigênio medida. 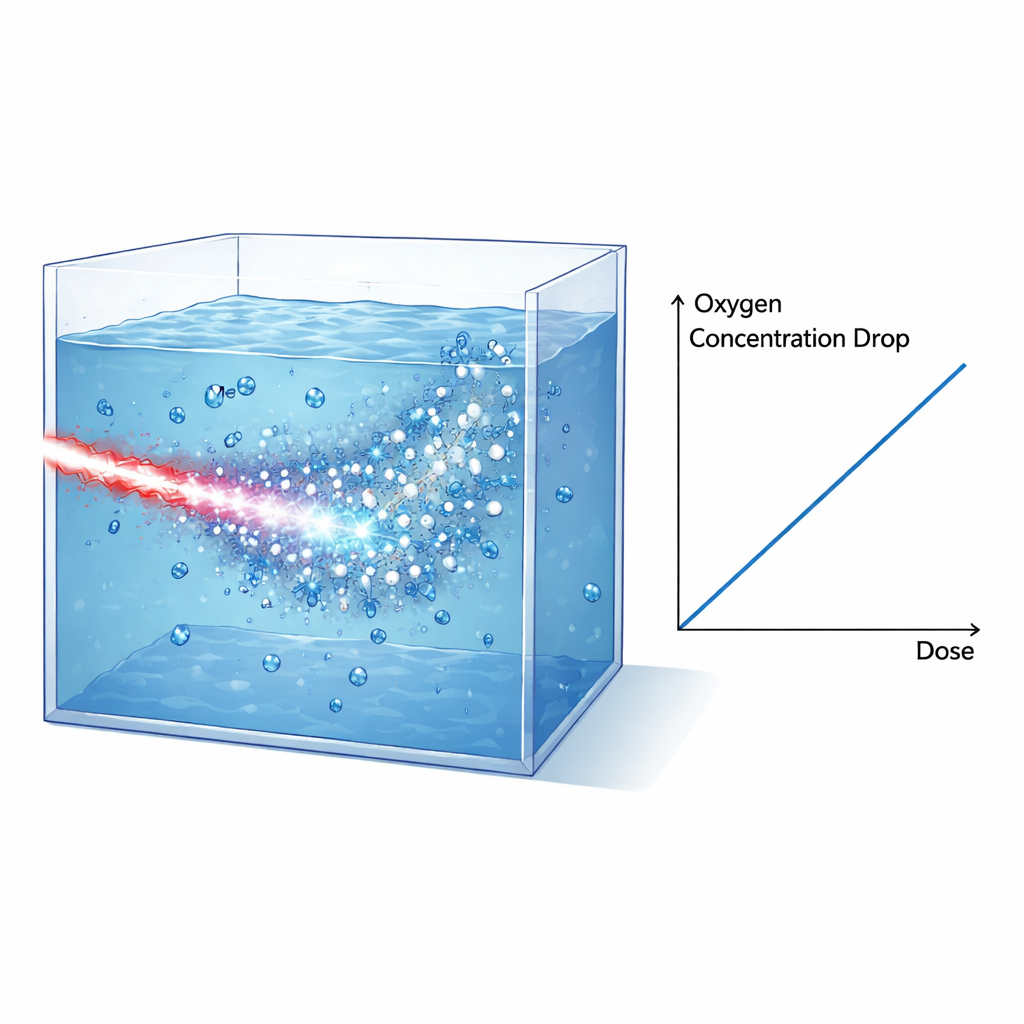
Ligando experimento e teoria
A descoberta-chave é que a diminuição do oxigênio dissolvido é proporcional à dose entregue tanto em água quanto em meio de cultura, com declividades muito semelhantes. Após corrigir por uma pequena dose adicional de raios X, o consumo de oxigênio medido na água é de cerca de 0,32 micromoles por litro por gray. Esse valor corresponde notavelmente bem às previsões de simulações detalhadas de estrutura de trilhas por Monte Carlo (TRAX-CHEM), que seguem os caminhos dos elétrons na água e modelam a química rápida que se desenrola nos microssegundos após a irradiação. Crucialmente, nesse arranjo impulsionado por laser, quase toda a dose é entregue em cerca de um picosegundo — muito mais curto que os tempos característicos para as reações químicas subsequentes. Isso significa que o experimento reproduz de perto as condições ideais assumidas nessas simulações, fornecendo um teste rigoroso dos modelos subjacentes.
Construindo um banco de testes melhor para a ciência FLASH
Além de validar a teoria, os autores usam seus resultados para projetar uma configuração experimental aprimorada. Ao simplificar a geometria, eliminar ímãs e dispor simetricamente água e filmes medidores de dose ao redor do feixe, montagens futuras poderiam medir diretamente a dose dentro do tanque sem reconstruções complexas, enquanto suprimem ainda mais as contribuições indesejadas de prótons e raios X. Simulações mostram que modificar o alvo — por exemplo, adicionando camadas finas de plástico ou ouro — permite ajustar a dose por disparo entre aproximadamente 40 e 80 gray, oferecendo uma plataforma flexível para explorar uma ampla gama de condições relevantes para FLASH.
O que isto significa para tratamentos futuros do câncer
Para não especialistas, a mensagem central é que essa fonte baseada em laser cria pulsos de elétrons extremamente intensos e ultracurtos que imitam — e em alguns aspectos superam — as condições imaginadas para a radioterapia FLASH. O estudo mostra que esses pulsos consomem rapidamente o oxigênio dissolvido em água e meios biológicos de uma forma que concorda com previsões teóricas avançadas. Como a depleção de oxigênio e a química dos radicais associados são as principais candidatas para explicar por que o FLASH pode poupar o tecido saudável, dispor de uma fonte controlável e bem compreendida como esta é um passo importante. Ela fornece um banco de testes poderoso para refinar modelos e, em última instância, orientar o projeto de futuras máquinas clínicas que possam tratar o câncer de forma mais eficaz, reduzindo os efeitos colaterais.
Citação: Gyrdymov, M., Bukharskii, N., Fabian, V. et al. Ultra-intense pulsed source of ionizing radiation based on direct laser acceleration of electrons for studying the FLASH effect. Sci Rep 16, 7164 (2026). https://doi.org/10.1038/s41598-026-40281-4
Palavras-chave: Radioterapia FLASH, elétrons acelerados por laser, taxa de dose ultra-alta, depleção de oxigênio, radiólise da água