Clear Sky Science · pt
Clareamento seletivo de anticorpos monoclonais pelo receptor da manose depende do pareamento de glicanos
Por que os padrões de açúcar em medicamentos importam
Muitos dos medicamentos de maior sucesso atualmente são anticorpos monoclonais — proteínas projetadas que podem permanecer na corrente sanguínea por semanas e atingir com precisão doenças como câncer e desordens autoimunes. Mas nem todos os anticorpos se comportam da mesma forma após a injeção. Este estudo faz uma pergunta aparentemente simples, com grandes consequências: como o fino “padrão de açúcares” ligado a um anticorpo determina a velocidade com que o corpo o remove, e isso poderia também moldar efeitos colaterais como reações imunes?
Açúcares minúsculos como sinais de trânsito
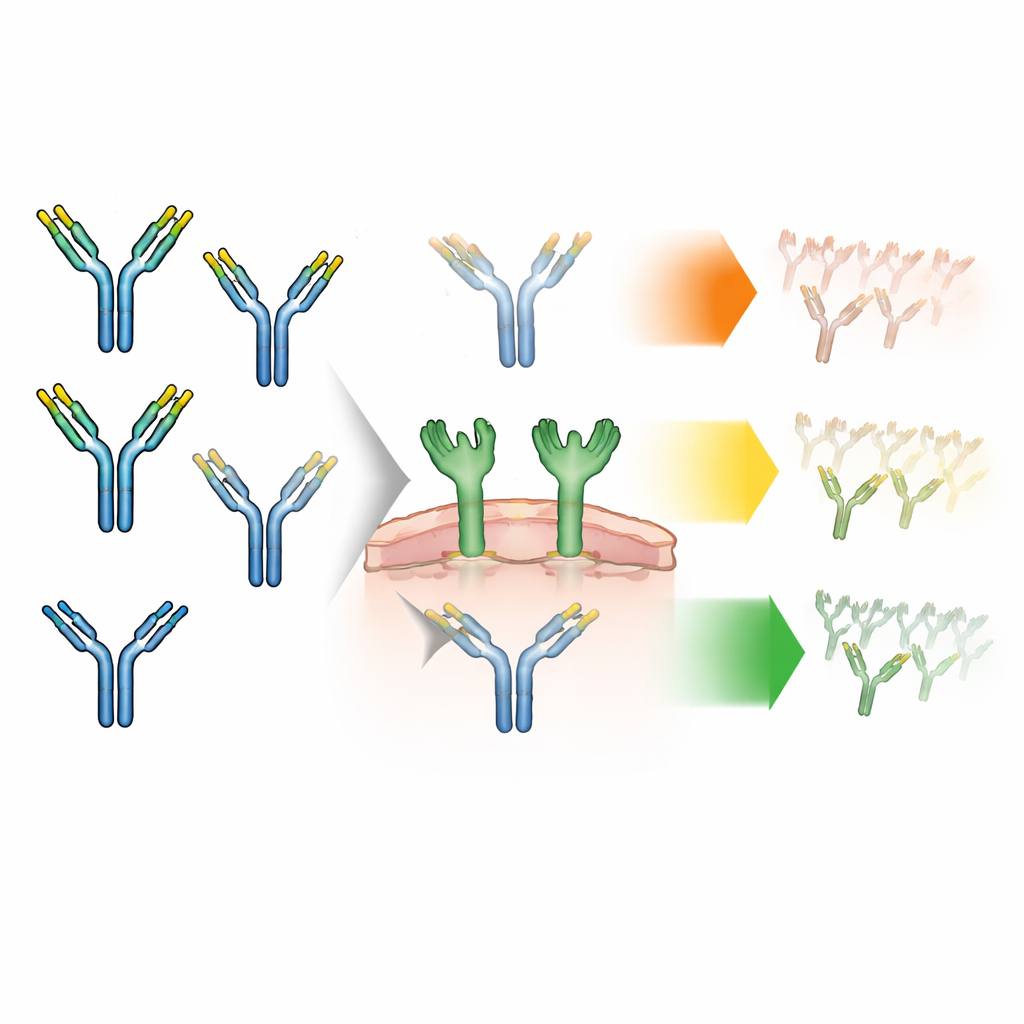
Anticorpos carregam naturalmente pequenas cadeias de açúcares — chamadas glicanos — em sua espinha dorsal. Esses glicanos aparecem em formatos diferentes. A maioria é do tipo “complexo”, mas uma minoria é “alto em manose” (high-mannose), um tipo mais simples que estudos anteriores associaram à remoção mais rápida do sangue. Cada anticorpo tem dois sítios de açúcar que atuam como um par, e esses podem ser iguais (pares simétricos) ou diferentes (pares assimétricos). Até agora, os fabricantes de medicamentos geralmente contavam quantos de cada tipo de açúcar estavam presentes no total, sem considerar como os dois açúcares no mesmo anticorpo eram pareados. Os autores suspeitaram que esse padrão de pareamento poderia alterar o grau de interação dos anticorpos com uma proteína sensora de açúcares nas células imunes chamada receptor da manose — e, portanto, quão rápido o corpo elimina o medicamento.
Separando anticorpos pelos seus pares de açúcares
Para investigar isso, a equipe engenheirou anticorpos enriquecidos em glicanos alto em manose e depois os separou fisicamente em três grupos principais: anticorpos com dois glicanos complexos, com um glicano complexo e um alto em manose (assimétrico), ou com dois glicanos alto em manose (simétrico). Eles verificaram cuidadosamente que esses grupos eram quase idênticos em todos os outros aspectos: mesmo tamanho, forma, carga e estabilidade, e ligação semelhante ao receptor de reciclagem que normalmente protege anticorpos da degradação. Isso significava que quaisquer diferenças observadas posteriormente em experimentos celulares ou em animais poderiam ser atribuídas apenas ao pareamento de glicanos, e não a danos ocultos ou impurezas.
Observando células engolirem anticorpos
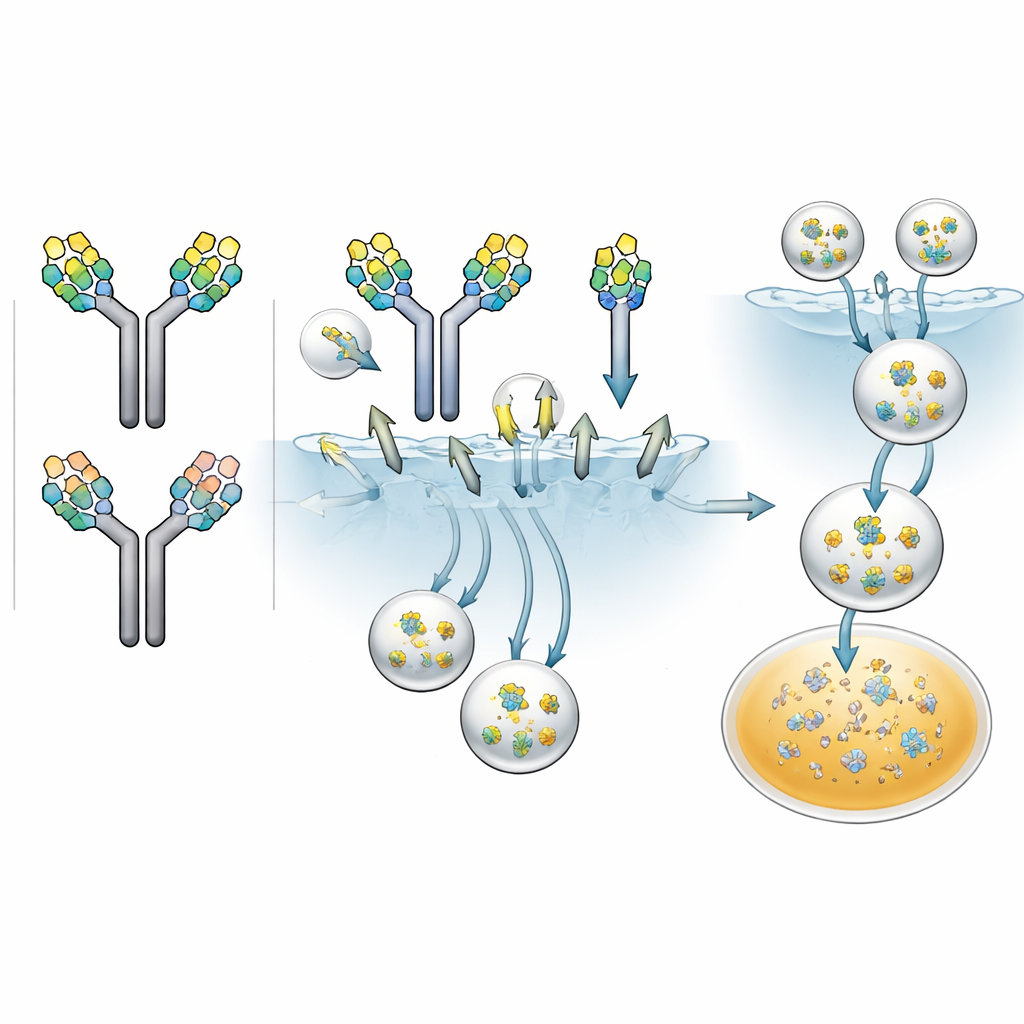
Em seguida, os pesquisadores mediram quão rapidamente cada padrão de açúcar permitia que os anticorpos fossem internalizados por células que exibem o receptor da manose. Eles marcaram as diferentes frações de anticorpos com uma etiqueta fluorescente e as incubaram com células humanas modificadas para apresentar esse receptor. Ao longo de quase três dias, monitoraram o brilho dentro das células como medida de captação. Todos os anticorpos foram internalizados em alguma medida, mas as taxas variaram: aqueles com dois glicanos alto em manose foram internalizados mais rapidamente, os com um glicano alto em manose tiveram taxa intermediária, e os com apenas glicanos complexos foram os mais lentos. Quando a equipe adicionou manana — um açúcar natural que compete pelo receptor da manose — a captação dos anticorpos alto em manose caiu drasticamente, confirmando que esse receptor era responsável por grande parte da internalização rápida.
Seguindo anticorpos marcados por açúcar em animais vivos
O teste crucial foi saber se essas diferenças celulares se traduziriam no comportamento real do fármaco. Os cientistas formularam um produto com anticorpos ricos tanto em pares alto em manose simétricos quanto assimétricos, além de pares apenas com glicanos complexos, e injetaram-no em ratos. Usando métodos sensíveis de espectrometria de massa, puderam rastrear não apenas o nível total de anticorpo ao longo de duas semanas, mas também como cada pareamento de glicanos declinou com o tempo. O padrão foi marcante: anticorpos com dois glicanos alto em manose desapareceram mais rápido, com meia-vida de cerca de 2,4 dias; aqueles com um glicano alto em manose duraram mais, cerca de 7,2 dias; e os com apenas glicanos complexos persistiram por aproximadamente 17,4 dias. A exposição ao longo do tempo — a área sob a curva de concentração — caiu para 38% para o par duplo alto em manose e para 73% para o par misto, em comparação com o par apenas complexo. Em essência, cada glicano alto em manose adicional agiu como uma bandeira extra de “claire-me” para o receptor da manose.
O que isso significa para medicamentos mais seguros e duradouros
Para pacientes, esses resultados esclarecem por que dois medicamentos anticorpos que parecem semelhantes no papel podem se comportar de forma diferente no organismo. O estudo mostra que não apenas a presença, mas o pareamento de glicanos alto em manose direciona fortemente a velocidade de remoção dos anticorpos, provavelmente por meio da captação e degradação mediadas pelo receptor da manose dentro de células imunes. Como a mesma via também pode direcionar antígenos para o maquinário que desencadeia respostas imunes, esses padrões de glicanos podem influenciar o risco de anticorpos anti-fármaco e reações alérgicas. Os autores argumentam que os fabricantes devem monitorar e controlar o pareamento de glicanos — não apenas a composição total de açúcares — ao projetar e testar terapias com anticorpos. Fazer isso pode ajudar a garantir dosagens mais previsíveis, benefícios de maior duração e menor probabilidade de respostas imunes indesejadas.
Citação: Baumeister, J., Meudt, M., Wei, W. et al. Selective clearance of monoclonal antibodies via the mannose receptor is dependent on glycan pairing. Sci Rep 16, 8489 (2026). https://doi.org/10.1038/s41598-026-40268-1
Palavras-chave: anticorpos monoclonais, glicosilação, receptor da manose, farmacocinética, imunogenicidade