Clear Sky Science · pt
Evolução molecular e diversidade da RNA-polimerase dependente de RNA do norovírus
Por que os vírus intestinais continuam nos surpreendendo
O norovírus é o infame vírus da “gripe estomacal” que pode paralisar navios de cruzeiro, escolas e hospitais em poucos dias. Ele se espalha facilmente, adoecendo centenas de milhões de pessoas por ano, e gera constantemente novas variantes. Este estudo examina o motor dessa evolução, concentrando-se em uma única enzima viral — uma “máquina de copiar” interna chamada RNA-polimerase — para investigar como ela muda ao longo do tempo e quão estável realmente é. Compreender esse motor oculto de mudança pode ajudar a explicar por que algumas linhagens de norovírus dominam globalmente e orientar o desenho de futuros antivirais.
A máquina interna de copiar do vírus
O norovírus carrega seu material genético em forma de RNA e depende de uma enzima chamada RNA-polimerase dependente de RNA para copiar esse RNA dentro das células infectadas. Essa enzima, com cerca de 510 blocos de construção, assemelha-se a uma mão enrolada com dedos, palma e polegar, formando um canal por onde o RNA e os novos blocos passam. Dentro dessa estrutura estão sete pequenos “pontos quentes” quase idênticos entre as linhagens; essas regiões executam a química central da cópia do genoma. Como a polimerase é essencial para a reprodução do vírus, mesmo pequenas perturbações nesses pontos quentes podem ser desastrosas para o vírus, de modo que a evolução tende a preservá-los com extremo rigor.
Centos de linhagens, algumas famílias-chave
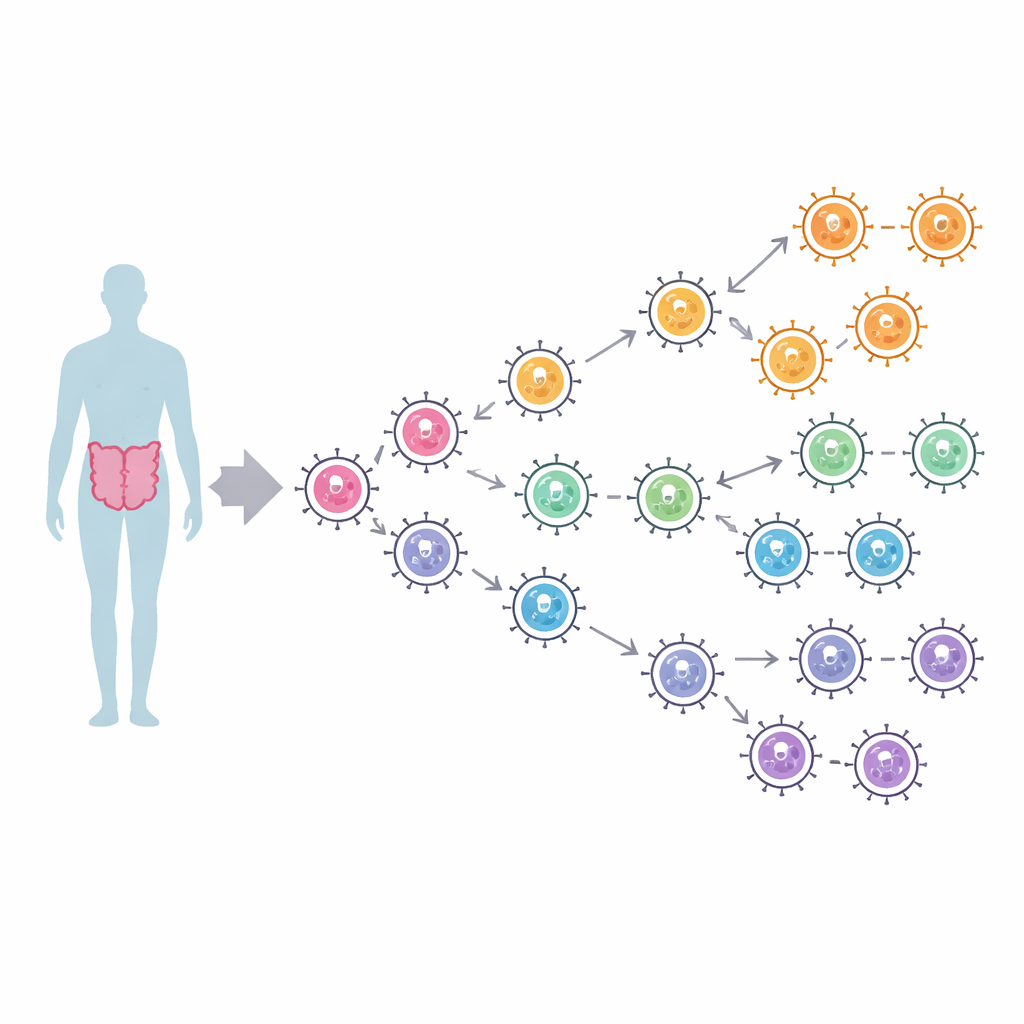
Os pesquisadores reuniram 1.094 sequências completas de polimerase de dois grandes grupos humanos de norovírus, denominados GI e GII, coletadas mundialmente entre 1972 e 2024. Usando árvores filogenéticas computacionais que incorporam datas e locais de amostragem, traçaram como essas enzimas se ramificaram ao longo de quase quatro séculos. As polimerases GI dividiram-se em três linhagens principais que provavelmente se separaram a partir do século XVII, enquanto as polimerases GII formaram quatro linhagens, incluindo um ramo distinto para um tipo conhecido como P16. As infecções modernas são dominadas por dois tipos de polimerase GII, P16 e P31, ambos historicamente associados ao genótipo de cápside pandêmico duradouro GII.4. Ainda assim, apesar da disseminação global, as árvores mostraram pouco agrupamento geográfico — linhagens de diferentes continentes se misturam — sugerindo que o norovírus circula rapidamente pelo mundo sem permanecer confinado a regiões específicas.
Mudança lenta e constante com núcleos bem protegidos
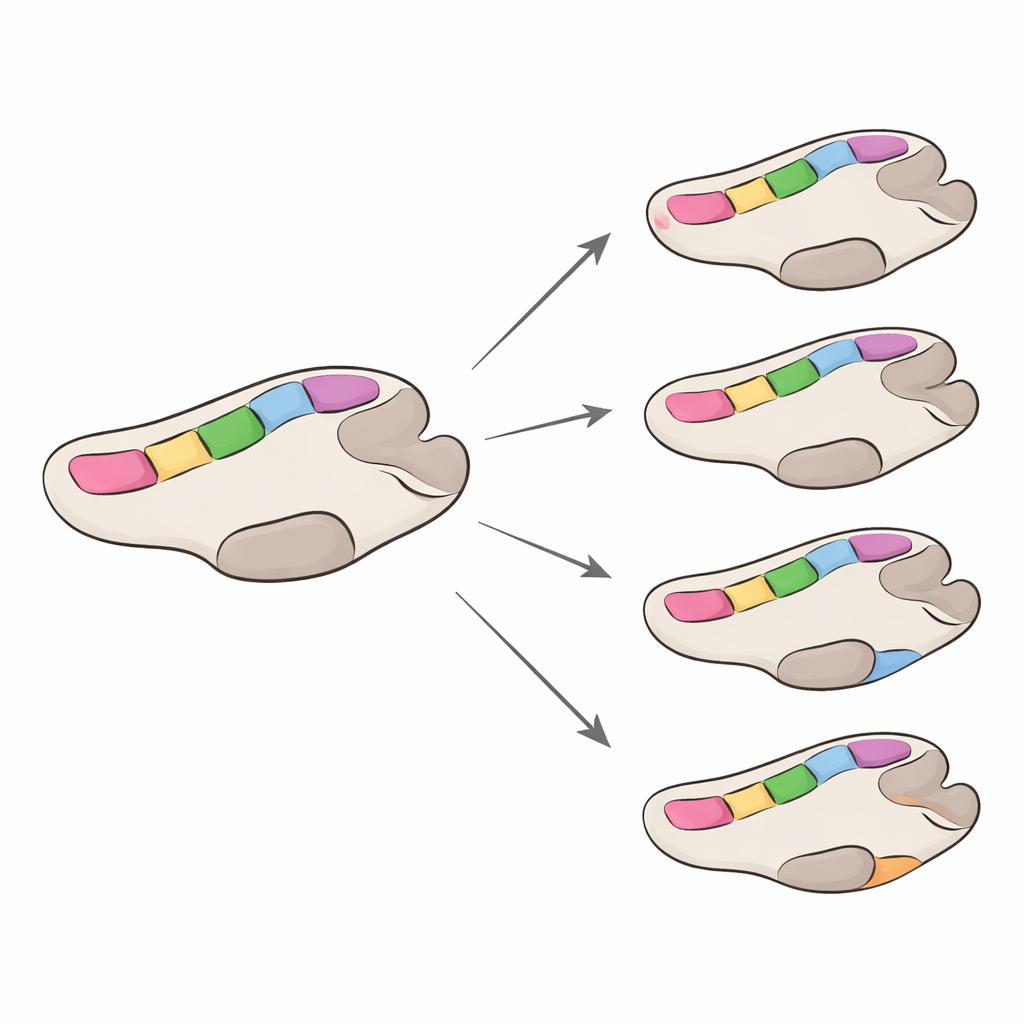
Ao comparar os aminoácidos em cada posição da polimerase, a equipe catalogou milhares de alterações entre os tipos. Encontraram muito menos mudanças em GI do que em GII, refletindo em parte o menor número de sequências disponíveis, mas emergiu um padrão claro: os sete pontos quentes conservados e o sítio de ligação ao RNA nas proximidades permaneceram quase intactos. Quando ocorreram substituições ali, trataram-se geralmente de trocas sutis entre aminoácidos quimicamente semelhantes, indicando que a enzima tolera apenas ajustes muito leves nessas zonas cruciais. A maioria das mudanças frequentes concentrou-se nos “dedos” e em outras regiões externas da enzima, afastadas da química central. Algumas posições até exibiram mudanças reversíveis ao longo de diferentes tipos de polimerase, um sinal de evolução convergente em que linhagens não relacionadas chegam a soluções semelhantes.
Velocidades diferentes para famílias virais distintas
A equipe então estimou quão rápido a polimerase evolui, com foco em alterações que mudam aminoácidos, as quais têm maior probabilidade de afetar a função. Em geral, as polimerases GII mudaram cerca de quatro vezes mais rápido que as GI, embora ambos evoluam mais lentamente do que a proteína externa do norovírus, conhecida por mudar rapidamente para escapar da imunidade. Dentro de cada grupo, alguns tipos de polimerase evoluíram um pouco mais rápido que outros, mas as diferenças foram modestas. Importante, a maioria das posições na enzima estava sob forte pressão de “purificação” — mutações que atrapalham a função foram eliminadas — enquanto apenas um punhado de sítios mostrou sinais de serem favorecidos pela seleção natural. Quando esses sítios sob seleção positiva foram mapeados em modelos tridimensionais da enzima, eles quase sempre ficaram fora dos pontos quentes mais conservados, embora alguns estivessem próximos o suficiente para possivelmente ajustar como a polimerase se liga ao RNA ou se move durante a cópia.
O que isso significa para surtos futuros e tratamentos
Em conjunto, esses achados desenham a polimerase do norovírus como um núcleo surpreendentemente estável envolto por regiões mais flexíveis que permitem adaptação gradual. As polimerases GII, especialmente as associadas a linhagens historicamente pandêmicas, estão evoluindo um pouco mais rápido, o que pode ajudar esses vírus a acompanhar mudanças no hospedeiro e variantes concorrentes. Ainda assim, a profunda conservação das regiões funcionais-chave ao longo de séculos sugere que essa enzima é um alvo promissor e estável para antivirais: interrompa a máquina central de cópia e o vírus tem pouca margem para escapar sem se incapacitar. Para não especialistas, a conclusão é que, enquanto as faces externas do norovírus provavelmente continuarão a mudar, tornando novos surtos inevitáveis, o motor interno que impulsiona essas mudanças é tanto rigidamente restrito quanto cientificamente acessível — oferecendo um alvo firme para futuras terapias.
Citação: Flint, A., Jawad, M. & Nasheri, N. Molecular evolution and diversity of the norovirus RNA-dependent RNA polymerase. Sci Rep 16, 9042 (2026). https://doi.org/10.1038/s41598-026-40248-5
Palavras-chave: norovírus, evolução viral, RNA-polimerase, alvos antivirais, epidemiologia molecular