Clear Sky Science · pt
Caracterização multimodal do início e crescimento de trombos induzidos por fluxo em oxigenação por membrana extracorpórea
Por que coágulos sanguíneos em aparelhos de suporte de vida importam
A oxigenação por membrana extracorpórea, ou ECMO, é uma forma de derivação coração-pulmão que pode manter pacientes criticamente doentes vivos enquanto seus órgãos se recuperam. Mas fazer o sangue circular por bombas e tubos plásticos o expõe a forças mecânicas severas para as quais nossos corpos não foram projetados. Essas forças podem desencadear coágulos perigosos dentro do circuito, o que por sua vez aumenta o risco de AVC, lesão orgânica ou falha do equipamento. Este estudo teve como objetivo descobrir como, exatamente, o fluxo de sangue através de uma bomba de ECMO molda o surgimento e o crescimento desses coágulos, com a meta de longo prazo de tornar a ECMO mais segura e mais eficaz.
Como a ECMO mantém pacientes vivos
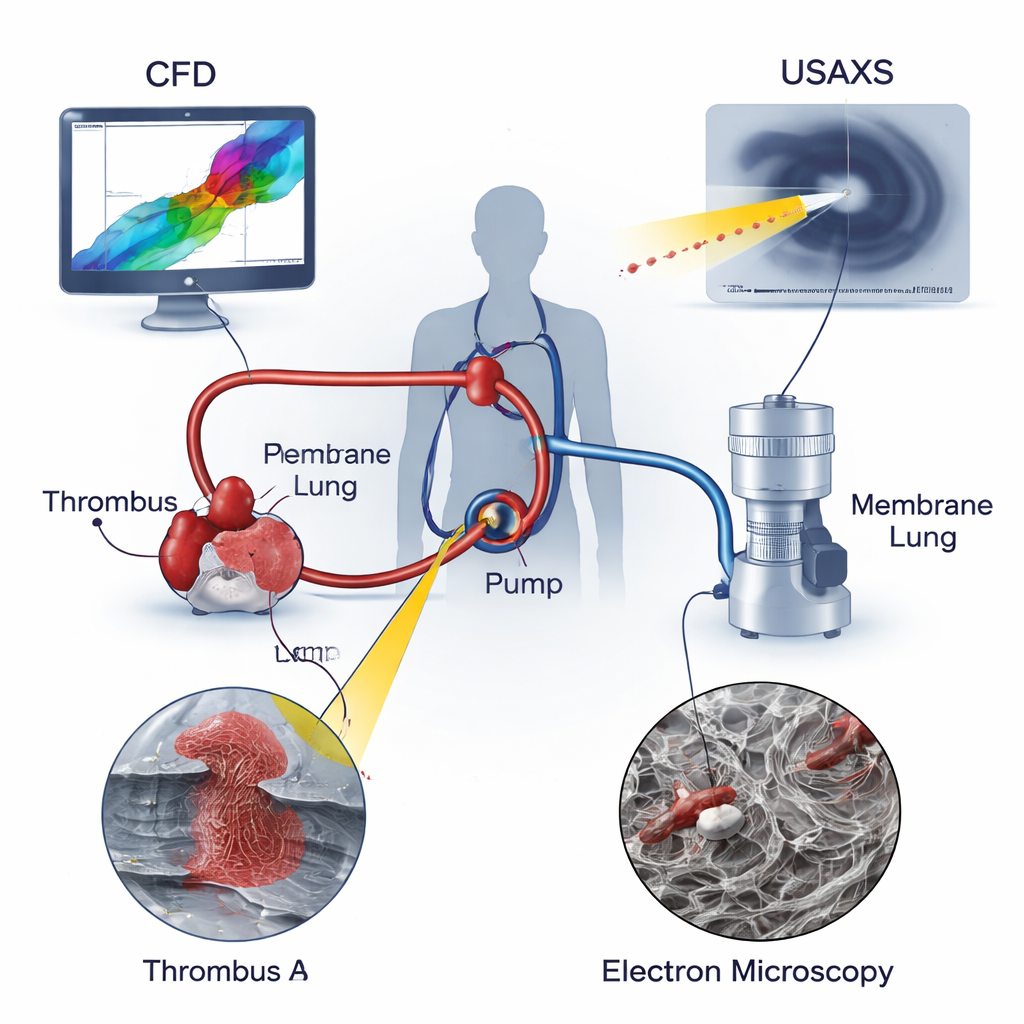
Na ECMO, o sangue é retirado de uma veia ou artéria grande, impulsionado por uma bomba centrífuga através de um “pulmão de membrana” que adiciona oxigênio e remove dióxido de carbono, e então retornado ao paciente. Ao contrário do sangue que flui suavemente por vasos naturais, o fluxo em um circuito de ECMO inclui condições extremas: correntes muito rápidas, mudanças bruscas de direção e bolsões quase estagnados onde o sangue permanece. Esses ambientes são conhecidos por danificar células sanguíneas e estimular a coagulação. Modelos médicos clássicos focam no fluxo lento ou bloqueado em vasos sanguíneos, mas não explicam totalmente o cisalhamento intenso e o alongamento que o sangue experimenta dentro de uma bomba giratória. Os autores defendem que, para entender de fato o risco de coágulos na ECMO, é preciso estudar tanto as forças mecânicas no dispositivo quanto a estrutura microscópica dos trombos que surgem.
Observando os coágulos por três ângulos
Os pesquisadores combinaram três ferramentas poderosas para analisar dois trombos reais retirados de circuitos de ECMO usados em crianças: um trombo na entrada da bomba (Trombo A) e outro em tubulação logo a jusante da bomba (Trombo B). Dinâmica de fluidos computacional (CFD) simulou como o sangue se movimentava pela bomba, revelando regiões de fluxo recirculante e vorticidade e apontando onde o cisalhamento e as forças de alongamento atingiam picos. Difração de raios X em ultra-ângulo pequeno (USAXS) investigou profundamente cada trombo, medindo quão compacta e quão alinhada direcionalmente era a matriz de fibrina — a malha proteica que mantém os coágulos unidos — ao longo da amostra. Microscopia eletrônica de varredura (SEM) forneceu imagens altamente ampliadas das superfícies dos trombos, mostrando as formas dos glóbulos vermelhos, glóbulos brancos, plaquetas e as fibras de fibrina circundantes. Ao sobrepor essas três visões, a equipe conseguiu ligar as condições locais de fluxo à arquitetura interna de cada trombo.
Uma zona de recirculação forma um coágulo rígido e alinhado
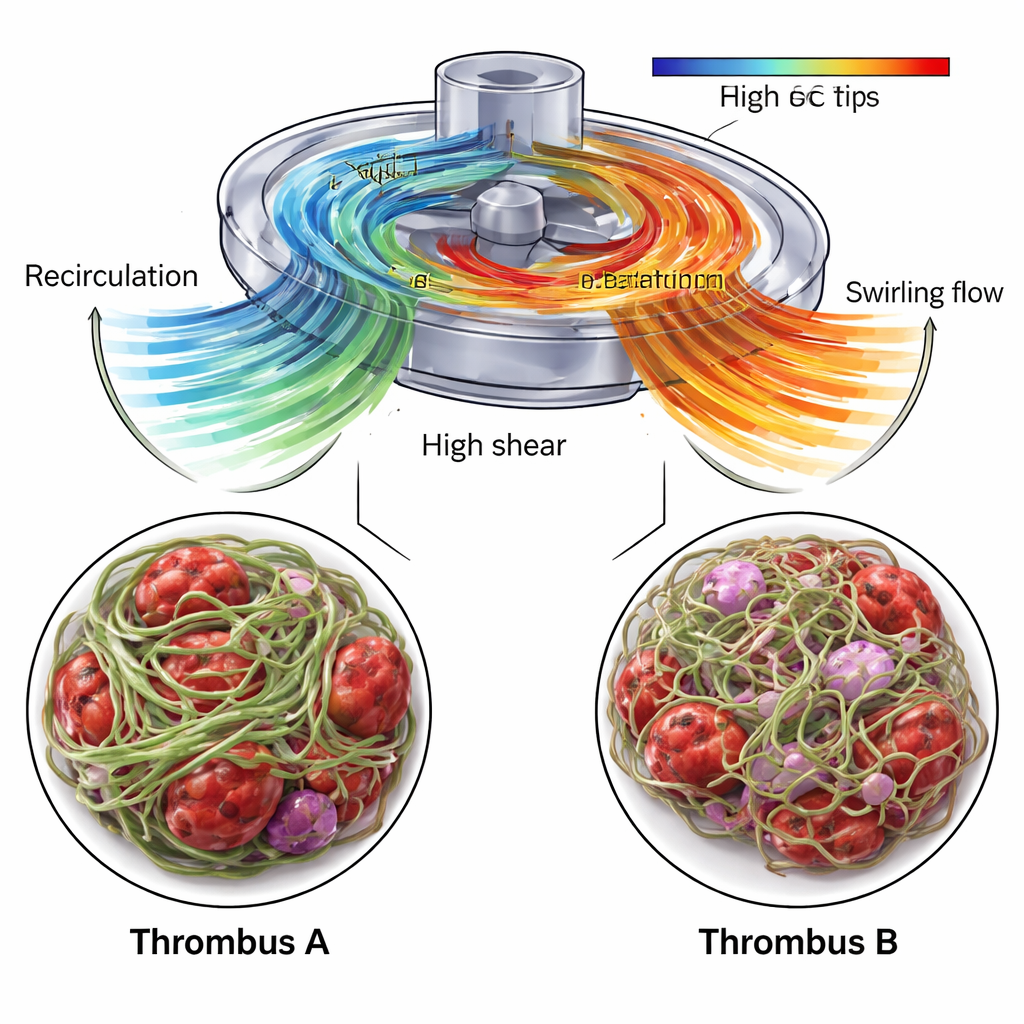
O CFD mostrou que a área próxima à entrada da bomba, onde o Trombo A se formou, continha uma zona de recirculação: o sangue era empurrado para trás e para cima ao longo da carcaça antes de se reintegrar ao fluxo principal. Essa região permitia que os componentes sanguíneos permanecessem por mais tempo, ao mesmo tempo em que experimentavam diferenças bruscas de velocidade na fronteira entre o fluxo recirculante e o fluxo que entrava. Dentro do Trombo A, o USAXS indicou um alto teor de fibrina — pelo menos 70% — e um forte alinhamento geral das fibras em uma direção preferencial, sugerindo uma matriz densa e rígida. As imagens de SEM confirmaram uma rede de fibrina fortemente entrelaçada, intercalada com glóbulos vermelhos de formato anormal e fragmentos de plaquetas. Os autores propõem que a combinação de tempos de residência longos e alto cisalhamento local favoreceu o crescimento de um coágulo compacto e altamente organizado, capaz de suportar os estresses mecânicos da bomba.
O escoamento em rotação molda um coágulo mais frouxo e torcido
Em contraste, o Trombo B, retirado da tubulação após a bomba, cresceu em uma região dominada por escoamento em rotação. O CFD revelou estruturas de fluxo rotativas, em espiral, emergindo da saída da bomba, e os dados de USAXS mostraram uma rede de fibrina que ainda predominava, mas era menos densa e menos fortemente alinhada no conjunto. A direção principal da orientação da fibrina mudou gradualmente através do trombo, de um ângulo de inclinação para outro, ecoando o padrão de fluxo torcido. Imagens de SEM mostraram filamentos de fibrina de espessuras variadas e numerosos glóbulos vermelhos e brancos aprisionados, incluindo sinais de dano celular e inflamação. Importante, as simulações também identificaram pequenas mas significativas partes do volume da bomba onde as forças de alongamento eram altas o suficiente para desenrolar o fator von Willebrand, uma proteína sanguínea chave que se torna pegajosa sob estresse e pode recrutar plaquetas rapidamente. Essas zonas estavam concentradas perto das lâminas do impulsor e da saída, tornando-as locais prováveis para os eventos de ativação inicial que levaram ao Trombo B.
Rumo a aparelhos de suporte de vida mais seguros
Ao unir simulações detalhadas do fluxo sanguíneo com medições por raios X e microscopia eletrônica de trombos reais de ECMO, este trabalho mostra que o “grão” interno e a densidade de um coágulo refletem o ambiente mecânico em que ele se formou. Fluxo recirculante perto da entrada da bomba foi ligado a uma matriz de fibrina densa e altamente alinhada, enquanto o escoamento em rotação foi associado a uma rede mais torcida e aberta que ainda prendia muitas células sanguíneas e imunes. Essas percepções destacam regiões específicas em bombas e tubulação de ECMO onde mudanças de projeto ou ajustes direcionados na anticoagulação poderiam reduzir mais eficazmente o risco de trombose. Em longo prazo, esse mapeamento multiescala — da geometria da bomba e dos padrões de fluxo até o arranjo proteico — pode orientar projetos de dispositivos mais seguros e ajudar os clínicos a equilibrar melhor os perigos duplos de sangramento e trombose durante o suporte vital com ECMO.
Citação: Nilsson, F., Sochor, B., Henriksson, S. et al. Multimodal characterization of flow-induced thrombus initiation and growth in extracorporeal membrane oxygenation. Sci Rep 16, 7166 (2026). https://doi.org/10.1038/s41598-026-40177-3
Palavras-chave: ECMO, coagulação sanguínea, tensão de cisalhamento, bomba de sangue centrífuga, estrutura de fibrina