Clear Sky Science · pt
Ciprofol atenua a lesão por isquemia‑reperfusão cerebral em ratos ao inibir a ferroptose por meio da regulação positiva da AMPK
Por que proteger o cérebro após um AVC é importante
Quando uma pessoa sofre um AVC isquêmico, os médicos se apressam para reabrir o vaso sanguíneo obstruído e restaurar o fluxo de sangue ao cérebro. Paradoxalmente, essa etapa que salva vidas pode causar dano adicional, um fenômeno chamado lesão por reperfusão. O cérebro, subitamente banhado por oxigênio e nutrientes após um período de privação, desencadeia uma tempestade de reações químicas que pode matar neurônios vulneráveis. Este estudo investiga se o ciprofol, um novo anestésico já usado para sedação, também pode proteger o cérebro durante essa janela crítica, acalmando alguns dos processos mais nocivos desencadeados quando o sangue retorna.
Do bloqueio do fluxo sanguíneo ao dano cerebral
Para simular o que ocorre em um AVC humano, os pesquisadores bloquearam temporariamente uma artéria cerebral principal em ratos e então restabeleceram o fluxo sanguíneo, criando o que se conhece como lesão por isquemia–reperfusão cerebral. Alguns ratos apenas foram submetidos ao procedimento, enquanto outros receberam ciprofol logo após a restauração do fluxo. A equipe avaliou então a mobilidade e as respostas táteis dos animais e examinou seus cérebros em busca de regiões de tecido necrosado e dano estrutural nos neurônios. Ratos que receberam ciprofol apresentaram áreas de lesão cerebral menores, neurônios com aspecto mais saudável e melhores escores de movimento e sensibilidade do que os animais não tratados, sugerindo que o fármaco atenuou as consequências mais graves do insulto.
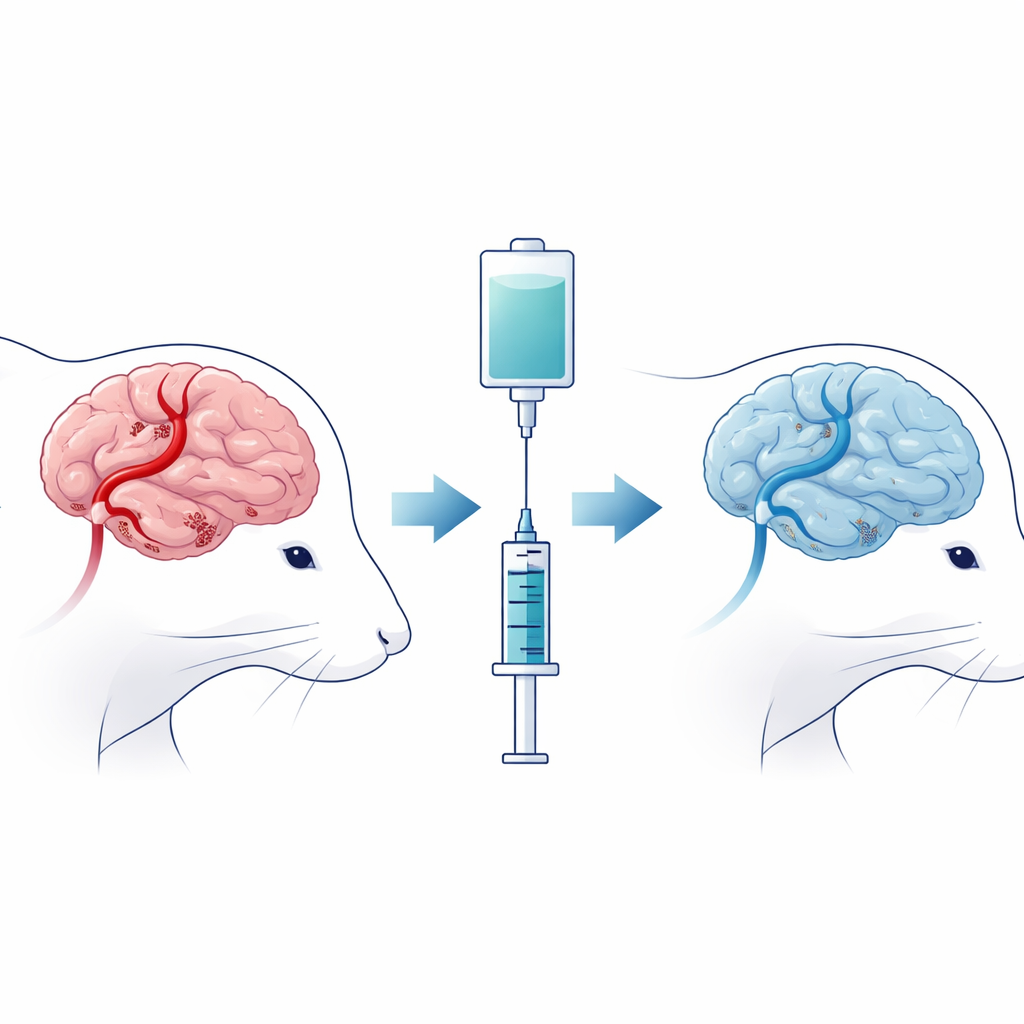
Uma forma oculta de morte celular impulsionada pelo ferro
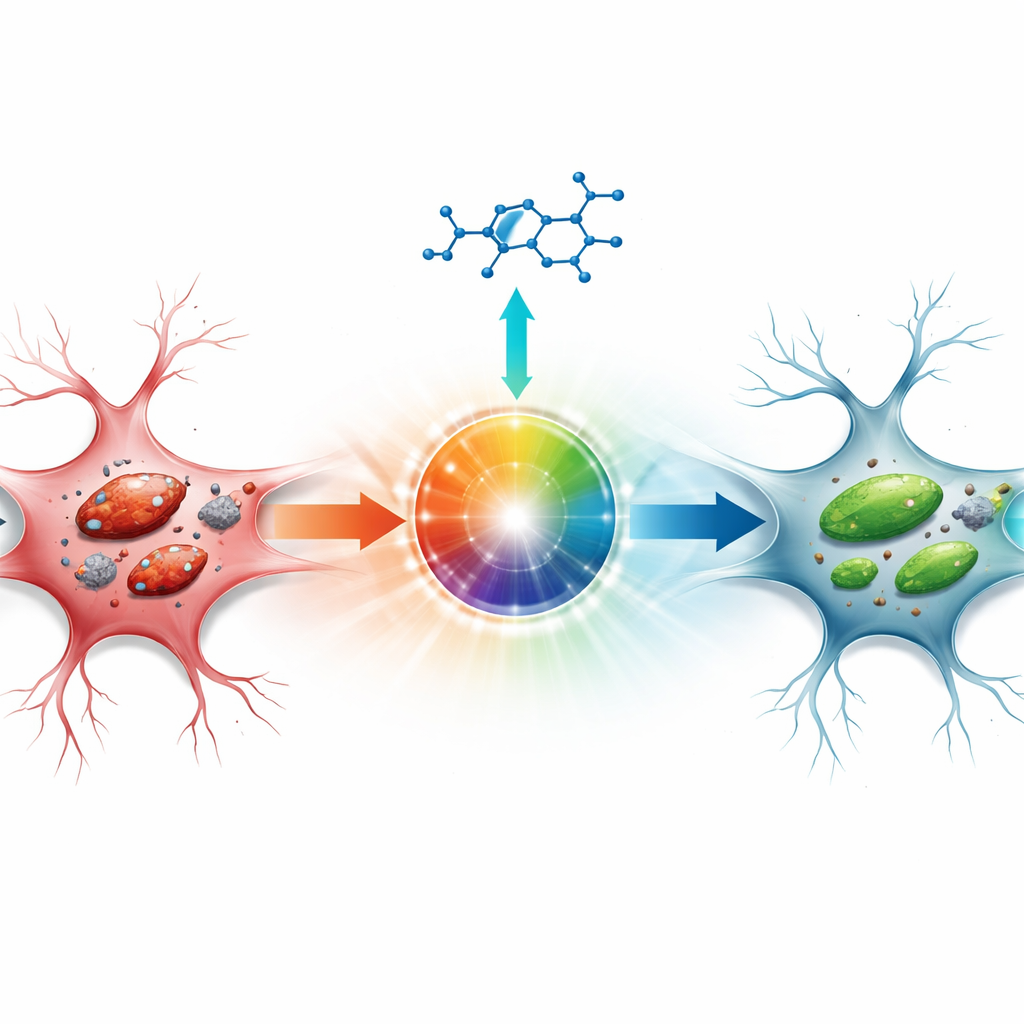
Além do dano tecidual visível, os autores focaram em um tipo de morte celular recentemente reconhecido chamado ferroptose, que é alimentado pelo ferro e por reações químicas desenfreadas que atacam os componentes lipídicos das membranas celulares. Nos ratos do modelo de AVC sem tratamento, o tecido cerebral da região vulnerável ao redor do núcleo da lesão continha mais ferro, níveis elevados de um subproduto lipídico de dano e mitocôndrias neuronais com aparência inchada e estruturalmente danificada ao microscópio eletrônico. Testes moleculares mostraram que proteínas protetoras que normalmente detoxificam subprodutos lipídicos nocivos estavam reduzidas, enquanto proteínas que promovem esse processo destrutivo estavam aumentadas. O ciprofol reverteu em grande parte essas alterações: ferro e dano lipídico diminuíram, o equilíbrio das proteínas-chave deslocou-se em direção à proteção e as mitocôndrias mantiveram formas e estruturas internas mais normais.
Um sensor de energia celular como interruptor de controle
O estudo investigou então como o ciprofol produz esses efeitos protetores. A atenção concentrou-se na AMPK, uma proteína que atua como sensor de energia celular e respondedor ao estresse. Nos cérebros lesionados dos ratos não tratados, a atividade da AMPK estava deprimida. O ciprofol aumentou a forma ativada da AMPK, em paralelo com as reduções no dano relacionado à ferroptose. Para testar se esse sensor de energia realmente fica a montante da cadeia de eventos protetores, os pesquisadores usaram outro fármaco, o Compósito C, que bloqueia a AMPK. Quando os animais receberam tanto ciprofol quanto esse bloqueador da AMPK, os benefícios do ciprofol foram parcialmente perdidos: marcadores relacionados à ferroptose retornaram gradualmente a níveis prejudiciais, o acúmulo de ferro reapareceu e o sinal de atividade da AMPK caiu ainda mais do que nos animais com AVC não tratados. Esse padrão apoia a ideia de que ativar a AMPK é um passo-chave no modo como o ciprofol protege as células cerebrais.
Reduzindo a tempestade inflamatória do cérebro
O dano relacionado ao AVC não é apenas uma questão de morte celular dentro dos neurônios; a resposta imune cerebral também desempenha papel importante. A equipe mediu várias moléculas mensageiras inflamatórias que tipicamente disparam após isquemia–reperfusão. Nos animais não tratados, esses sinais estavam fortemente elevados, refletindo uma reação inflamatória intensa. O ciprofol reduziu os três principais marcadores inflamatórios medidos, sugerindo que ele não apenas suprime o dano de membrana conduzido pelo ferro, mas também mitiga a tempestade inflamatória subsequente. Quando a AMPK foi bloqueada com o Compósito C, esses efeitos calmantes sobre a inflamação foram enfraquecidos, novamente ligando os benefícios do ciprofol a essa via central de detecção de energia.
O que isso pode significar para cuidados futuros
Em conjunto, os resultados apontam para o ciprofol como mais do que um sedativo: neste modelo em ratos, ele parece limitar o dano cerebral relacionado ao AVC ao ativar a AMPK, que por sua vez reprime a morte celular impulsionada pelo ferro e atenua a inflamação. Como o ciprofol já vem sendo usado em clínicas para anestesia e sedação de procedimentos, seu potencial adicional como agente protetor do cérebro é especialmente interessante. Ainda assim, o trabalho tem limitações importantes, incluindo a dependência de um único modelo animal e a possibilidade de que o fármaco bloqueador da AMPK tenha efeitos colaterais próprios. Serão necessários mais estudos, incluindo em outras espécies e, por fim, em pacientes humanos, para confirmar se o ciprofol pode proteger o cérebro de forma segura durante e após o tratamento do AVC.
Citação: Zeng, H., Yu, X., Zheng, Z. et al. Ciprofol attenuates cerebral Ischemia‒reperfusion injury in rats by inhibiting ferroptosis through upregulating AMPK. Sci Rep 16, 9282 (2026). https://doi.org/10.1038/s41598-026-40104-6
Palavras-chave: acidente vascular isquêmico, lesão por reperfusão, ciprofol, ferroptose, neuroproteção