Clear Sky Science · pt
Dinâmica da actina mediada por caldesmon‑1 é essencial para a diferenciação osteogênica das células intersticiais da válvula aórtica
Por que o endurecimento das válvulas cardíacas importa
Com o envelhecimento, uma das principais portas do coração — a válvula aórtica — pode gradualmente ficar rígida e praticamente pedra. Essa condição, chamada estenose aórtica, obriga o coração a bombear com mais esforço e pode levar à insuficiência cardíaca. Hoje, os únicos tratamentos confiáveis são a substituição cirúrgica ou por cateter da válvula. O estudo resumido aqui faz uma pergunta básica, porém crucial: o que faz o tecido suave e flexível da válvula se transformar gradualmente em material semelhante ao ósseo? Ao descobrir um jogador molecular chave nesse processo, a pesquisa aponta para futuros medicamentos que possam retardar ou até prevenir a calcificação valvar, em vez de simplesmente substituir a válvula danificada.
Um olhar mais atento aos trabalhadores ocultos da válvula
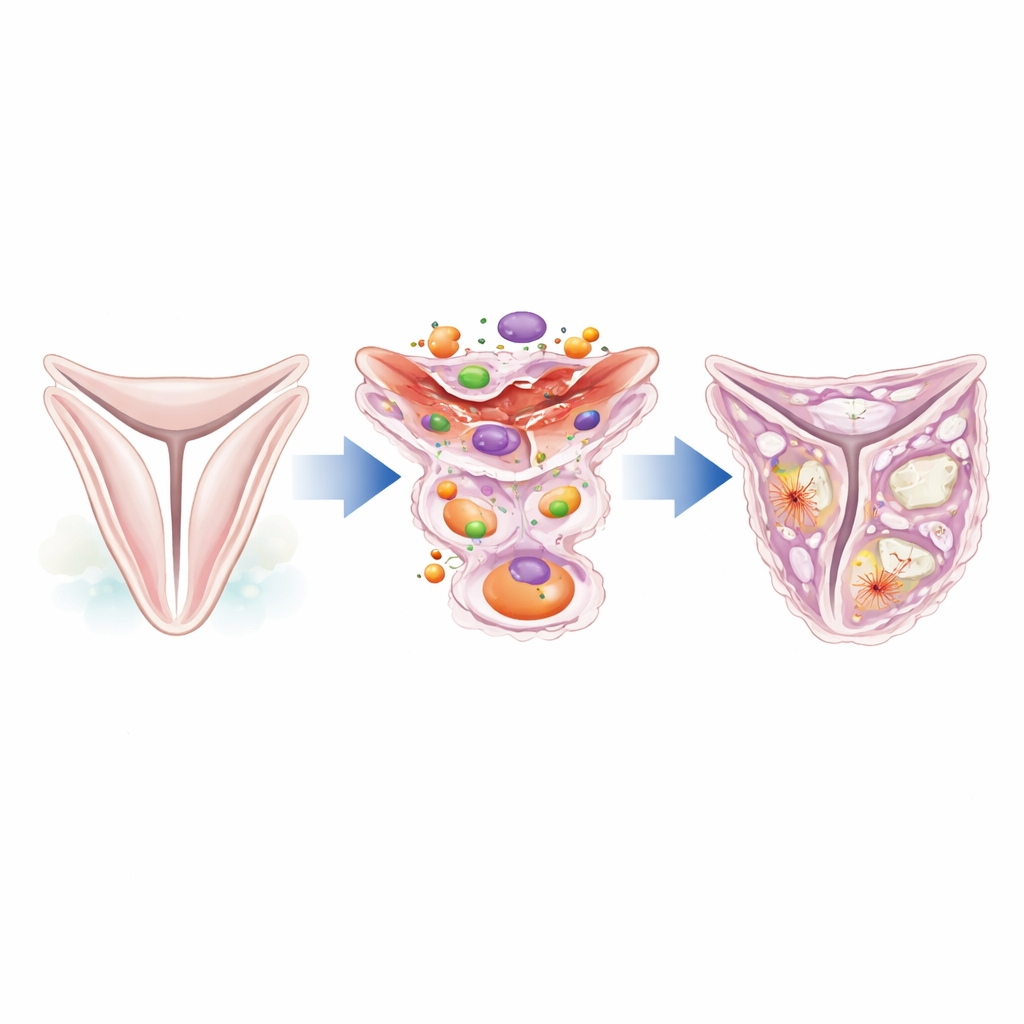
As cúspides da válvula aórtica são sustentadas por uma camada fina de células de suporte especializadas conhecidas como células intersticiais da válvula. Em uma válvula saudável, essas células permanecem discretas e ajudam a manter a estrutura do tecido. Sob estresse ou lesão, entretanto, elas podem mudar de identidade e começar a comportar‑se como células formadoras de cicatriz ou até de osso. Os autores focaram em uma proteína chamada caldesmon‑1, que ajuda a controlar o andaime interno das células formado por filamentos de actina. Ao explorar dados existentes de RNA de célula única de válvulas humanas, eles descobriram que a caldesmon‑1 está fortemente aumentada em válvulas de pacientes com estenose aórtica em comparação com válvulas normais, particularmente em células intersticiais encontradas em regiões espessas e fibróticas.
Do tecido flexível a áreas fibróticas e semelhantes a osso
Estudos ao microscópio de amostras humanas de válvula revelaram que a proteína caldesmon‑1 é abundante em cúspides doentes e se alinha com marcadores de células ativadas e contráteis e de células do tipo fibroblasto que produzem colágeno. Essas células ricas em caldesmon‑1 se agrupam em torno de áreas de fibrose e calcificação inicial, sugerindo que ajudam a construir a matriz extra que espessa a válvula. Análises adicionais mostraram que essas células expressam genes típicos de tipos celulares semelhantes a músculo liso e propensos a formar osso, e são grandes produtoras de proteínas estruturais como o colágeno tipo I. Em outras palavras, onde quer que a válvula esteja endurecendo e formando cicatriz, células intersticiais positivas para caldesmon‑1 estão presentes.
Como uma proteína que controla forma empurra as células rumo ao osso
Para entender causa e efeito, a equipe isolou células intersticiais de válvulas humanas e usou RNA interferente para reduzir a caldesmon‑1. Sem essa proteína, as células perderam sua forma alongada e em esp spindle e ficaram mais arredondadas. Seus filamentos internos de actina afinaram, e a capacidade de proliferar e migrar de forma dirigida diminuiu. Quando os pesquisadores expuseram essas células a um meio de cultura osteogênico, ou estimulador de formação óssea, células normais formaram depósitos de cálcio com facilidade, mas células com caldesmon‑1 reduzida mostraram muito menos acúmulo mineral. Sequenciamento em grande escala de RNA confirmou que muitos genes envolvidos na formação óssea e no remodelamento tecidual, incluindo motores osteogênicos bem conhecidos como RUNX2 e fosfatase alcalina, foram fortemente ativados em condições osteogênicas, mas não aumentaram quando a caldesmon‑1 foi silenciada.
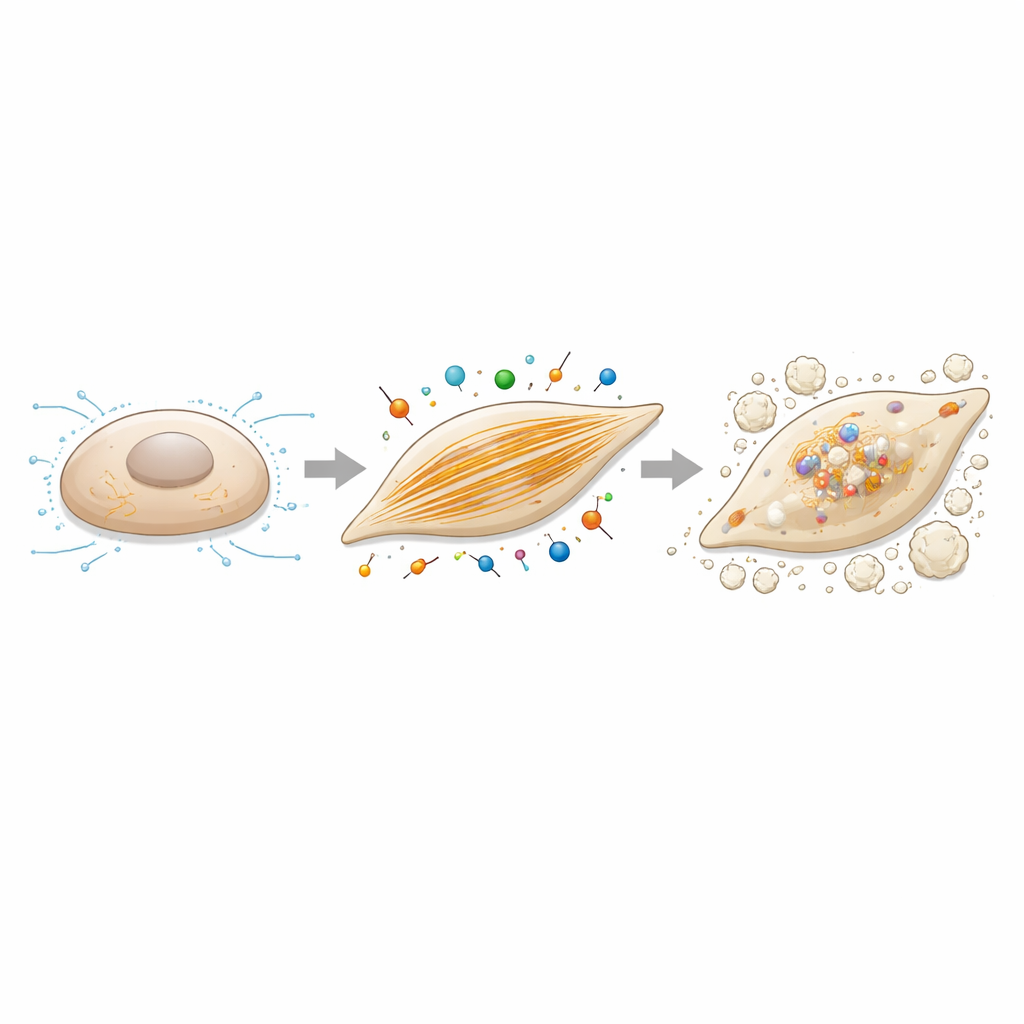
Filamentos de actina como alavanca de controle para a calcificação
Como a caldesmon‑1 é um regulador da actina, os autores perguntaram em seguida se alterar a montagem da actina em si mudaria a tendência das células de calcificar. Eles trataram as células intersticiais da válvula com citocalasina B, um composto que perturba suavemente o crescimento dos filamentos de actina, enquanto aplicavam as mesmas condições de cultura promotoras de osso. Em doses que não prejudicaram seriamente a sobrevivência celular, esse tratamento reduziu drasticamente a deposição de cálcio e baixou a expressão de genes relacionados à ossificação, incluindo caldesmon‑1 e RUNX2. Juntamente com os experimentos de silenciamento, essas descobertas desenham um quadro coerente: redes robustas de filamentos de actina e as forças contráteis que elas sustentam não são meros coadjuvantes — elas impulsionam ativamente a mudança de células de suporte silenciosas para células formadoras de osso na válvula.
O que isso significa para tratamentos futuros
Para o leitor leigo, a mensagem principal é que o endurecimento da válvula aórtica é um processo ativo e regulado, e não simples "desgaste". Este estudo identifica a caldesmon‑1 como um coordenador central que liga o esqueleto interno da célula ao programa genético de produção de tecido semelhante ao ósseo. Ao ajudar as células intersticiais da válvula a adotarem uma identidade contrátil, fibrótica e, por fim, osteogênica, a caldesmon‑1 contribui diretamente para o acúmulo de depósitos duros que estreitam a válvula. Embora qualquer terapia direcionada a essa proteína ou à dinâmica da actina exija testes cuidadosos para evitar efeitos indesejados em outros tecidos, as vias mediadas pela caldesmon‑1 emergem agora como candidatas promissoras para medicamentos projetados para retardar ou interromper a calcificação valvar antes que a cirurgia se torne necessária.
Citação: Komoda, M., Sakaue, T., Nakao, Y. et al. Caldesmon-1–mediated actin dynamics is essential for osteogenic differentiation of aortic valve interstitial cells. Sci Rep 16, 9385 (2026). https://doi.org/10.1038/s41598-026-39938-x
Palavras-chave: calcificação da válvula aórtica, caldesmon‑1, células intersticiais da válvula, citoesqueleto de actina, diferenciação osteogênica