Clear Sky Science · pt
RBP4 interfere na progressão do carcinoma de células escamosas da língua ao inibir a via de sinalização PI3K/AKT e promover a polarização de macrófagos para o tipo M1
Por que o câncer de língua precisa de novas ideias
O câncer de língua pode privar as pessoas da capacidade de falar, se alimentar e sentir gosto; mesmo com cirurgia, quimioterapia e radiação, a sobrevida a longo prazo frequentemente segue decepcionante. Este estudo investiga um ajudante inesperado no nosso sangue, uma proteína transportadora de vitamina A chamada RBP4, e mostra como ela pode tanto retardar o crescimento de tumores de língua quanto mobilizar os próprios defensores imunes do organismo. Ao revelar como essa molécula age dentro das células cancerosas e nas células imunes ao redor, a pesquisa aponta para estratégias novas que podem um dia tornar os tratamentos mais eficazes e menos lesivos.
Uma proteína oculta nos tumores da língua
Os pesquisadores começaram vasculhando grandes bancos de dados genômicos de câncer para ver quais genes relacionados ao sistema imune poderiam predizer o desfecho de pacientes com carcinoma de células escamosas da língua ao longo do tempo. Entre centenas de candidatos, RBP4, uma proteína mais conhecida por transportar vitamina A na corrente sanguínea, destacou-se como especialmente interessante. Quando a equipe comparou amostras tumorais com tecido saudável adjacente da língua, encontrou níveis de RBP4 consistentemente muito mais baixos no câncer. Esse padrão foi confirmado em vários conjuntos de dados independentes e em amostras de tecido de 20 pacientes, sugerindo que a perda de RBP4 é uma característica comum dessa doença.
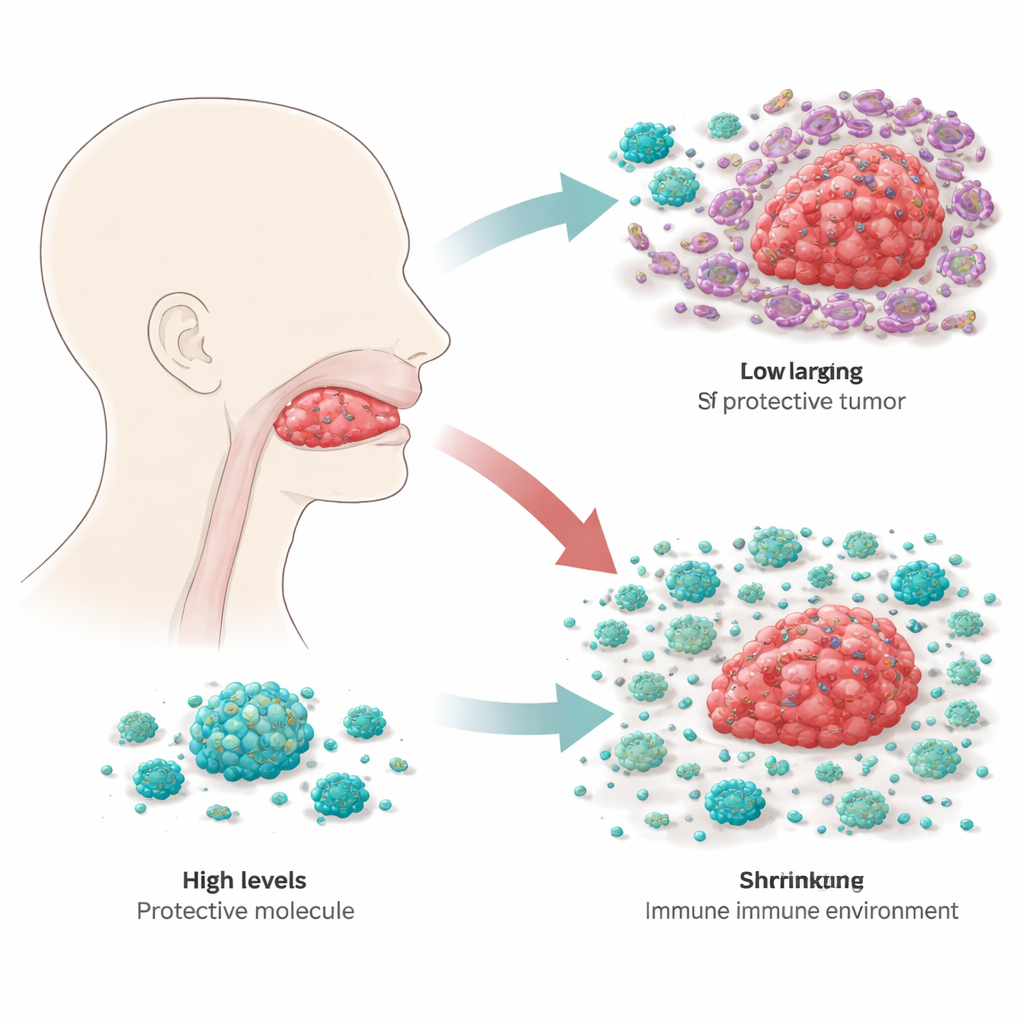
Retardando o crescimento tumoral de dentro
Para descobrir o que RBP4 realmente faz nas células do câncer de língua, os cientistas modificaram linhagens tumorais para produzir RBP4 em excesso ou para diminuir fortemente sua expressão. Em cultura, células com níveis mais altos de RBP4 cresceram mais devagar, enquanto aquelas com RBP4 reduzido se multiplicaram mais rápido e foram melhores em migrar e invadir membranas artificiais, comportamentos ligados à disseminação e recidiva. Quando essas células modificadas foram implantadas em camundongos, tumores com RBP4 extra permaneceram menores, ao passo que tumores com RBP4 reduzido cresceram de forma mais agressiva. Ao acompanhar interruptores-chave do controle de crescimento dentro das células, a equipe mostrou que RBP4 atenua uma via de crescimento principal conhecida como PI3K–AKT–mTOR, da qual muitos cânceres dependem como um pedal do acelerador interno. Com RBP4 elevado, essa via fica mais silenciosa e as células tumorais têm menos capacidade de assumir o estado flexível e móvel que favorece a migração.
Transformando células imunes em combatentes do tumor
O câncer não cresce isoladamente; ele vive dentro de um bairro de células imunes, vasos sanguíneos e células de suporte chamado microambiente tumoral. Nesse contexto, os macrófagos — grandes células imunes que podem tanto atacar quanto auxiliar tumores — desempenham papel central. Os investigadores observaram que tumores com mais RBP4 também tendiam a conter mais macrófagos do tipo “M1”, associados à inflamação e à destruição tumoral, em vez do tipo “M2”, que frequentemente apoia o crescimento tumoral. Em cultura celular, quando macrófagos foram expostos a RBP4 purificada ou a células de câncer de língua modificadas para secretar mais RBP4, eles migraram para esse estado M1, de combate ao tumor. Quando RBP4 foi reduzido nas células cancerosas, os macrófagos tenderam a assumir um perfil mais favorável ao tumor.
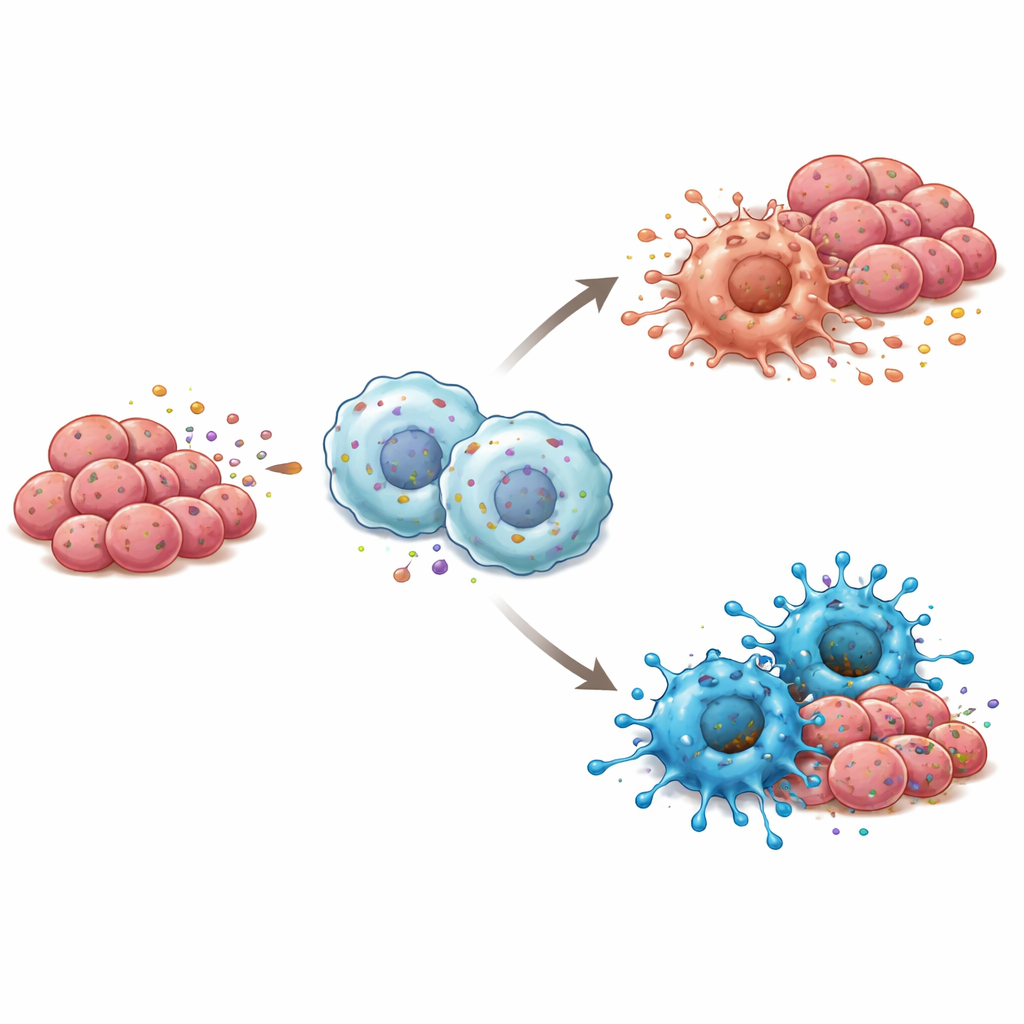
Vias de sinalização por trás da mudança imune
Para entender como RBP4 empurra os macrófagos para uma postura mais hostil ao tumor, os pesquisadores examinaram quais sistemas de alarme internos eram ativados nessas células imunes. Eles descobriram que RBP4 estimulava um sensor chamado TLR4 na superfície dos macrófagos e, por sua vez, ativava NF-κB, um interruptor mestre que dirige respostas inflamatórias. Bloquear TLR4 com um inibidor químico interrompeu essa reação em cadeia e impediu que os macrófagos adotassem o estado M1, mesmo na presença de RBP4. Em camundongos, tumores formados por células de câncer de língua ricas em RBP4 e misturadas com macrófagos cresceram mais lentamente e continham mais células do tipo M1, junto com maior atividade de TLR4 e NF-κB, reforçando a ideia de que essa via é fundamental para os efeitos imunes do RBP4.
O que isso pode significar para cuidados futuros
Em conjunto, o trabalho descreve RBP4 como um freio de dupla ação contra o câncer de língua: dentro das células tumorais, reduz um circuito de crescimento hiperativo, e na vizinhança tumoral, contribui para converter macrófagos em defensores mais vigilantes. Embora muitas questões permaneçam — como exatamente RBP4 interage com seus alvos e qual a melhor forma de aumentá-lo com segurança — o estudo sugere que restaurar ou mimetizar as ações de RBP4 poderia tanto retardar a expansão tumoral quanto fortalecer a pressão imune natural do organismo sobre o câncer. Para os pacientes, isso abre a perspectiva de terapias futuras que não apenas removam tumores, mas também reconfigurem sua fiação interna e o “ecossistema” local para impedir recidivas.
Citação: Yan, Y., Miao, N. & Wang, X. RBP4 interferes with tongue squamous cell carcinoma progression by inhibiting the PI3K/AKT signaling pathway and promoting macrophage M1-type polarization. Sci Rep 16, 9375 (2026). https://doi.org/10.1038/s41598-026-39915-4
Palavras-chave: câncer de língua, RBP4, microambiente tumoral, macrófagos, via PI3K AKT