Clear Sky Science · pt
Identificação multiômica de alvos-chave para a diferenciação osteogênica de células estromais mesenquimais da medula óssea humana sob estresse oxidativo
Por que ossos estressados importam
À medida que envelhecemos ou desenvolvemos doenças crônicas como diabetes e osteoporose, nossos ossos perdem a capacidade de se reparar. Um grande culpado é o “estresse oxidativo” — o acúmulo de moléculas reativas que danificam as células. Este estudo faz uma pergunta prática com importantes implicações para fraturas e implantes ósseos: o que exatamente dá errado dentro das células-tronco da medula óssea humana quando elas são expostas ao estresse oxidativo, e é possível encontrar um interruptor molecular que as ajude a continuar formando osso novo?
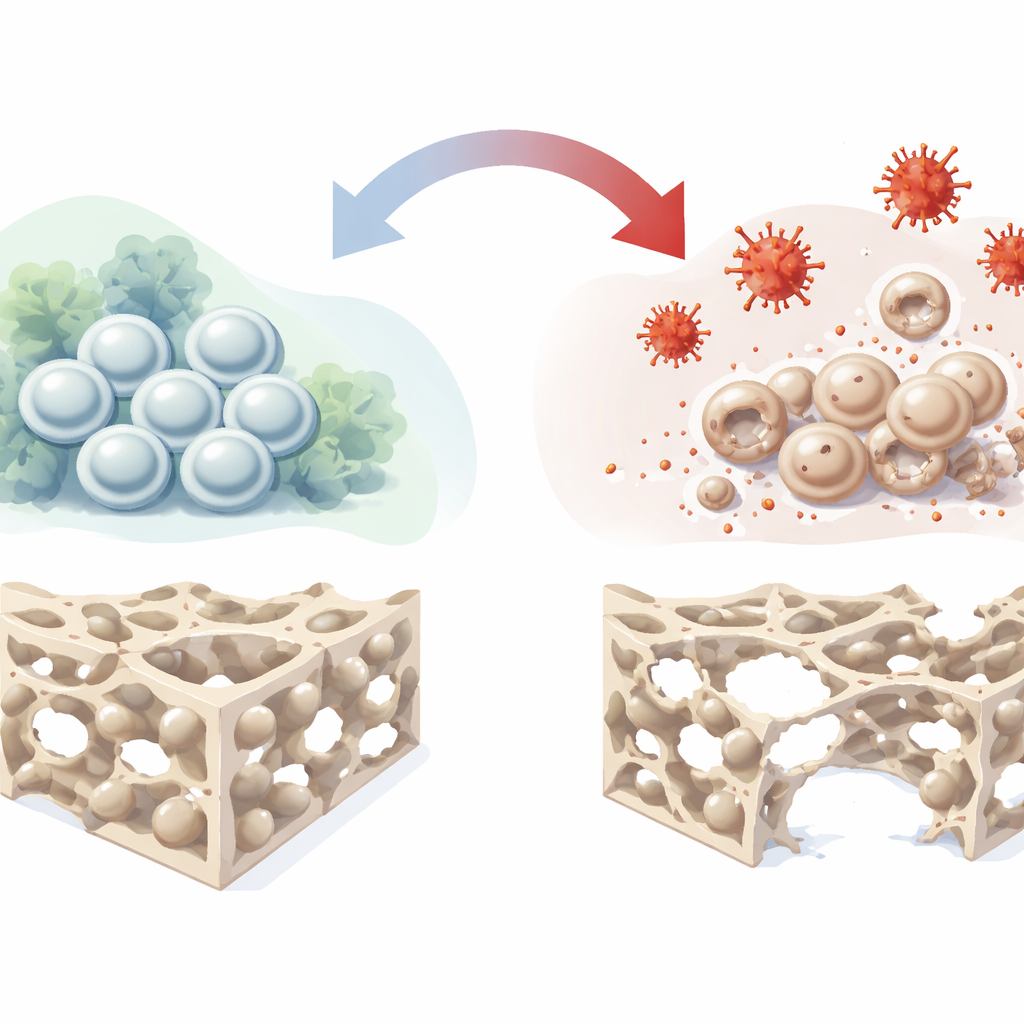
Células-tronco que constroem osso
Nas profundezas dos nossos ossos vivem células estromais mesenquimais da medula óssea, uma população versátil que pode se renovar e se maturar em células formadoras de osso, cartilagem e gordura. Como ajudam naturalmente a reparar tecido danificado, são candidatas principais para tratamentos de próxima geração para reparar defeitos ósseos e osteonecrose. Contudo, em pacientes reais essas células frequentemente estão em ambientes hostis marcados por fluxo sanguíneo ruim, baixo oxigênio, inflamação e estresse oxidativo. Nesses contextos, sua habilidade de se tornar células ósseas falha, limitando o sucesso de terapias baseadas em células-tronco. Os autores propuseram recriar esse ambiente hostil no laboratório e mapear, em detalhe, como ele atrapalha a formação óssea.
Recriando um ambiente adverso no laboratório
Os pesquisadores usaram peróxido de hidrogênio, uma fonte comum de espécies reativas de oxigênio, para impor estresse oxidativo a células-tronco da medula óssea humana cultivadas em laboratório. Eles titraram cuidadosamente a dose para encontrar um ponto em que as células ficassem estressadas, mas não fossem mortas. Em concentrações iguais ou inferiores a 400 micromolar, as células mantiveram sua morfologia alongada e permaneceram viáveis, embora sua química interna tenha mudado claramente: os níveis de espécies reativas aumentaram, a função mitocondrial começou a sofrer alterações e o equilíbrio entre proteínas relacionadas à sobrevivência e à morte inclinou-se para adaptação ao estresse. Em doses mais altas, as células perderam a forma e morreram em grande número. Usando a dose bem tolerada de 400 micromolar, a equipe então induziu as células a formar osso e observou o que aconteceu.
Como o estresse bloqueia a construção óssea
Sob estresse oxidativo, a capacidade das células-tronco de se tornar células ósseas diminuiu em vários testes complementares. A atividade óssea inicial, monitorada por uma enzima chamada fosfatase alcalina, caiu conforme o estresse aumentava. Mais tarde, quando as células deveriam depositar minerais, as placas de cultura mostraram menos e mais fracos nódulos de cálcio. Genes e proteínas-chave relacionados ao osso, como RUNX2 e osteopontina, também foram reduzidos. Para investigar em profundidade, os cientistas combinaram duas abordagens “ômicas” poderosas: sequenciamento de RNA para perfilar quais genes estavam mais ou menos ativos, e análise proteômica em grande escala para ver quais proteínas realmente mudaram em abundância. Em conjunto, esses conjuntos de dados revelaram centenas de mudanças no controle do ciclo celular, no comportamento dos cromossomos, no metabolismo e na organização do arcabouço extracelular, pintando o quadro de células-tronco cujo tempo interno e suporte estrutural são alterados pelo estresse oxidativo.
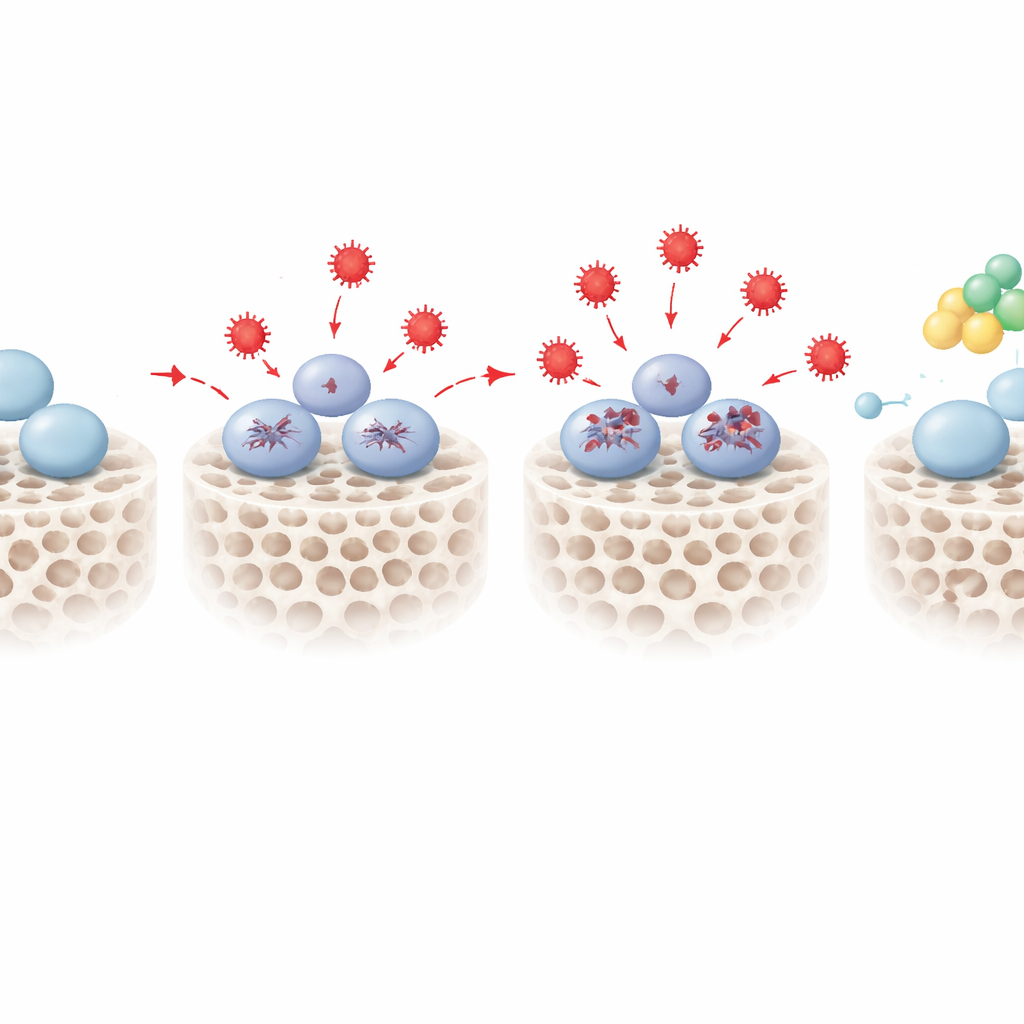
Encontrando um interruptor protetor chamado PENK
Ao sobrepor os mapas de RNA e proteína, a equipe concentrou-se em 18 moléculas que mudaram de forma consistente em células estressadas e estavam ligadas tanto às respostas ao estresse quanto à formação óssea. Uma se destacou: proencefalina, ou PENK, mais conhecida como precursora de peptídeos opioides naturais. Sob estresse oxidativo, os níveis de PENK aumentaram de maneira dependente da dose. Quando os cientistas reduziram artificialmente o PENK com ferramentas genéticas, as células-tronco estressadas pioraram ainda mais na formação óssea, exibindo atividade enzimática inicial mais fraca e menor deposição mineral. Quando elevaram o PENK, ocorreu o oposto: mesmo sob as mesmas condições oxidativas, as células recuperaram grande parte de sua capacidade de construir matriz óssea mineralizada. Análises adicionais de vias sugeriram que o PENK pode atuar ajustando certas rotas metabólicas, incluindo o metabolismo de esfingolipídios, que conectam o equilíbrio redox às decisões sobre manter o potencial da célula-tronco ou avançar para um destino ósseo.
O que isso significa para a reparação óssea futura
Este estudo demonstra que o estresse oxidativo por si só é suficiente para incapacitar a capacidade formadora de osso das células-tronco da medula óssea humana, e identifica o PENK como um fator protetor intrínseco que as ajuda a resistir a esse dano. Para não-especialistas, a mensagem é clara: o sucesso de terapias ósseas baseadas em células-tronco dependerá não apenas das próprias células, mas também dos ambientes estressantes em que são implantadas e dos interruptores moleculares que as ajudam a lidar com isso. Ao destacar o PENK como um alvo promissor, o trabalho aponta para futuros fármacos ou abordagens baseadas em genes que poderiam reforçar a reparação óssea em pacientes cujos tecidos estão imersos em estresse oxidativo, desde idosos até pessoas com doenças metabólicas ou inflamatórias crônicas.
Citação: Dong, W., Zheng, Y., Zhou, Y. et al. Multi-omics identification of key targets for the osteogenic differentiation of human bone marrow mesenchymal stromal cells under oxidative stress. Sci Rep 16, 8215 (2026). https://doi.org/10.1038/s41598-026-39818-4
Palavras-chave: regeneração óssea, estresse oxidativo, células-tronco mesenquimais, diferenciação osteogênica, PENK