Clear Sky Science · pt
Impacto da oxidação do RNA G-quádruplex em sua dinâmica conformacional e interação com a TDP-43 associada à ELA
Por que isso importa para a saúde dos nervos
A esclerose lateral amiotrófica (ELA) é uma doença fatal na qual as células nervosas que controlam o movimento morrem lentamente, mas as causas fundamentais desse dano seletivo permanecem misteriosas. Este estudo faz uma pergunta simples, porém importante: à medida que envelhecemos e nossas células sofrem mais danos químicos “tipo ferrugem”, esse desgaste no RNA — a cópia funcional de nossos genes — interrompe sinais vitais que mantêm os neurônios motores vivos? Ao focalizar uma forma especial dobrada do RNA e uma proteína-chave ligada à ELA chamada TDP-43, o trabalho revela como pequenas cicatrizes químicas podem contribuir para criar o terreno favorável à doença. 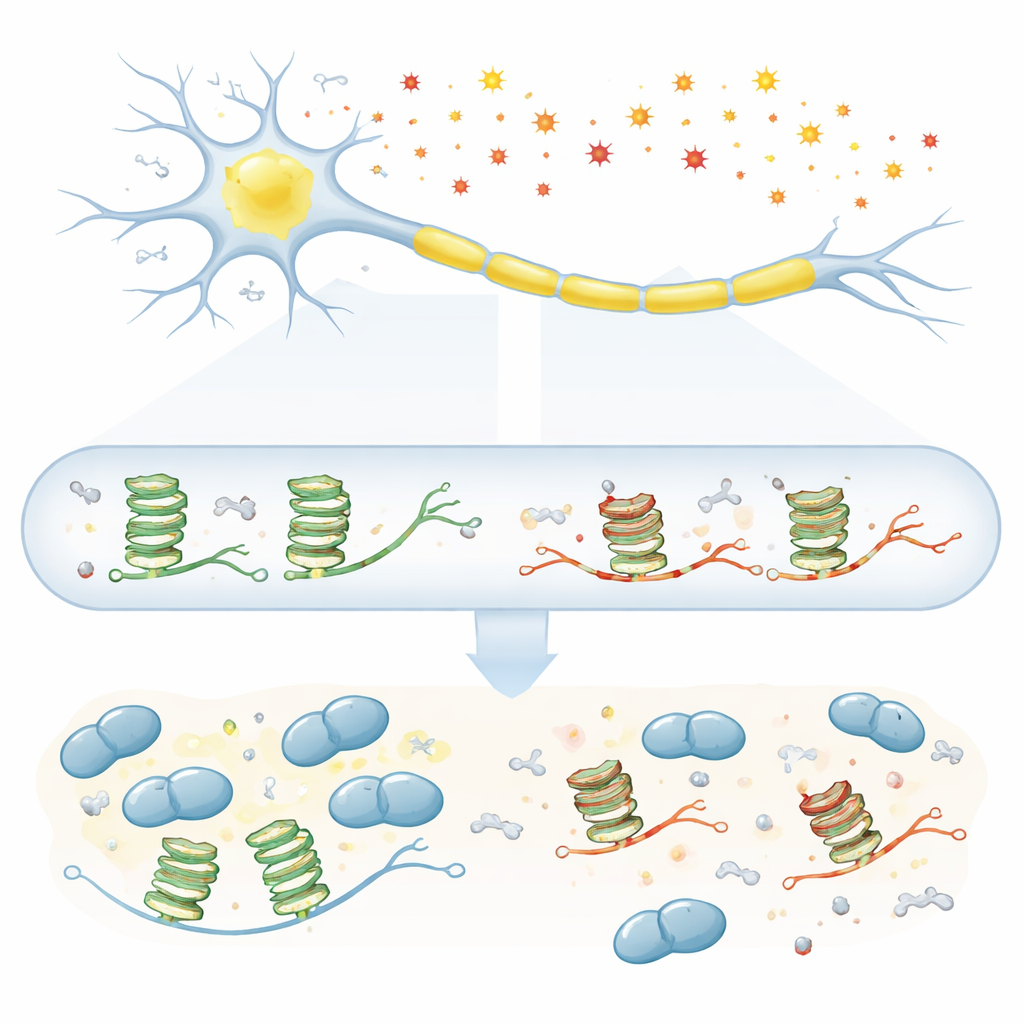
Um nó de RNA frágil no coração dos neurônios motores
Os neurônios motores dependem do transporte de longa distância de mensagens de RNA ao longo de seus axônios para que proteínas possam ser produzidas localmente, perto das conexões com o músculo. Muitas dessas mensagens carregam um “nó” estrutural especial chamado G-quádruplex, formado por trechos ricos na base guanina. Proteínas como a TDP-43 reconhecem esse nó e prendem o RNA em grânulos de transporte que se movem ao longo do axônio. O problema é que a guanina também é a base mais suscetível à oxidação quando as células estão sob estresse por espécies reativas de oxigênio, que se acumulam com o envelhecimento. Indícios anteriores sugeriam que G-quádruplexes e TDP-43 são centrais na ELA, mas não estava claro exatamente como a oxidação desses nós de RNA poderia atrapalhar essa parceria.
Observando o estresse oxidativo deformar formas de RNA
O pesquisador primeiro expôs células humanas de neuroblastoma ao peróxido de hidrogênio, um agente oxidante comum, e então examinou o estado das estruturas de G-quádruplex. Sinais de uma sonda sensível a G-quádruplexes caíram conforme o estresse oxidativo aumentou, indicando que esses nós compactos de RNA estavam perdendo sua forma normal. Para especificar a química envolvida, a equipe então construiu RNAs sintéticos que formam G-quádruplexes e deliberadamente incorporou quantidades variadas de 8-oxoguanina, uma forma oxidada bem conhecida de guanina encontrada em neurônios envelhecidos e em tecido de ELA. Usando um conjunto de ferramentas biofísicas, mostraram que mesmo níveis modestos dessa modificação afrouxam o empilhamento ordenado do G-quádruplex, embora o desfecho exato dependa da sequência de RNA ao redor. 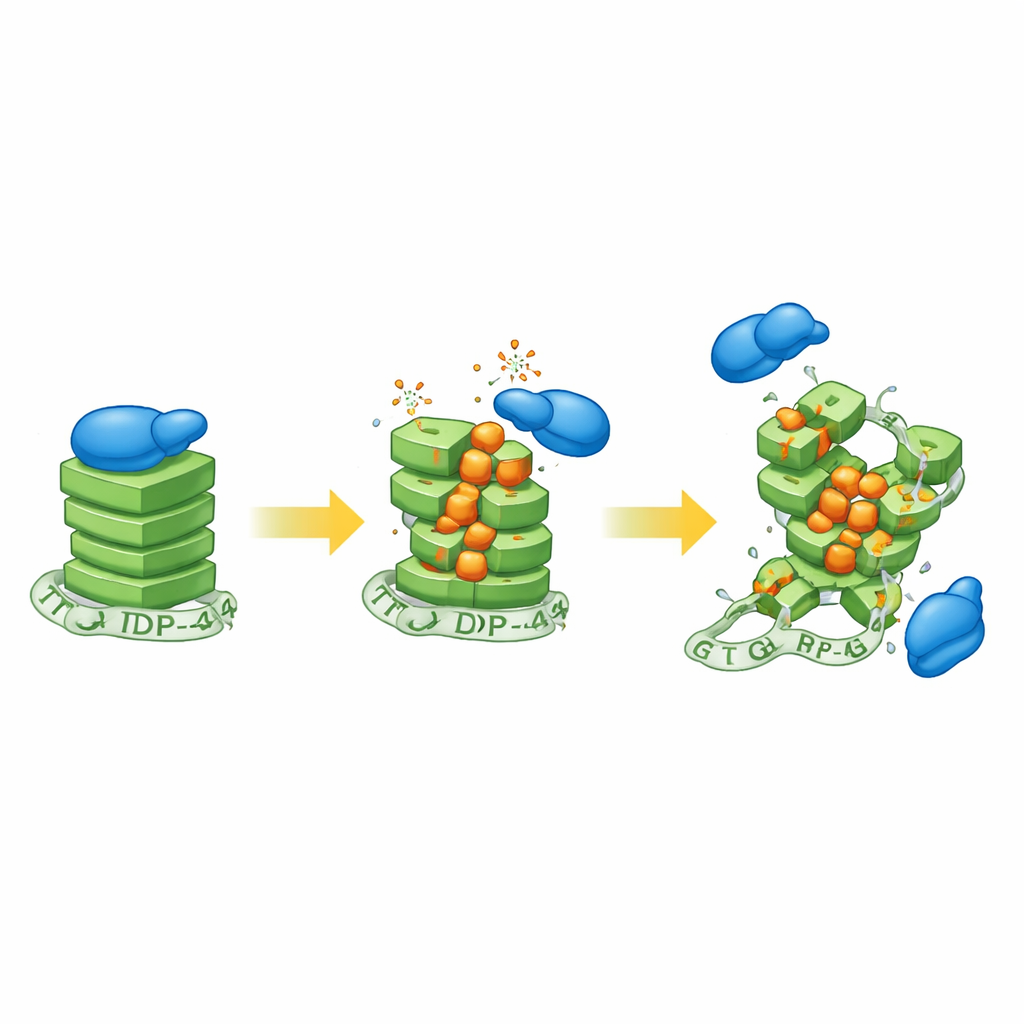
Novas falhas: bases desencontradas e fitas mal emparelhadas
Análises mais detalhadas revelaram dois tipos distintos de problema estrutural. Em um G-quádruplex derivado da mensagem PSD-95, guaninas oxidadas tenderam a emparelhar inadequadamente com adeninas próximas, formando “desencontros” que distorcem sutilmente a dobra. Esses desencontros surgiram mais prontamente em níveis intermediários de oxidação, quando o RNA ainda podia montar-se transitoriamente em um G-quádruplex que colocava os parceiros errados em contato. Em outro G-quádruplex da mensagem CaMKIIα, oxidação intensa desestabilizou tão fortemente o nó intramolecular habitual que as guaninas restantes intactas buscaram parceiros em outras fitas de RNA, promovendo G-quádruplexes intermoleculares anormais. Estruturas assim mal conectadas poderiam emaranhar diferentes RNAs e interferir com o tráfego normal de RNA dentro dos neurônios.
Quando o RNA danificado perde seu parceiro proteico
O estudo então investigou como esses nós distorcidos interagem com a TDP-43. Usando ensaios de ligação baseados em gel, o pesquisador mostrou que a TDP-43 prefere fortemente G-quádruplexes intactos e paralelos e falha progressivamente em se ligar à medida que mais bases oxidadas são introduzidas. A estrutura de CaMKIIα, já fortemente compactada, mostrou-se especialmente sensível: mesmo baixa oxidação quase aboliu a ligação à TDP-43. Uma segunda proteína, FUS — também associada à ELA — apresentou perda de afinidade semelhante, embora ligeiramente menos severa, sugerindo que a oxidação enfraquece de modo geral a aderência das proteínas que se ligam a G-quádruplexes. Curiosamente, quando a TDP-43 foi misturada com RNA levemente oxidado, as evidências apontaram para a proteína envolvendo uma forma intermediária instável do G-quádruplex em vez de um nó totalmente dobrado, sugerindo uma luta dinâmica entre estabilização e degradação.
Vulnerabilidade extra em proteínas mutantes ligadas à ELA
O trabalho examinou ainda dez variantes de TDP-43 encontradas em pacientes com ELA, a maioria com alterações em uma cauda flexível rica em glicina que ajusta o reconhecimento de RNA. Todas essas mutantes já se ligavam a G-quádruplexes normais de forma mais fraca do que a proteína selvagem. Quando G-quádruplexes de RNA oxidados foram introduzidos como competidores, as mutantes mostraram ainda menos capacidade do que a proteína normal de reconhecer e ligar as estruturas danificadas. Algumas variantes localizadas em regiões particularmente propensas à desordem foram as mais afetadas. Isso sugere um golpe duplo em indivíduos envelhecendo que carregam tais mutações: não apenas sua TDP-43 é intrinsecamente menos eficaz, como a oxidação relacionada à idade ainda degrada sua capacidade de escoltar mensagens cruciais ao longo dos axônios dos neurônios motores.
O que isso significa para a compreensão da ELA
Em termos simples, este estudo mostra que o dano químico impulsionado pela idade remodela nós delicados de RNA que guiam o transporte de mensagens nos neurônios motores, e esses nós deformados deixam de cooperar bem com a TDP-43 ou proteínas relacionadas. O resultado é maior probabilidade de cargas de RNA mal direcionadas ou paradas, justamente nos axônios longos e vulneráveis que controlam os músculos. Para pessoas que também herdam mutações em TDP-43, esse enfraquecimento das interações RNA–proteína induzido pela oxidação pode empurrar neurônios já estressados mais perto do colapso. Ao iluminar essa cadeia sutil, porém potente, de eventos — do estresse oxidativo à alteração da arquitetura do RNA até o transporte prejudicado — o trabalho destaca a oxidação do RNA G-quádruplex como um elo molecular promissor entre o envelhecimento e a ELA, e como um alvo potencial para futuras terapias protetoras.
Citação: Ishiguro, A. Impact of G-quadruplex RNA oxidation on its conformational dynamics and interaction with ALS-associated TDP-43. Sci Rep 16, 8802 (2026). https://doi.org/10.1038/s41598-026-39767-y
Palavras-chave: esclerose lateral amiotrófica, oxidação de RNA, G-quádruplex, TDP-43, degeneração de neurônio motor