Clear Sky Science · pt
Identificação de biomarcadores relacionados a lesão da barreira hematoencefálica em infarto cerebral por meio de análise transcriptômica
Por que isso importa para AVC e saúde cerebral
Quando alguém sofre um AVC causado por um vaso sanguíneo bloqueado no cérebro, os médicos conseguem ver o dano em exames de imagem, mas ainda têm dificuldade em prever quem terá inchaço agravado, hemorragia ou deficiência a longo prazo. Grande parte desse dano ocorre no guardião protetor do cérebro, a barreira hematoencefálica, que normalmente impede que substâncias nocivas do sangue vazem para o tecido nervoso frágil. Este estudo fez uma pergunta simples, porém importante: existem sinais moleculares claros que revelem quando essa barreira está se rompendo e esses sinais poderiam, no futuro, orientar melhor o diagnóstico e o tratamento de pacientes com AVC?
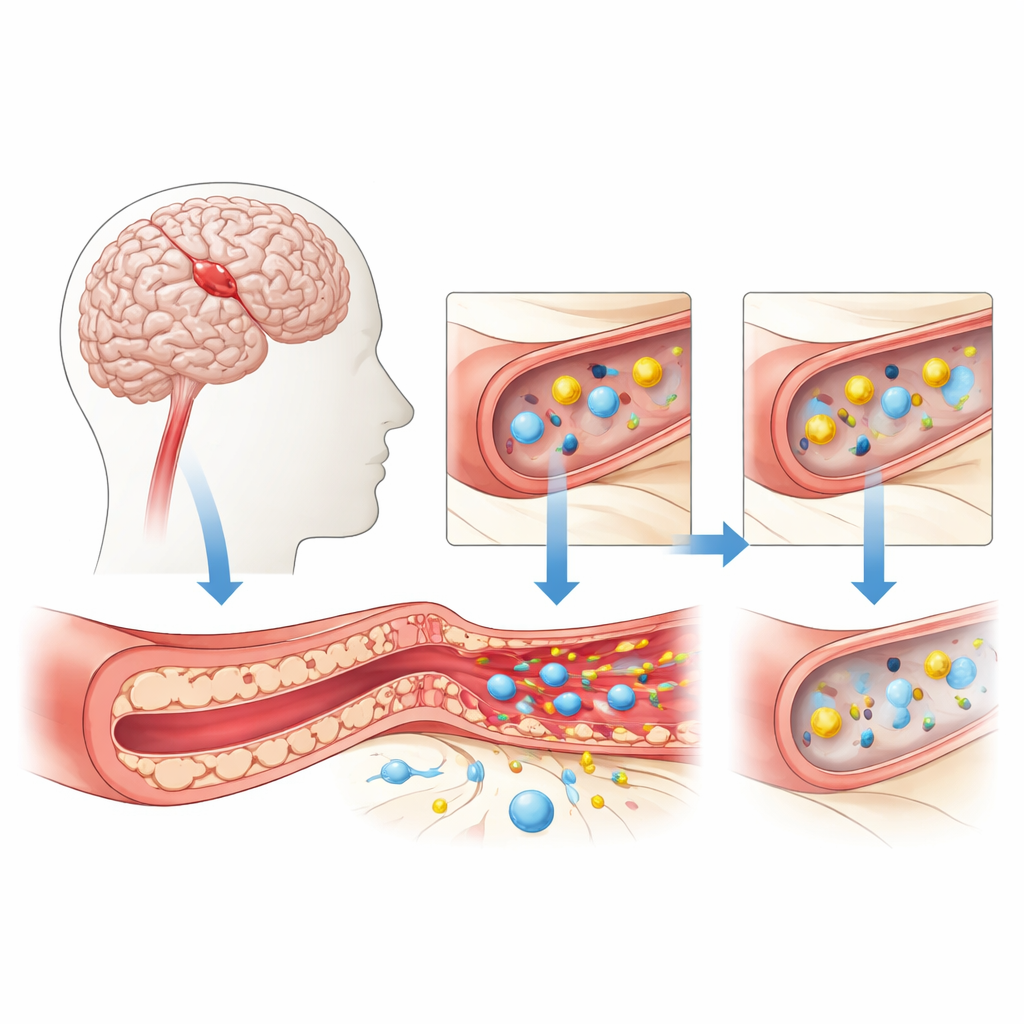
O portão protetor do cérebro sob estresse
A barreira hematoencefálica é formada por células bem unidas que revestem os minúsculos vasos sanguíneos do cérebro. Essas células controlam cuidadosamente o que pode passar do sangue para o cérebro, permitindo nutrientes vitais como oxigênio e glicose e bloqueando toxinas e células imunes que poderiam causar dano. Durante um infarto cerebral, ou AVC isquêmico, o fluxo sanguíneo cai subitamente. Sem oxigênio e glicose suficientes, essas células que revestem os vasos ficam estressadas e começam a perder seu selo apertado. Aberturas surgem entre elas, fluido infiltra o tecido ao redor e mensageiros químicos da inflamação invadem a área, tudo o que pode piorar o inchaço e a lesão cerebral.
Recriando o dano do AVC no laboratório
Para investigar o que acontece dentro dessas células da barreira, os pesquisadores usaram uma linha celular humana bem caracterizada que imita o revestimento dos vasos cerebrais. Eles expuseram essas células a um ambiente de baixo oxigênio e sem glicose — chamado privação de oxigênio e glicose — para imitar as condições de um AVC, e então restauraram as condições normais para simular o tratamento e a recuperação. Mediram a sobrevivência celular, a liberação de uma enzima indicadora de dano celular e a quantidade de moléculas inflamatórias liberadas. Como esperado, o tratamento estressante reduziu a saúde celular, aumentou sinais inflamatórios como IL-1β, IL-6 e TNF-α, e elevou o vazamento de um marcador de dano chamado LDH. Quando oxigênio e nutrientes foram restaurados, muitas dessas mudanças nocivas diminuíram e as células recuperaram parte da capacidade de formar estruturas semelhantes a vasos em um teste de crescimento.
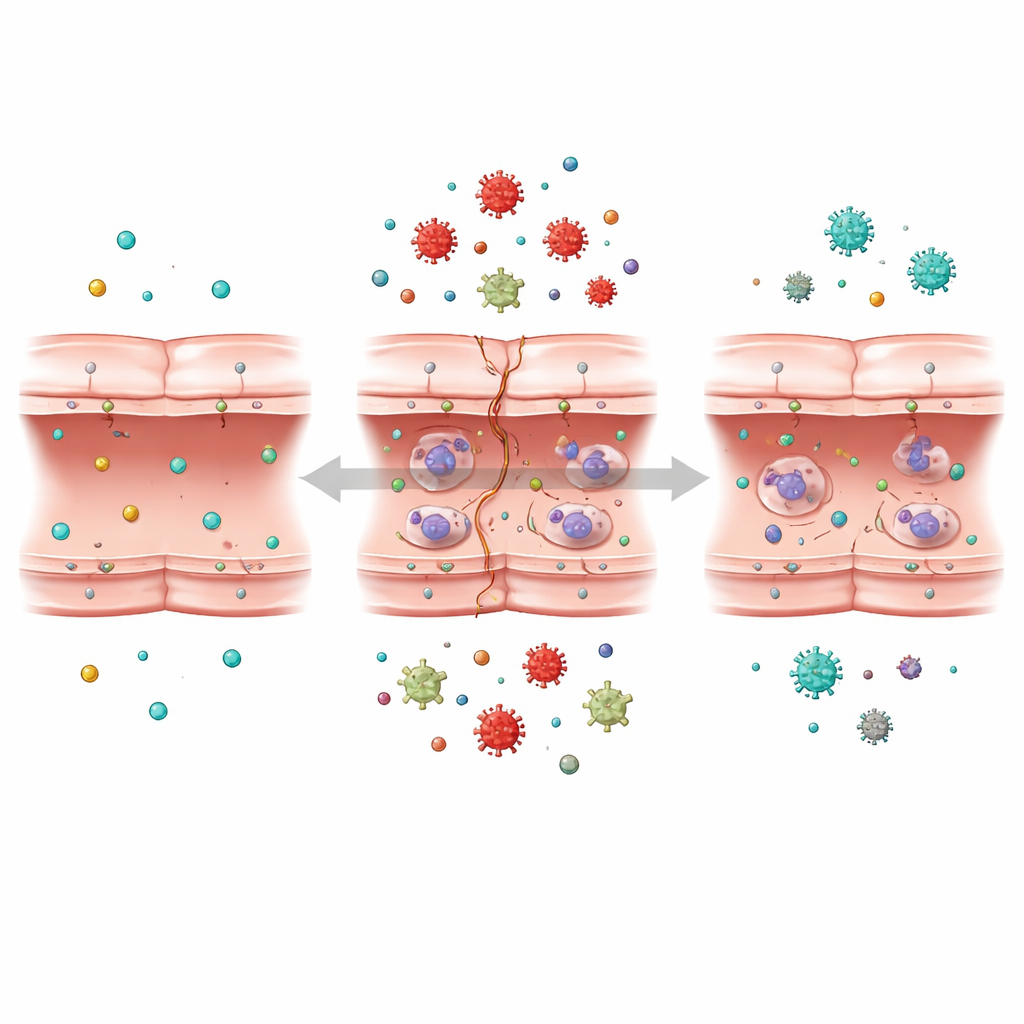
Ouvindo a conversa molecular da célula
A equipe então recorreu a uma técnica poderosa conhecida como transcriptômica, que lê os níveis de atividade de milhares de genes simultaneamente. Comparando células normais, células submetidas à privação de oxigênio e glicose e células permitidas a se recuperar, eles identificaram mais de mil genes cuja atividade mudou em resposta ao estresse semelhante ao do AVC. Usando ferramentas avançadas de análise de dados e aprendizado de máquina, agruparam genes que se comportavam de forma semelhante e buscaram aqueles mais fortemente ligados à lesão da barreira. Encontraram que muitos dos genes mais afetados estavam relacionados a três estruturas-chave dentro da célula: o ribossomo, que sintetiza proteínas; o retículo endoplasmático, que ajuda a dobrar e processar essas proteínas; e as mitocôndrias, as pequenas usinas de energia que fornecem energia.
Ribossomos emergem como sinais reveladores
A partir desse grande conjunto de genes, os pesquisadores usaram um algoritmo random forest — um tipo de aprendizado de máquina baseado em árvores de decisão — para reduzir a lista a um grupo curto de genes especialmente informativos. Em seguida mapearam como as proteínas correspondentes interagem entre si. Essa análise destacou seis genes centrais, a maioria relacionada ao ribossomo, a fábrica de proteínas da célula. Na condição semelhante ao AVC, esses genes ligados ao ribossomo foram ativados mais intensamente, enquanto sua atividade diminuiu em direção ao normal quando oxigênio e glicose foram restaurados. Esse padrão sugere que mudanças na maquinaria de produção de proteínas da célula podem ser um sinal precoce sensível de dano e recuperação da barreira hematoencefálica.
O que isso pode significar para o cuidado futuro
Para um público leigo, a mensagem principal é que este estudo aponta para uma nova classe de “luzes de alerta” moleculares que se acendem quando a barreira protetora do cérebro é lesionada durante um AVC. Em vez de focar apenas em culpados já conhecidos, como enzimas que degradam a parede vascular, o trabalho mostra que as próprias fábricas de proteínas celulares respondem fortemente ao dano e se acalmam quando as condições melhoram. Se pesquisas futuras confirmarem que esses marcadores relacionados a ribossomos podem ser detectados em amostras de pacientes, como sangue, os médicos poderão um dia usá-los para avaliar a gravidade da lesão da barreira, programar tratamentos que reduzam inflamação e edema, e testar novos fármacos destinados a preservar esse guardião crucial da saúde cerebral.
Citação: Liu, X., He, Y., Zhang, N. et al. Identification of blood-brain barrier injury-related biomarkers in cerebral infarction using transcriptomic analysis. Sci Rep 16, 8119 (2026). https://doi.org/10.1038/s41598-026-39763-2
Palavras-chave: acidente vascular isquêmico, barreira hematoencefálica, biomarcadores, genes ribossomais, células endoteliais