Clear Sky Science · pt
Mutação associada ao transtorno do espectro do autismo Sema5A p.Arg676Cys ativa sinalização Arf6/FE65 e morfogênese celular aberrante
Como uma pequena alteração pode atrapalhar a fiação cerebral
O transtorno do espectro do autismo afeta a maneira como as pessoas se comunicam, interagem e respondem ao mundo ao redor, mas os passos biológicos que ligam uma mudança no DNA a uma alteração na função cerebral costumam ser misteriosos. Este estudo investiga uma dessas alterações genéticas em uma proteína de "orientação" cerebral chamada Sema5A e mostra, em detalhes incomuns, como um único bloco construtor trocado nessa proteína pode levar células nervosas jovens a formar ramos excessivamente longos e emaranhados. Entender esse erro microscópico na fiação pode, eventualmente, ajudar cientistas a projetar tratamentos que estimulem as células cerebrais a retomar uma forma mais saudável.
Células cerebrais que crescem demais
Durante o desenvolvimento cerebral, células nervosas jovens estendem prolongamentos longos e finos que buscam os parceiros corretos, formando os circuitos que sustentam o pensamento e o comportamento. Esse crescimento precisa ser rigidamente controlado: ramificação insuficiente impede conexões; excesso pode tornar os circuitos barulhentos ou mal conectados. Trabalhos anteriores mostraram que uma versão de Sema5A ligada ao autismo, na qual um aminoácido na posição 676 é trocado de arginina para cisteína, faz com que neurônios em cultura cresçam processos incomumente longos. O novo estudo procurou descobrir quais interruptores internos e proteínas auxiliares esse Sema5A mutante usa para impulsionar esse crescimento descontrolado.
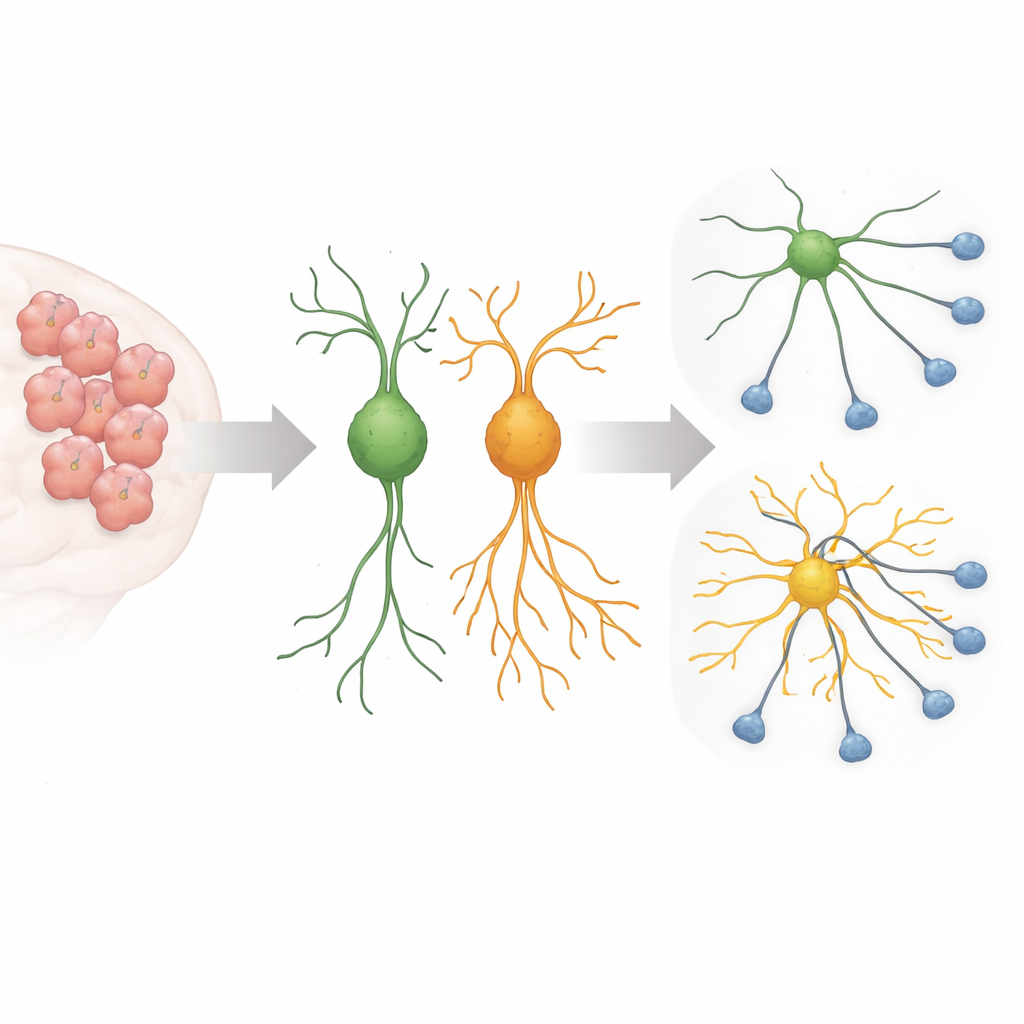
Um sinal enganoso dentro da célula
Os pesquisadores se concentraram em um pequeno interruptor molecular chamado Arf6 e em uma proteína andaime chamada FE65, ambas conhecidas por ajudar a moldar as membranas celulares e o esqueleto interno que sustenta os prolongamentos celulares. Usando um sistema CRISPR–Cas13 para reduzir seletivamente essas proteínas em células com características neuronais de camundongo e em neurônios primários de camundongo, eles descobriram que diminuir Arf6 ou FE65 reduziu fortemente o crescimento excessivo causado pela Sema5A mutante. Os processos longos e aracnídeos encolheram em direção a comprimentos mais típicos, e marcadores de maturação neuronal diminuíram, sugerindo que o efeito da mutação depende fortemente dessa via de sinalização específica.
Conectando-se ao motor de forma da célula
No interior dos neurônios, uma família de moléculas atua como um "motor" de forma controlando a actina, o principal filamento estrutural nos ramos celulares. Um membro chave dessa família, Rac1, normalmente se ativa para ajudar a extensão dos neuritos, mas atividade excessiva pode provocar crescimento descontrolado. A equipe mostrou que, em células com Sema5A normal, Arf6 é necessário para a ativação ordinária de Rac1 durante o crescimento saudável, enquanto FE65 não é essencial. Com a Sema5A mutante, porém, tanto Arf6 quanto FE65 tornaram-se críticos: reduzir qualquer um deles, ou inundar a célula apenas com a região de FE65 que se liga ao parceiro ELMO2, reduziu a atividade anormalmente alta de Rac1 de volta a níveis próximos do normal. Isso implica que a versão prejudicial de Sema5A explora especificamente um complexo Arf6–FE65–ELMO2–DOCK5 para hiperestimular Rac1 e levar os neuritos a crescer em excesso.
Um centro lotado de parceiros de sinalização
Para entender como essas peças se encaixam, os cientistas também examinaram "sinalossomos" baseados em ELMO2 — aglomerados de proteínas que se montam para transmitir sinais de crescimento. Quando Arf6 ou FE65 foi reduzido, células expressando Sema5A mutante formaram menos desses complexos de ELMO2 em seus corpos e nas pontas em crescimento, consistente com a ideia de que Arf6 e FE65 ajudam a montar a maquinaria que traduz a mutação de Sema5A em uma mudança física na forma celular. O trabalho se insere em um quadro mais amplo no qual pequenos interruptores moleculares como Arf6 e Rac1, auxiliados por andaimes como FE65, atuam como centros que ligam muitos genes associados ao autismo à arquitetura final dos circuitos cerebrais.
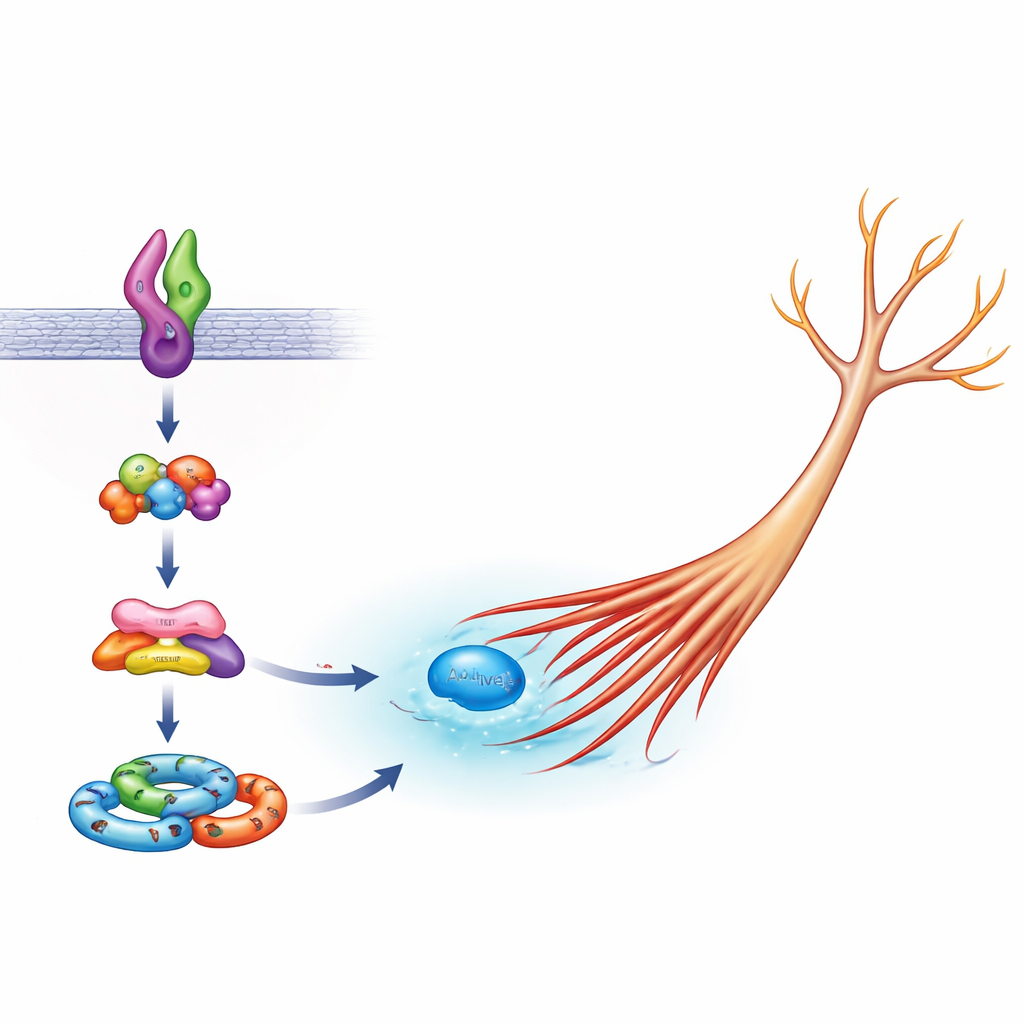
Por que essa cadeia microscópica importa
Para um não especialista, a sopa de letras de nomes de proteínas pode parecer distante da experiência vivida do autismo. Ainda assim, este estudo oferece uma ponte concreta: traça como uma alteração genética precisa em Sema5A pode hiperativar uma cadeia específica de moléculas auxiliares, fazendo com que neurônios estendam seus ramos em excesso e potencialmente conectem o cérebro de maneiras atípicas. Ao apontar Arf6, FE65 e o complexo sinalizador ELMO2 como elos cruciais nessa cadeia, o trabalho destaca potenciais alvos farmacológicos futuros. Em princípio, medicamentos que suavemente reduzam essa via hiperativa poderiam um dia ajudar a corrigir as mudanças subjacentes na forma celular associadas a formas de autismo relacionadas à Sema5A, adicionando uma peça importante ao grande quebra-cabeça dos transtornos do desenvolvimento neuropsicológico.
Citação: Takahashi, M., Yako, H., Miyamoto, Y. et al. Autism spectrum disorder-associated Sema5A p.Arg676Cys drives Arf6/FE65 signaling and aberrant cell morphogenesis. Sci Rep 16, 9423 (2026). https://doi.org/10.1038/s41598-026-39722-x
Palavras-chave: transtorno do espectro do autismo, mutação Sema5A, morfogênese neuronal, sinalização Rac1, via Arf6 FE65