Clear Sky Science · pt
Direcionamento de tipos neuronais específicos no cérebro de primatas não humanos usando um imunotóxico recombinante específico para CD25 murino
Por que este estudo cerebral é importante
Compreender como grupos específicos de células cerebrais controlam movimento, emoção e comportamento é fundamental para tratar distúrbios como a doença de Parkinson e o autismo. Mas o cérebro é uma floresta densa de células entrelaçadas, e a maioria das ferramentas derruba muitas árvores de uma vez. Este estudo apresenta uma forma de remover apenas um tipo escolhido de neurônio no cérebro de um macaco, com dano colateral mínimo, abrindo caminho para experimentos muito mais precisos sobre como circuitos particulares moldam comportamento e doença.
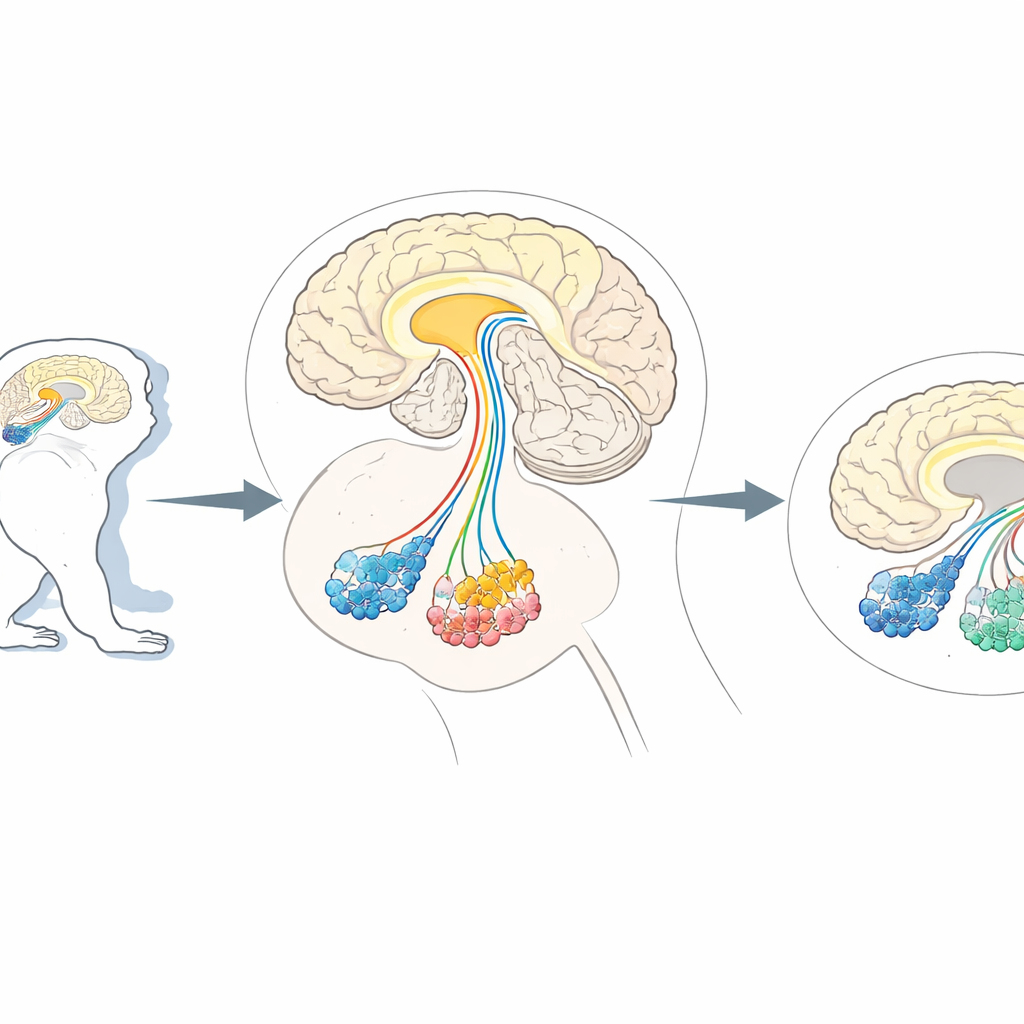
A necessidade de uma "poda" celular cerebral precisa
Pesquisadores frequentemente recorrem a primatas não humanos, como saguis e macacos, porque seus cérebros são organizados de forma muito parecida com o nosso. Esses animais são modelos inestimáveis para condições que afetam funções cerebrais superiores, desde problemas de movimento parkinsonianos até alterações sociais semelhantes ao autismo. Métodos existentes podem silenciar ou estimular vias específicas, mas remover realmente apenas um tipo de neurônio nesses cérebros complexos, sem prejudicar outros, continua difícil. Trabalhos anteriores em camundongos usaram um artifício: neurônios selecionados foram geneticamente modificados para exibir um marcador de superfície celular chamado CD25, que pode ser reconhecido por uma toxina projetada que mata apenas as células marcadas. Contudo, esse mesmo marcador ocorre naturalmente nas células imunes de primatas e possivelmente em células cerebrais, aumentando o risco de que a toxina ataque alvos errados em macacos.
Desenhando um bisturi molecular mais seguro
Os autores propuseram construir um novo bisturi molecular adaptado para uso em primatas. Em vez de mirar na versão humana do CD25, focaram na versão murina, que é muito menos semelhante ao CD25 natural encontrado em macacos. Primeiro imunizaram um coelho com a proteína CD25 de camundongo e usaram um método baseado em chip para selecionar células individuais do coelho que produziam anticorpos que se ligavam fortemente ao CD25 murino, mas não à forma humana. A partir dessas, identificaram um anticorpo de destaque, chamado RMAb-52, com afinidade muito alta. Em seguida, juntaram as partes-chave desse anticorpo com um fragmento tóxico da bactéria Pseudomonas para criar uma única proteína imunotóxica engineered, denominada anti-mCD25-PE38.
Testando a ferramenta
Em experimentos em tubo de ensaio, o novo imunotóxico ligou-se ao CD25 murino muito mais firmemente do que ao CD25 humano, confirmando sua seletividade. Quando aplicado a células cultivadas geneticamente modificadas para portar o CD25 murino, a toxina reduziu drasticamente sua sobrevivência em doses muito baixas, enquanto deixou intactas células que expressavam CD25 humano. Em seguida, a equipe passou para saguis vivos. Usando um vetor viral especial que viaja retrogradamente ao longo de fibras nervosas, eles entregaram o gene do CD25 murino em neurônios produtores de dopamina que enviam sinais de uma região profunda do cérebro chamada substância negra para o estriado, uma via crucial para o controle do movimento. Após dar tempo para o vírus ativar o marcador nesses neurônios, injetaram a proteína anti-mCD25-PE38 diretamente na área alvo do mesencéfalo.
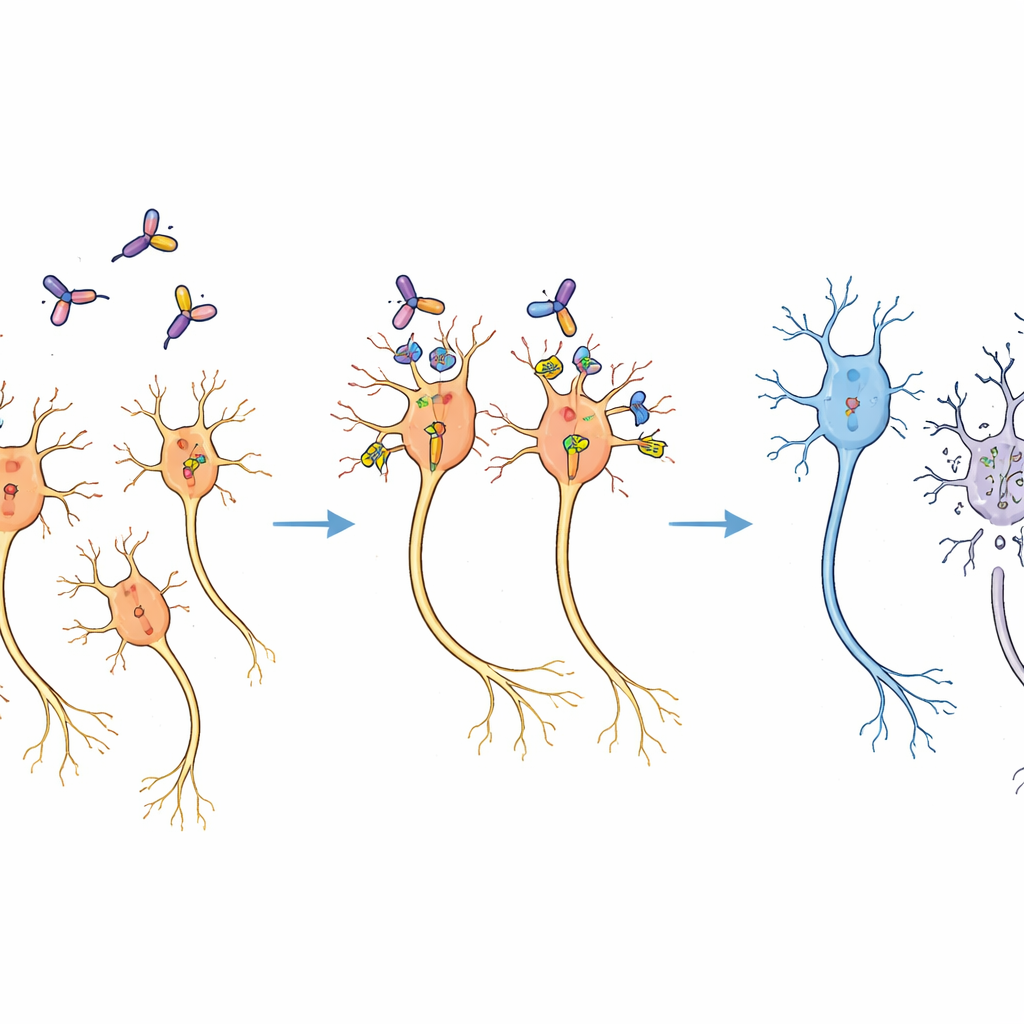
Perda seletiva sem dano generalizado
Duas semanas após o tratamento, cortes cerebrais dos saguis contaram uma história clara. Do lado que recebeu o imunotóxico, o número de neurônios dopaminérgicos foi reduzido para cerca de dois terços do observado no lado não tratado, conforme demonstrado por coloração para uma enzima produtora de dopamina. Ainda assim, o tecido cerebral circundante parecia normal ao microscópio, e outras regiões cerebrais que também receberam o vetor viral não apresentaram perda óbvia de células. Experimentos piloto já haviam estabelecido uma faixa de dose que evitava lesão tecidual inespecífica, e a dose escolhida ficou bem dentro dessa janela segura. O padrão de perda correspondia à propagação esperada do vírus e da toxina, indicando que os neurônios foram eliminados especificamente porque haviam sido geneticamente programados para exibir CD25 murino, e não porque a toxina estava prejudicando células indiscriminadamente.
O que isso significa para pesquisas cerebrais futuras
Para um leitor leigo, a mensagem-chave é que os pesquisadores construíram um botão de exclusão altamente seletivo para populações neuronais escolhidas em cérebros de primatas. Ao combinar um sistema de entrega viral retrógrado com um imunotóxico específico para murino, eles podem remover vias definidas — por exemplo, circuitos dopaminérgicos implicados na doença de Parkinson — preservando as células vizinhas. Essa estratégia evita reações cruzadas perigosas com o CD25 natural do animal e deve ser especialmente útil quando esse receptor natural está presente ou aumentado na doença. A longo prazo, essa abordagem ajudará cientistas a mapear como rotas individuais na fiação cerebral contribuem para movimento, tomada de decisão e sintomas psiquiátricos, aproximando-nos de tratamentos direcionados que ajustem circuitos defeituosos em vez de afetar amplamente todo o cérebro.
Citação: Kobayashi, T., Kato, S., Kimura, S. et al. Targeting of specific neuronal types in the non-human primate brain by using a murine CD25-specific recombinant immunotoxin. Sci Rep 16, 8247 (2026). https://doi.org/10.1038/s41598-026-39662-6
Palavras-chave: neurociência em primatas não humanos, direcionamento por imunotóxico, neurônios dopaminérgicos, circuitos cerebrais de saguis, modelos da doença de Parkinson