Clear Sky Science · pt
Um conjunto multimodal em zebrafish para estudar a barreira hematoencefálica na saúde e na doença
Por que vasos cerebrais permeáveis importam
Quando os vasos sanguíneos no cérebro ou no olho começam a vazar, fluido e proteínas penetram no tecido nervoso circundante, causando inchaço que pode turvar a visão ou prejudicar o raciocínio. Esse tipo de “encharcamento” — conhecido como edema vasogênico — contribui para perda visual relacionada ao diabetes, AVC, trauma cerebral e algumas formas de demência. Ainda assim, os cientistas não dispõem de métodos simples e acessíveis para observar essa barreira protetora falhar em tempo real. Este estudo apresenta um modelo versátil em zebrafish que permite aos pesquisadores visualizar, quantificar e investigar como a hiperglicemia enfraquece a barreira vascular do cérebro, potencialmente acelerando a busca por novos tratamentos.
Um peixinho com uma vantagem clara
Larvas de zebrafish oferecem uma janela única para o cérebro vivo. Ao contrário dos mamíferos, seus corpos são transparentes nas fases iniciais de vida, e os vasos sanguíneos cerebrais podem ser tornados fluorescentes ao microscópio. Os autores aproveitaram isso ao focar na barreira hematoencefálica, o selo apertado entre o sangue e o tecido cerebral que se assemelha à barreira hemato-retiniana interna que protege nossos olhos. Como os mesmos tipos celulares e muitas das mesmas proteínas protetoras são compartilhados entre cérebro e retina, a equipe usou a barreira cerebral no zebrafish como substituta para estudar doenças como edema macular diabético e outros distúrbios neurovasculares, mas em um sistema mais rápido, mais ético e menos caro que os modelos tradicionais em roedores.
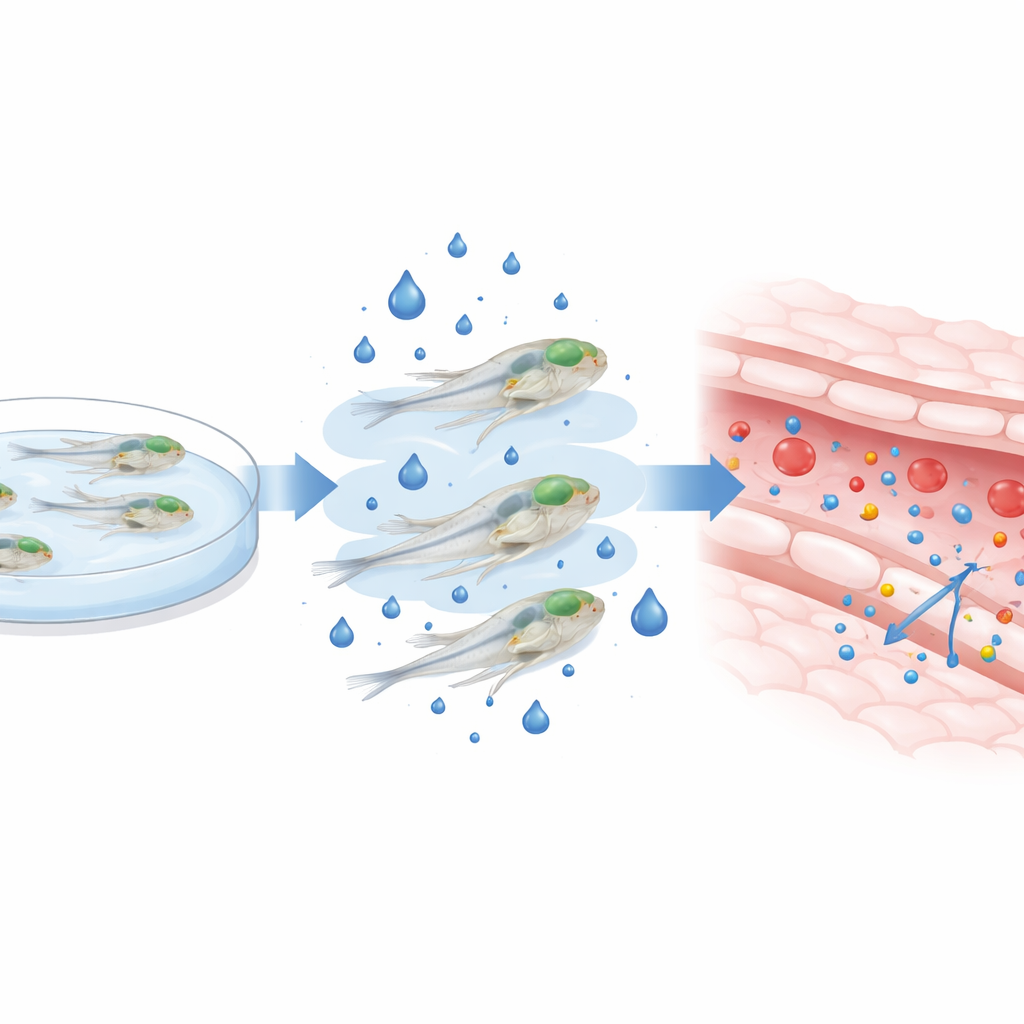
Aumentando a glicose em filhotes de zebrafish
Para imitar a alta glicemia observada no diabetes, os pesquisadores criaram larvas de zebrafish em água contendo glicose adicional entre três e cinco dias após a fertilização — uma janela crítica em que a barreira cerebral ainda está se desenvolvendo. Confirmaram que esse banho externo de açúcar elevou os níveis internos de glicose várias vezes sem matar as larvas ou alterar sua forma geral. Com os peixes ainda vivos e nadando, injetaram corantes fluorescentes de diferentes tamanhos na circulação e usaram microscopia confocal de alta resolução para rastrear quanto corante escapava dos vasos cerebrais para o tecido circundante. Após dois dias de exposição à glicose elevada, tanto moléculas de corante pequenas quanto grandes vazaram mais para o cérebro, especialmente na dose maior de açúcar, indicando que a barreira havia se tornado mais permeável.
O que acontece na parede do vaso
Além de simplesmente medir o vazamento, a equipe construiu uma “caixa de ferramentas” multimodal para examinar o que estava dando errado na própria parede vascular. Mediram a largura de uma artéria cerebral chave e descobriram que a glicose elevada causou dilatação do vaso — uma mudança precoce também observada em pessoas com doença ocular diabética. Usando zebrafish geneticamente modificados para iluminar proteínas específicas, mostraram que a glicose elevada reduziu os níveis de claudina-5, um componente importante dos selos estreitos entre células vasculares vizinhas, e aumentou os níveis de PLVAP, uma proteína associada a vasos imaturos e propensos a vazamentos que transportam material através da camada celular. A microscopia eletrônica, capaz de revelar estruturas na escala nanométrica, confirmou um alargamento sutil nas junções entre células, embora os pequenos bolsões de transporte chamados caveolas fossem escassos demais para quantificação confiável nesta primeira análise.
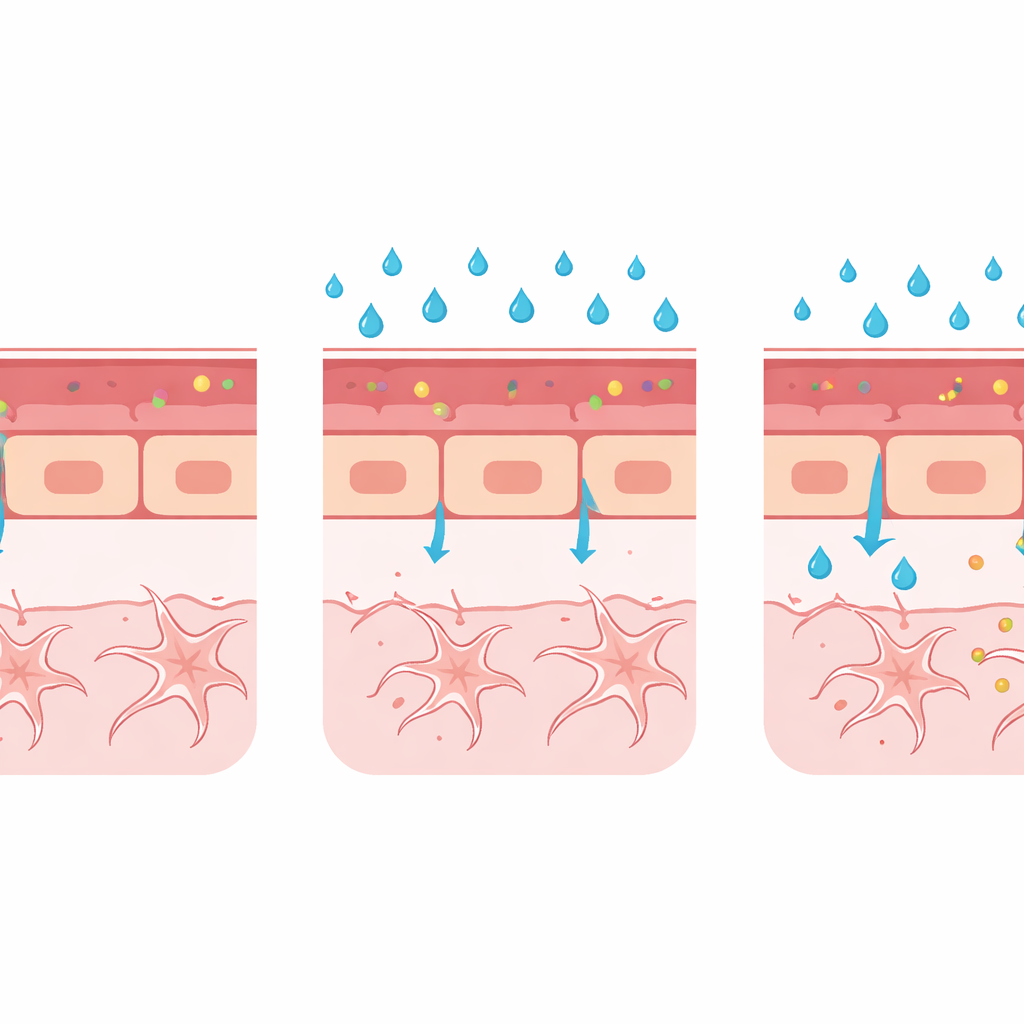
Uma plataforma flexível para pesquisas futuras sobre doenças
Em conjunto, essas mudanças — mais vazamento de corante, vasos mais dilatados, junções celulares mais fracas e aumento de PLVAP — desenham um quadro consistente: a glicemia elevada pode atrasar ou atrapalhar a formação adequada da barreira no cérebro em desenvolvimento. O modelo ainda não reproduz a ruptura de uma barreira plenamente madura, como ocorre em doenças humanas crônicas, mas é excelente para mostrar como condições prejudiciais durante o desenvolvimento podem impedir que a barreira se feche corretamente. Como as técnicas são compatíveis com uma variedade de linhagens repórter fluorescentes e imageamento avançado, a mesma plataforma pode ser ampliada para estudar outros gatilhos de falha da barreira, como moléculas inflamatórias, alterações em células de suporte como pericitos e glia, ou interrupções em vias de sinalização-chave.
O que isso significa para os pacientes
Para não especialistas, a mensagem principal é que este trabalho oferece um ensaio prático e vivo para observar a falha da parede protetora do cérebro sob estresse, usando peixinhos minúsculos e transparentes em vez de mamíferos maiores. Ao acompanhar como a glicemia elevada remodela a estrutura e a função dos vasos em tempo real, os pesquisadores podem identificar mais rapidamente quais moléculas e tipos celulares devem ser alvos para manter a barreira intacta. Em última análise, esses conhecimentos podem orientar o desenvolvimento de novos medicamentos ou estratégias terapêuticas para prevenir ou reduzir o vazamento de fluidos nos olhos e no cérebro — ajudando a preservar a visão e proteger a função cognitiva em pessoas com diabetes e outras doenças neurovasculares.
Citação: Bakker-van Bugnum, N., Snijders, E.E., Hogendorp, E.F. et al. A zebrafish multimodal toolbox to study the blood-brain barrier in health and disease. Sci Rep 16, 9422 (2026). https://doi.org/10.1038/s41598-026-39616-y
Palavras-chave: barreira hematoencefálica, modelo em zebrafish, complicações diabéticas, vazamento vascular, doença neurovascular