Clear Sky Science · pt
Caracterização genômica e in vitro de dois bacteriófagos líticos que infectam a cepa multirresistente de Erwinia AnSW2-5
Por que bactérias que destroem plantações importam para todos
Ao redor do mundo, agricultores enfrentam doenças bacterianas que apodrecem frutos, murcham folhas e arrasam colheitas. Muitos desses surtos agora são causados por linhagens que não respondem mais a antibióticos comuns, ameaçando tanto o abastecimento de alimentos quanto os meios de subsistência dependentes deles. Este estudo explora uma alternativa emergente: usar vírus que atacam bactérias, chamados bacteriófagos, para desarmar com segurança um patógeno vegetal particularmente persistente encontrado em solo associado ao intenso uso de antibióticos.
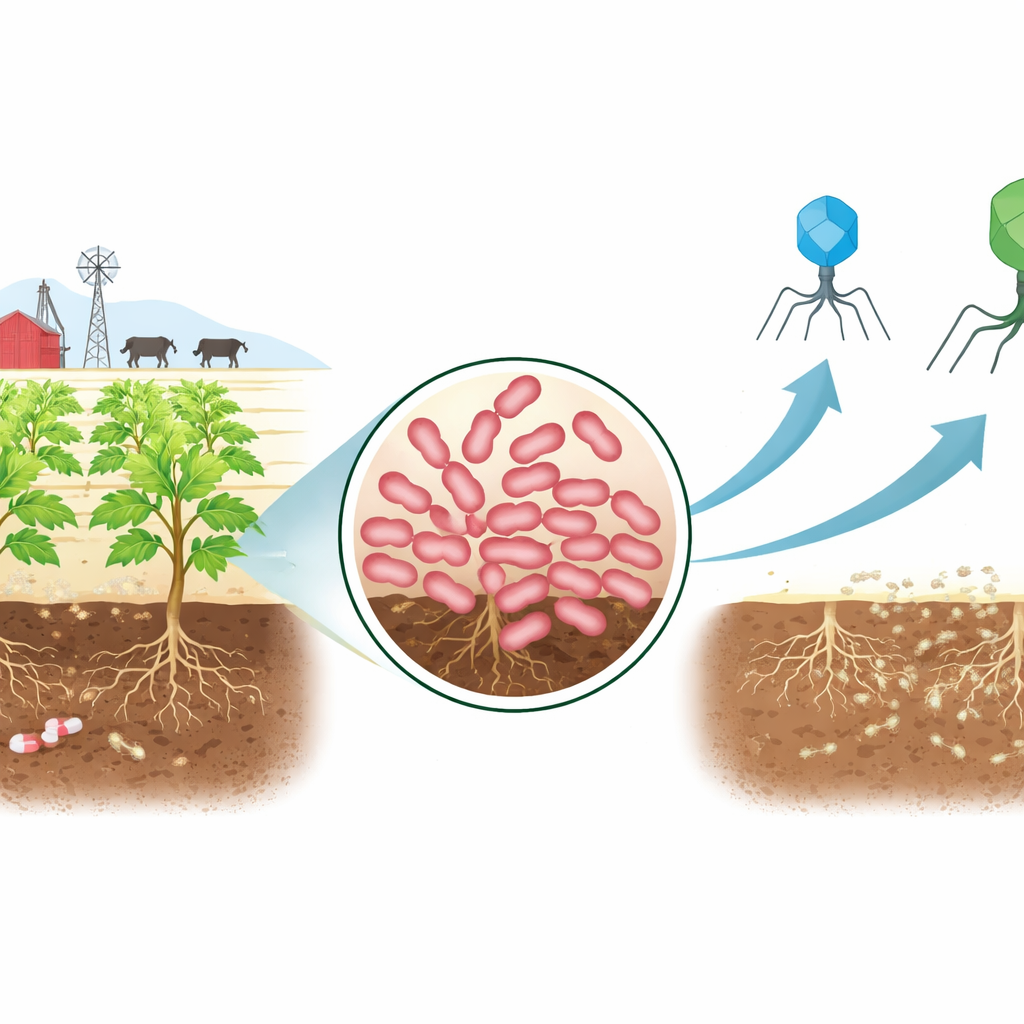
Um invasor novo e difícil no campo
Os pesquisadores começaram coletando amostras de solo de um curral conhecido por receber resíduos de gado e antibióticos. Desse ambiente desafiador eles isolaram uma cepa de Erwinia, um grupo bacteriano que inclui os notórios responsáveis pela queimadura bacteriana em macieiras e pela podridão em batatas. Testes mostraram que essa cepa, nomeada AnSW2-5, resistia a várias classes principais de antibióticos, incluindo drogas usadas contra uma ampla gama de infecções. A análise genética confirmou a razão: seu DNA carregava vários genes de resistência conhecidos e poderosas bombas moleculares que ejetam antibióticos da célula. Ao mesmo tempo, comparações genômicas revelaram que essa cepa é distinta de espécies de Erwinia descritas anteriormente, tornando-a um modelo útil para estudar como controlar novos patógenos de plantas de difícil tratamento.
Dois predadores minúsculos com pontos fortes diferentes
Para encontrar inimigos naturais dessa bactéria multirresistente, a equipe recorreu à água doce do mesmo local e a enriquecendo para bacteriófagos capazes de infectar AnSW2-5. Eles isolaram dois candidatos promissores, rotulados P-A e P-K. Ao microscópio eletrônico, P-A parecia compacto com uma cauda curta, uma morfologia associada a infectação rápida e direta. P-K, em contraste, apresentava uma cauda contratátil mais longa com uma base complexa, sugerindo um modo mais vigoroso de perfurar seu hospedeiro. O sequenciamento de seus genomas mostrou que ambos os fagos são estritamente líticos: invadem, replicam e rompem a célula, em vez de permanecerem ocultos no DNA bacteriano. Ainda assim, fazem isso com ferramentas genéticas muito diferentes — o genoma enxuto de P-A sustenta um ataque rápido, enquanto o genoma maior de P-K codifica maquinaria estrutural e de replicação mais elaborada.
Como a dupla viral ataca
Quando os cientistas acompanharam o ciclo de vida de cada fago em laboratório, descobriram que P-A ataca rapidamente: leva apenas cerca de 20 minutos antes que novas partículas virais comecem a aparecer, e cada bactéria infectada libera cerca de 70 descendentes. P-K demora mais — cerca de 35 minutos antes de começar a produzir novos fagos — mas cada célula infectada gera aproximadamente 110 novas partículas. Em testes de cocultura nos quais bactérias e fagos crescem juntos por três dias, ambos os fagos isoladamente retardaram o crescimento bacteriano, mas não o impediram completamente. As bactérias eventualmente se recuperaram, refletindo o aparecimento de sobreviventes resistentes. No entanto, quando P-A e P-K foram combinados em um único coquetel, reduziram a população bacteriana em mais de 80% e a mantiveram suprimida durante todo o experimento de 72 horas.
Impedindo que a resistência crie raízes
Uma das descobertas mais marcantes foi como o par de fagos afetou a emergência de mutantes resistentes. Quando expostas apenas a P-A ou a P-K, uma pequena fração de bactérias — aproximadamente uma em um milhão a uma em dez milhões — conseguiu escapar e crescer apesar do ataque viral. Mas quando os dois fagos foram usados juntos, colônias resistentes tornaram-se tão raras que caíram abaixo do limite de detecção do experimento. Isso sugere que os dois vírus provavelmente se ligam a alvos diferentes na superfície bacteriana ou perturbam a célula de maneiras complementares. Para uma única bactéria sobreviver, ela precisaria superar ambos ao mesmo tempo, um evento extraordinariamente improvável. Em termos práticos, isso torna o coquetel muito mais robusto contra as manobras evolutivas que frequentemente condenam os antibióticos.
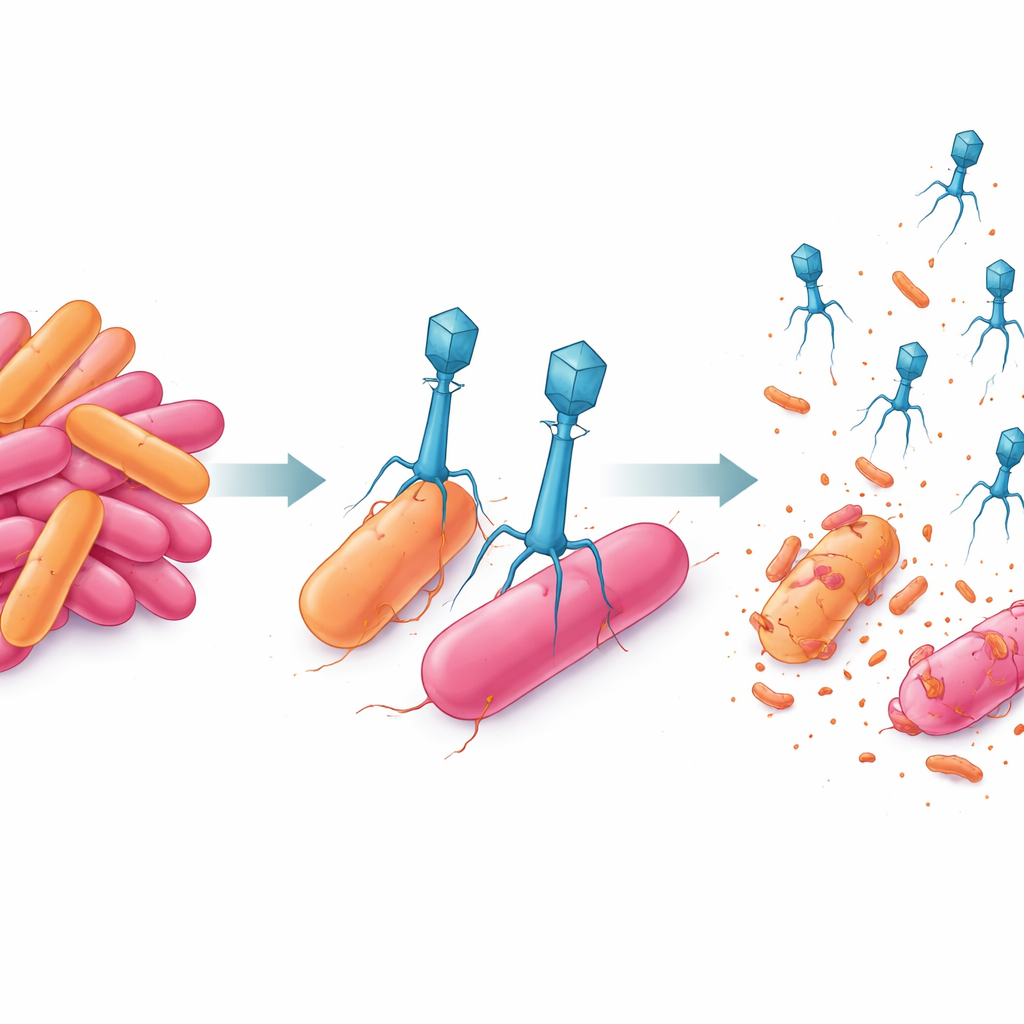
O que isso pode significar para colheitas futuras
Em conjunto, o trabalho mostra que pares cuidadosamente escolhidos de bacteriófagos podem fazer mais do que apenas reduzir bactérias vegetais perigosas — eles também podem limitar a capacidade das bactérias de evoluir resistência. Ao combinar um fago de ação rápida com outro que produz maior número de descendentes, os pesquisadores criaram uma dupla viral que manteve sob controle uma cepa multirresistente de Erwinia por dias, além de impedir variantes detectáveis de escape. Embora esses experimentos tenham sido realizados em laboratório e não em pomares ou campos, apontam para um futuro em que misturas de fagos direcionadas façam parte do manejo integrado de pragas, ajudando agricultores a proteger culturas com muito menor dependência de antibióticos tradicionais.
Citação: Baek, K., Goh, J. & Choi, A. Genomic and in vitro characterization of two lytic bacteriophages infecting multidrug-resistant Erwinia sp. strain AnSW2-5. Sci Rep 16, 8172 (2026). https://doi.org/10.1038/s41598-026-39563-8
Palavras-chave: controle biológico por bacteriófagos, doenças bacterianas de plantas, resistência a antibióticos na agricultura, terapia por fagos contra Erwinia, coquetéis de fagos