Clear Sky Science · pt
Perfil proteômico do líquido de lavagem broncoalveolar após desafio endotóxico segmentar em humanos — um possível modelo de exacerbação
Por que um curto surto de inflamação pulmonar importa
Doenças pulmonares crônicas, como a doença pulmonar obstrutiva crônica (DPOC), frequentemente pioram de forma súbita quando as vias aéreas se inflamam agudamente, geralmente por infecções. Esses episódios, chamados exacerbações, levam muitas pessoas ao hospital e podem piorar permanentemente a função respiratória. Estudá‑los diretamente em pacientes é difícil e arriscado. Este estudo usa uma irritação pulmonar breve e cuidadosamente controlada em voluntários saudáveis para imitar alguns aspectos dessas crises e, em seguida, mede centenas de proteínas no fluido pulmonar para ver quais sinais são ativados. As descobertas ajudam os pesquisadores a entender a química da inflamação pulmonar e podem acelerar a busca por novos tratamentos.
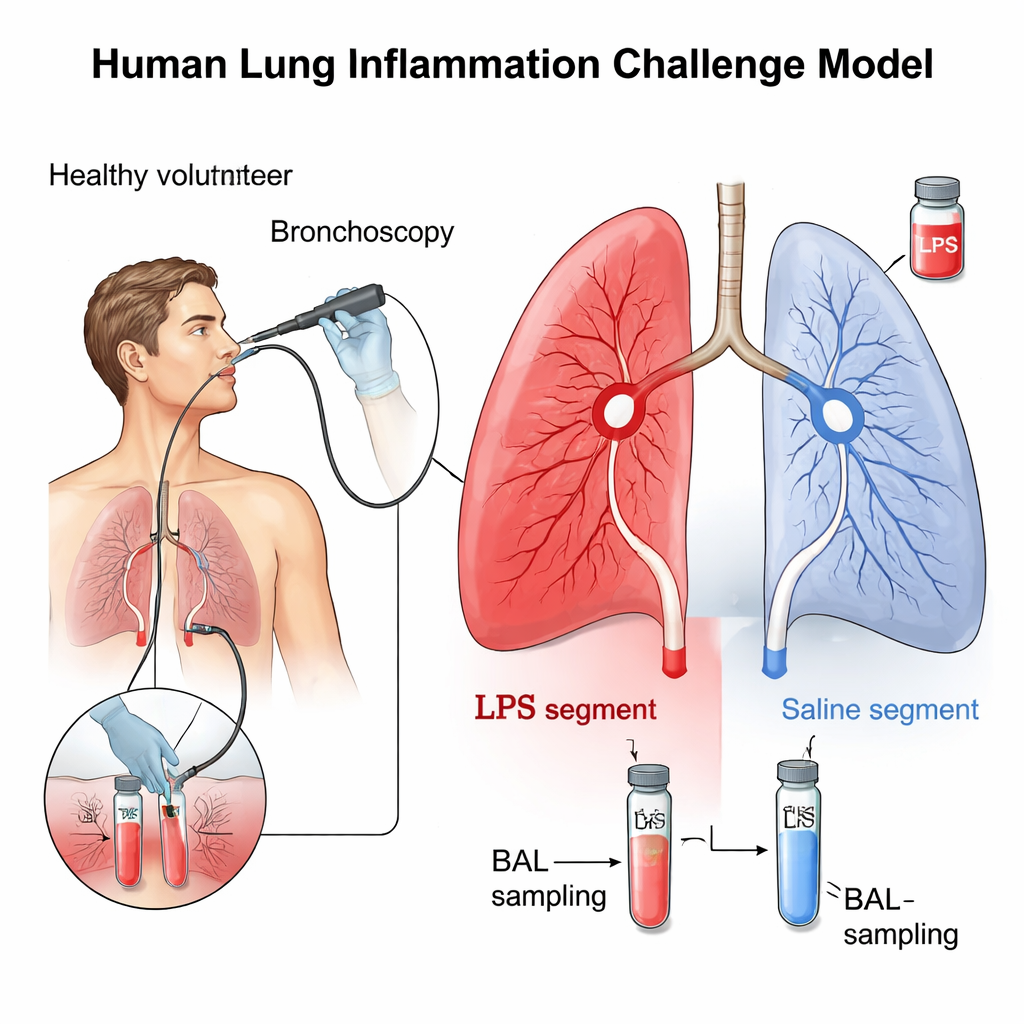
Criando uma mini “explosão” pulmonar segura
Os pesquisadores usaram uma técnica bem estabelecida que irrita brevemente e de forma localizada uma pequena região do pulmão. Dez adultos saudáveis e não fumantes foram submetidos a broncoscopia, na qual um tubo fino e flexível é guiado pelas vias aéreas. Através desse tubo, a equipe colocou uma pequena dose de endotoxina bacteriana, conhecida como lipopolissacarídeo (LPS), em um segmento pulmonar e soro fisiológico em um segmento correspondente do outro lado como controle. O LPS é um componente natural de certas bactérias que ativa fortemente as defesas do organismo. Após 24 horas, as mesmas áreas foram lavadas com solução salina, um procedimento chamado lavagem broncoalveolar (LBA), para coletar o fluido e as células do interior profundo dos pulmões para análise detalhada.
Fazendo um censo de proteínas no fluido pulmonar
Em vez de olhar apenas alguns marcadores conhecidos, a equipe aplicou uma tecnologia de alto rendimento (plataforma SomaScan) que pode medir cerca de 1.500 proteínas diferentes de uma só vez no fluido de LBA. Eles compararam amostras tomadas antes de qualquer desafio, após aplicação de soro fisiológico e após LPS. Como esperado, amostras pré‑desafio e de soro fisiológico eram muito semelhantes, confirmando que o próprio procedimento não provocou inflamação. Em contraste, os segmentos tratados com LPS mostraram uma mudança dramática: 599 proteínas aumentaram significativamente e apenas quatro diminuíram. Muitas das proteínas elevadas são mensageiros inflamatórios bem conhecidos, incluindo IL‑6 e IL‑8, enzimas como mieloperoxidase (MPO) e MMP9, e proteínas de fase aguda como proteína C‑reativa (PCR) e fator von Willebrand (VWF). Análises de componentes principais e de agrupamento mostraram que as amostras de LPS formaram um grupo claramente separado, ressaltando o quão fortemente esse desafio local altera o ambiente pulmonar.
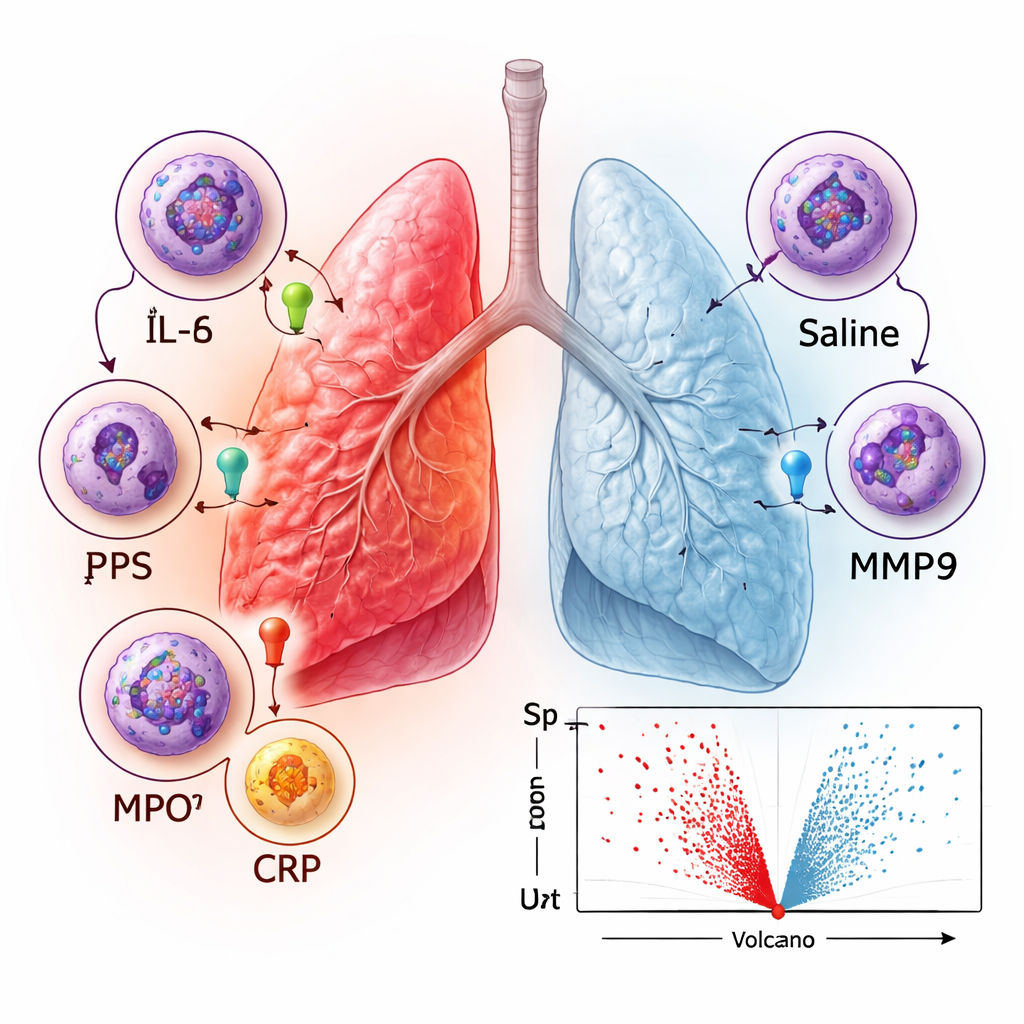
O que os padrões de proteínas revelam sobre as defesas pulmonares
Para ir além de marcadores isolados, a equipe examinou quais tipos de processos biológicos eram mais enriquecidos entre as proteínas que aumentaram após LPS. Os sinais mais fortes envolveram atividade imune geral e respostas a estímulos externos ou químicos, junto com processos relacionados ao movimento celular e à morte celular programada. A análise de rede de como as proteínas interagem entre si destacou agrupamentos de quimiocinas (moléculas que atraem células imunes), enzimas de remodelamento tecidual chamadas metaloproteinases da matriz e componentes do imunoproteassoma, uma máquina celular que ajuda a processar proteínas estranhas para reconhecimento imune. Esses padrões correspondem ao que se sabe sobre a resposta pulmonar a infecções: células imunes como neutrófilos são atraídas para as vias aéreas, microrganismos nocivos são atacados e o tecido circundante é remodelado e, se necessário, reparado.
Conectando o modelo às exacerbações reais de DPOC
Os autores então investigaram o quanto esse modelo de LPS de curto prazo reflete as exacerbações reais da DPOC. Eles compararam seus dados do fluido pulmonar com uma lista publicada de biomarcadores sanguíneos que aumentam quando pessoas com DPOC têm uma crise. De 17 marcadores avaliáveis, 16 — incluindo IL‑6, IL‑8, PCR, fibrinogênio e várias quimiocinas — também estavam elevados no LBA após LPS. Apenas um (sTREM‑1) não mudou, em linha com resultados anteriores mistos sobre sua utilidade. Essa forte sobreposição sugere que muitas das mesmas vias inflamatórias são ativadas quando um pulmão saudável é desafiado brevemente com LPS e quando um pulmão vulnerável com DPOC sofre uma exacerbação séria. Ao mesmo tempo, os autores observam que a resposta ao LPS é temporária e não reproduz completamente o dano estrutural crônico observado em doença de longa duração.
O que isso significa para tratamentos futuros
Em termos simples, este estudo mostra que uma irritação controlada e de curta duração em parte do pulmão de voluntários saudáveis pode desencadear uma tempestade química que se assemelha de perto ao que ocorre durante exacerbações de DPOC. Ao mapear centenas de proteínas que aumentam ou diminuem durante essa resposta, os pesquisadores obtêm um quadro detalhado de quais sinais e vias podem ser mais importantes de serem alvo. Como o modelo é seguro, repetível e já é usado em ensaios iniciais de fármacos, ele oferece um campo de testes poderoso para novas medicações anti‑inflamatórias e para identificar biomarcadores mais precisos que, um dia, possam ajudar médicos a prever, detectar e tratar melhor o agravamento súbito da doença pulmonar crônica.
Citação: Gress, C., Müller, M. & Hohlfeld, J.M. Proteomic profiling of bronchoalveolar lavage following human segmental endotoxin challenge—a potential exacerbation model. Sci Rep 16, 6145 (2026). https://doi.org/10.1038/s41598-026-39528-x
Palavras-chave: inflamação pulmonar, exacerbação de DPOC, lavagem broncoalveolar, desafio com endotoxina, proteômica