Clear Sky Science · pt
Modelagem estrutural e análise de docking de mutações missense canônicas e novas associadas à resistência em Escherichia coli sudanesa
Por que isso importa para a saúde do dia a dia
Infecções resistentes a antibióticos deixaram de ser curiosidades médicas raras; elas ameaçam cada vez mais tratamentos rotineiros para infecções do trato urinário, procedimentos cirúrgicos e cuidados intensivos. Este estudo examina de perto bactérias Escherichia coli do Sudão e faz uma pergunta bem específica: como pequenas alterações genéticas em proteínas bacterianas remodelam a ação de antibióticos comuns? Ao usar modelagem estrutural por computador em vez de experimentos laboratoriais caros, os autores revelam padrões de resistência ocultos que testes padrão e bancos de dados globais podem não detectar — especialmente em ambientes com poucos recursos, onde a resistência cresce mais rapidamente. 
Explorando as ferramentas das bactérias
Os pesquisadores concentraram-se em mutações “missense” — mudanças de uma única letra no DNA que trocam um dos blocos construtores de uma proteína por outro. Eles analisaram genomas completos de 55 isolados de E. coli coletados no Sudão e focalizaram proteínas bacterianas que são alvos diretos de grandes classes de antibióticos, incluindo fluoroquinolonas, macrolídeos e rifampicina. Esses alvos incluem enzimas que giram o DNA (giroase e topoisomerase IV), o ribossomo que fabrica proteínas e a enzima RNA polimerase. Das 71 mutações encontradas nessas proteínas, 19 foram sinalizadas por múltiplas ferramentas preditivas como provavelmente prejudiciais à função proteica e, de maneira notável, a maioria dessas parecia ser variações inéditas ainda não catalogadas em bancos de dados globais de resistência.
Novos pontos críticos em alvos conhecidos
Algumas das mudanças mais importantes concentraram-se em uma proteína ribossomal chamada L22, que ajuda a formar o túnel por onde as proteínas recém-sintetizadas saem do ribossomo. Essa região também funciona como sítio de ancoragem para antibióticos macrolídeos, como a eritromicina. O estudo identificou um conjunto denso de mutações em L22 previamente não relatadas, muitas dentro de uma única linhagem, que se situam ao longo desse túnel e em pontos de contato com o RNA ribossomal. Análises computacionais sugeriram que várias dessas alterações desestabilizam a estrutura local ou a tornam mais flexível, potencialmente remodelando o túnel para que moléculas de macrolídeo se encaixem menos firmemente. Ao mesmo tempo, mutações de resistência mais familiares — as “canônicas” — apareceram em proteínas de processamento do DNA, ParC e ParE, e na RNA polimerase, confirmando que cepas sudanesas compartilham alguns sinais globais de resistência enquanto também abrigam variações locais próprias.
Como mudanças na forma enfraquecem a aderência do antibiótico
A equipe foi além de listas de sequências e investigou como essas mutações podem alterar o encaixe tridimensional entre antibióticos e seus alvos. Usando simulações de docking molecular, compararam como diferentes fármacos se ligavam a proteínas normais e mutadas. Para a topoisomerase IV ParC, mutações-chave próximas ao sítio de contato com o fármaco reduziram substancialmente a ligação prevista da fluoroquinolona trovafloxacino, refletindo uma aderência mais frouxa na junção enzima–DNA–droga. Na proteína ParE relacionada, as mutações reduziram modestamente a ligação da novobiocina. Em contraste, uma mutação nova na giroase GyrA pareceu desestabilizar a estrutura da enzima sem alterar de forma perceptível a afinidade com que a fluoroquinolona moxifloxacino se ligava, sugerindo que a resistência às vezes pode surgir por meio da perturbação sutil do desempenho enzimático em vez de apenas pela expulsão direta do fármaco. 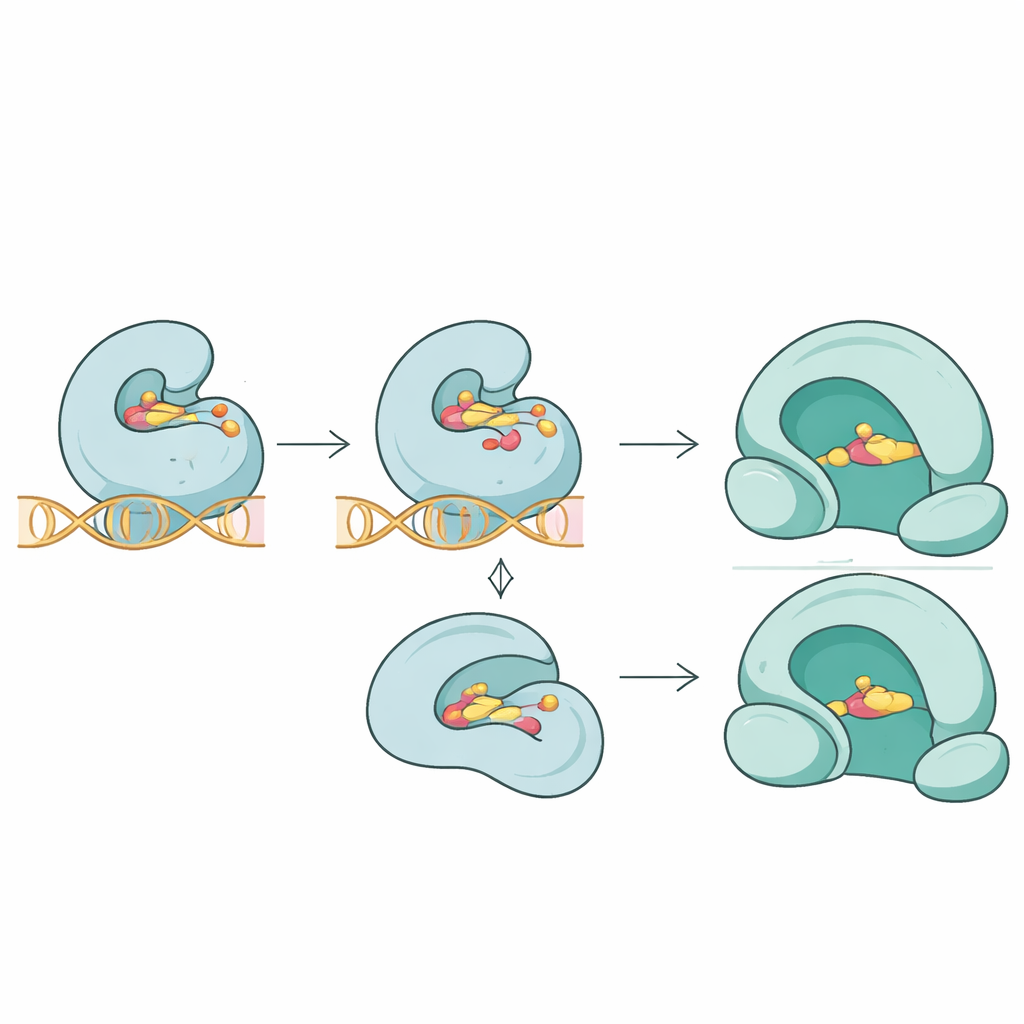
Efeitos mistos em diferentes drogas
Nem todas as mutações tiveram o mesmo impacto. Mudanças clássicas associadas à resistência à rifampicina na proteína RNA polimerase RpoB pouco alteraram a ligação de um inibidor mais recente e estruturalmente distinto que atua em um sítio próximo, sugerindo que fármacos futuros poderiam ser projetados para contornar padrões de resistência existentes. Para a proteína ribossomal L22, estudos de docking com eritromicina revelaram um quadro variado: algumas mutações enfraqueceram a ligação, outras tiveram pouco efeito, e uma até melhorou ligeiramente o encaixe previsto. Esses resultados enfatizam que a resistência raramente é tudo-ou-nada; em vez disso, cada mutação ajusta a estabilidade proteica, a flexibilidade e a ligação ao fármaco em direções diferentes, e o efeito geral no tratamento depende de como essas mudanças se combinam dentro de uma célula bacteriana viva.
O que isso significa para pacientes e vigilância
Do ponto de vista leigo, a mensagem-chave é que bactérias em lugares como o Sudão estão evoluindo resistência por rotas conhecidas e por rotas menos estudadas. As rotas bem conhecidas envolvem mutações clássicas já monitoradas por programas internacionais, mas este estudo mostra que muitas mutações adicionais, enriquecidas localmente, também podem enfraquecer antibióticos de maneiras mais sutis. Ao mapear essas mudanças em estruturas proteicas detalhadas, os autores oferecem uma lista curta de mutações que devem ser testadas em laboratório e consideradas em painéis diagnósticos regionais. Na prática, o trabalho defende que modelagem computacional inteligente pode ajudar países com capacidade laboratorial limitada a monitorar melhor a emergência de resistência, apoiando escolhas terapêuticas mais confiáveis e inspirando o desenho de fármacos que se mantenham um passo à frente da evolução bacteriana.
Citação: Sage, E.E., Ibrahim, S.A.E., Firdaus-Raih, M. et al. Structural modeling and docking analysis of canonical and novel resistance-associated missense mutations in Sudanese Escherichia coli. Sci Rep 16, 8995 (2026). https://doi.org/10.1038/s41598-026-39491-7
Palavras-chave: resistência antimicrobiana, Escherichia coli, mutações missense, bioinformática estrutural, Sudão