Clear Sky Science · pt
Integrar aprendizagem profunda com modelagem baseada em física possibilita previsão de alta precisão da interface anticorpo-antígeno
Por que isso importa para medicamentos do futuro
Anticorpos são os mísseis guiados do nosso sistema imunológico e de muitos fármacos modernos. Para projetar anticorpos melhores, os cientistas precisam saber exatamente como um anticorpo segura sua molécula-alvo, o antígeno. Medir essas estruturas experimentalmente é lento e caro. Este estudo mostra como combinar aprendizagem profunda com modelagem clássica no estilo físico pode melhorar de forma acentuada as previsões computacionais de onde um anticorpo e um antígeno se tocam, potencialmente acelerando o projeto e a triagem de anticorpos.
Encontrando a zona do aperto de mão
Anticorpos reconhecem seus alvos usando pequenos laços flexíveis em suas pontas, chamados regiões de ligação, que se reúnem para formar um patch de contato. Esses laços podem dobrar e torcer, e a zona correspondente no antígeno costuma ser espalhada e rasa em vez de formar um bolso profundo. Essa flexibilidade e sutileza tornam o problema de docking — descobrir como as duas formas se encaixam — extremamente difícil para computadores. Programas tradicionais de docking testam muitas posições relativas das duas proteínas e as pontuam usando regras físicas, como atração eletrostática e deslocamento de água, mas sem pistas biológicas frequentemente acabam em combinações incorretas.
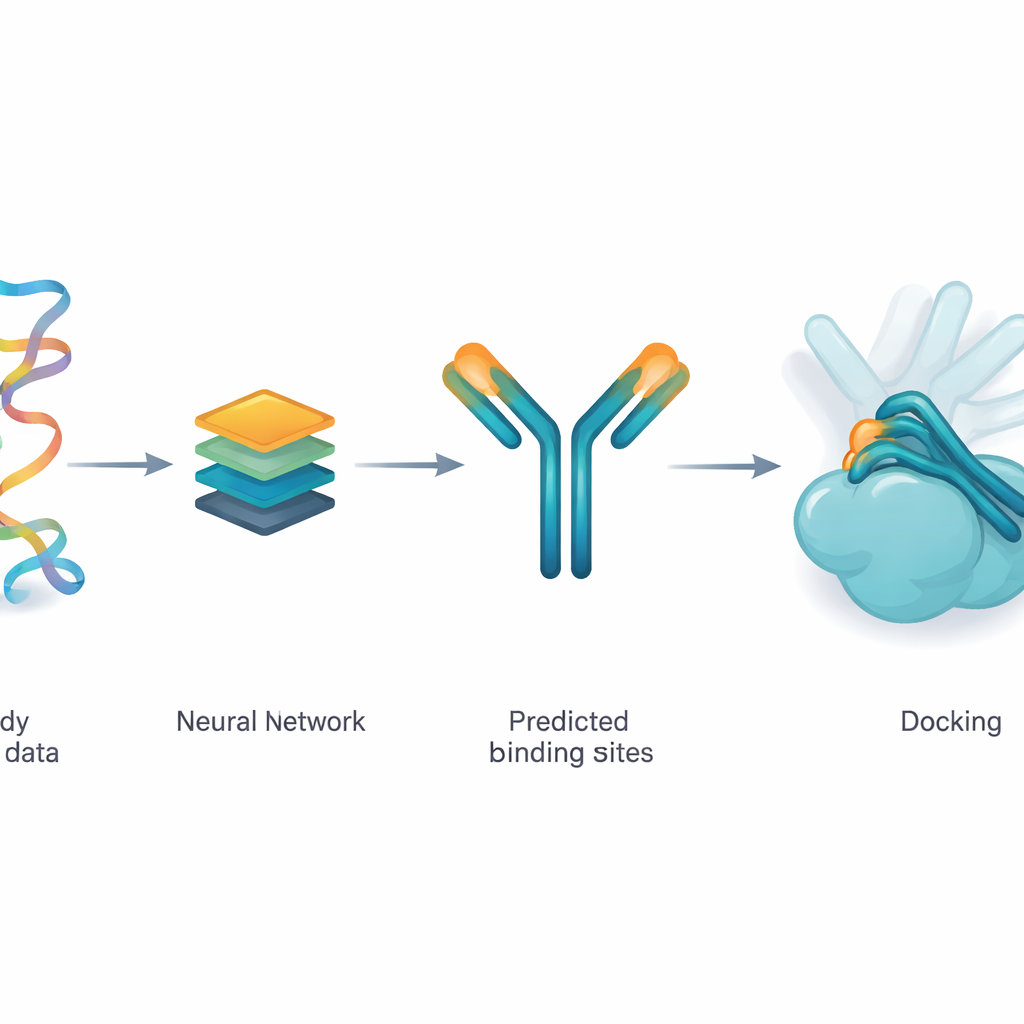
Ensinando uma rede a sugerir pontos de contato prováveis
Os autores usam um modelo de aprendizagem profunda chamado ParaDeep para estimar quais aminoácidos em um anticorpo têm maior probabilidade de tocar o antígeno. O ParaDeep faz isso usando apenas a sequência do anticorpo — a ordem de seus blocos construtores — em vez de precisar de uma estrutura 3D completa. Ele lê as sequências das cadeias pesada e leve em conjunto, codifica suas características químicas e posicionais, e usa mecanismos de atenção para destacar resíduos que parecem bons candidatos à ligação. Cada posição recebe uma pontuação de probabilidade; aquelas acima de um limiar são tratadas como uma zona de contato prevista que pode ser mapeada de volta na estrutura do anticorpo.
Guiando um motor físico em vez de substituí-lo
Em vez de usar aprendizagem profunda para gerar complexos anticorpo–antígeno completos do zero, a equipe insere os resíduos de contato previstos pelo ParaDeep em um motor de docking baseado em física existente chamado PyDockWEB. Esse programa de docking amostra milhares de maneiras possíveis pelas quais o anticorpo e o antígeno poderiam se encontrar e as pontua com uma função de energia. No novo framework, os resíduos de contato previstos atuam como restrições suaves: eles tendem a orientar a busca para que muitas das orientações amostradas aproximem esses resíduos da superfície do antígeno. Importante: a pontuação física subjacente e o tratamento de corpos rígidos das proteínas permanecem inalterados, tornando o processo transparente e relativamente leve para executar.
Quanto as previsões melhoraram?
Os pesquisadores testaram sua abordagem híbrida em 50 complexos anticorpo–antígeno conhecidos de um banco de dados curado. Para cada caso, compararam o docking “às cegas” padrão com o docking guiado pelas restrições do ParaDeep. Eles mediram a precisão local da interface (quão de perto a região de contato prevista correspondia à realidade), similaridade de forma global e uma pontuação de qualidade combinada amplamente usada para avaliar modelos de docking. Nesse conjunto, o método guiado reduziu muito os erros no sítio de ligação, aproximou as estruturas previstas dos complexos verdadeiros e moveu muitas previsões de claramente erradas para categorias de qualidade média ou alta. Quase metade dos modelos guiados ficou na faixa de alta qualidade, contra cerca de um quarto para o docking cego.
O que torna alguns encaixes mais fáceis que outros
A equipe também investigou por que alguns complexos se beneficiaram mais do que outros. Constatou-se que simplesmente prever mais resíduos de contato não garantia sucesso; o que importava era colocar as restrições na área certa, não a quantidade. Interfaces mais hidrofílicas e com mais segmentos flexíveis em coil tenderam a fazer um docking melhor, provavelmente porque casam bem com a ênfase do PyDockWEB em eletrostática e são mais fáceis de alinhar sem grandes mudanças de forma. Quando os pesquisadores repetiram alguns casos fracassados usando informações de contato “oráculo” extraídas diretamente de estruturas experimentais, a maioria desses casos melhorou, confirmando que a localização precisa do patch de contato é um ingrediente chave — mas o docking de corpos rígidos ainda tem limites quando são necessários grandes ajustes conformacionais.
O que isso significa daqui para frente
Em termos práticos, este trabalho mostra que dar a um programa de docking baseado em física uma pista inteligente sobre onde um anticorpo provavelmente agarrará seu alvo pode melhorar muito sua mira, sem transformar o processo em uma caixa-preta opaca. O pipeline combinado ParaDeep–PyDockWEB não substitui métodos flexíveis ou gerativos mais avançados, mas oferece uma maneira prática de usar sinais de aprendizagem profunda ao nível de sequência para guiar ferramentas de docking familiares e interpretáveis. À medida que esforços de descoberta e engenharia de anticorpos geram bibliotecas de sequência cada vez maiores, tais abordagens híbridas podem ajudar os pesquisadores a filtrar rapidamente candidatos que sejam estruturalmente consistentes com um alvo desejado, tornando o caminho da sequência para um anticorpo funcional mais rápido e mais bem informado.
Citação: Kodchakorn, K., Udomwong, P., Pamonsupornwichit, T. et al. Integrating deep learning with physics based modeling enables high precision antibody antigen interface prediction. Sci Rep 16, 8134 (2026). https://doi.org/10.1038/s41598-026-39466-8
Palavras-chave: encaixe de anticorpo, aprendizagem profunda, previsão de parátopo, interações proteína–proteína, design de anticorpos