Clear Sky Science · pt
Impacto da quimioterapia neoadjuvante na funcionalidade de células estromais mesenquimais derivadas do tecido adiposo e seus efeitos de modulação em fibroblastos de pacientes oncológicos
Por que isso importa para os sobreviventes de câncer
Muitas pessoas que passam por tratamento contra o câncer apresentam posteriormente feridas de cicatrização lenta e complicações pós‑operatórias. Ao mesmo tempo, os médicos investigam cada vez mais formas de usar as próprias células reparadoras derivadas da gordura do paciente para ajudar a recuperar os tecidos. Este estudo aborda uma questão prática e urgente: após a quimioterapia, essas células reparadoras ainda são adequadas para uso e, se não, quais células são mais afetadas?
Os ajudantes ocultos de reparo do corpo
Nosso tecido adiposo é mais do que um depósito de energia. Ele abriga uma população rica de células reparadoras versáteis chamadas células estromais mesenquimais derivadas do tecido adiposo, ou AD‑MSCs. Essas células não ficam inativas; elas liberam um coquetel de moléculas sinalizadoras que podem reduzir a inflamação, estimular a formação de novos vasos sanguíneos e encorajar células próximas a crescer e reconstruir tecidos danificados. Logo acima da gordura, na pele, vivem os fibroblastos — células operárias que migram para as feridas e depositam colágeno, a matriz protéica que confere resistência ao tecido novo. Juntas, AD‑MSCs e fibroblastos ajudam a determinar quão bem a pele se recupera após uma lesão ou cirurgia.
Testando as células reparadoras da gordura antes e depois do tratamento
Os pesquisadores coletaram pequenas amostras de pele e gordura de 66 pacientes submetidos à cirurgia, alguns dos quais haviam recebido quimioterapia previamente e outros não. Da gordura, isolaram AD‑MSCs e confirmaram que essas células ainda apresentavam a aparência e o comportamento típicos de células reparadoras: exibiam os marcadores de superfície esperados e podiam se diferenciar em células com características de osso, cartilagem e gordura em laboratório. Da pele, isolaram fibroblastos. A equipe então comparou como AD‑MSCs e fibroblastos de pacientes expostos e não expostos à quimioterapia cresciam, passavam pelo ciclo celular, liberavam moléculas sinalizadoras e expressavam genes ligados à cicatrização e regeneração.
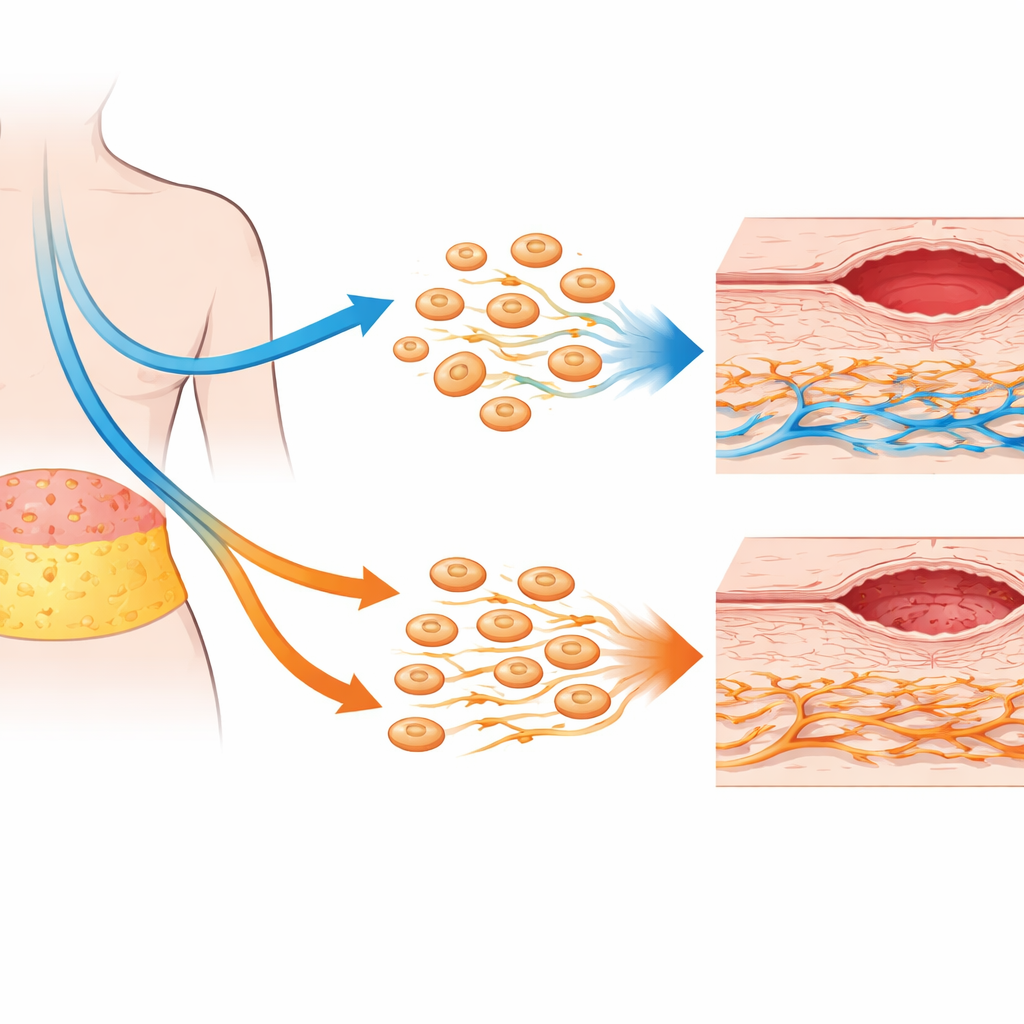
As células reparadoras da gordura permanecem surpreendentemente robustas
Contrariando preocupações de que a quimioterapia pudesse reduzir o potencial das AD‑MSCs, o estudo constatou que essas células derivadas da gordura foram notavelmente resilientes. Seus marcadores de identidade básicos, padrão de crescimento e perfil de proteínas secretadas permaneceram em grande parte inalterados pela quimioterapia prévia. A atividade gênica associada ao crescimento, autorrenovação e reparo das feridas mostrou apenas pequenas variações sem significado relevante. De fato, AD‑MSCs de pacientes tratados com quimioterapia exibiram atividade mitocondrial ligeiramente maior, sugerindo um metabolismo mais ativo em vez de dano. Em experimentos de cocultura — onde AD‑MSCs e fibroblastos compartilhavam o mesmo meio, sem contato direto — as AD‑MSCs ainda estimularam certos comportamentos dos fibroblastos, como movimento direcionado em resposta a sinais de reparo, especialmente em amostras de pacientes que não haviam recebido quimioterapia.
Os construtores da pele suportam o impacto da quimioterapia
O quadro foi muito diferente para os fibroblastos. Células extraídas da pele de pacientes tratados com quimioterapia mostraram sinais claros de vigor biológico reduzido. Sua capacidade de migrar para uma “ferida” simulada por um risco em uma placa de cultura foi significativamente prejudicada, e sua produção de colágeno tendia a ser menor. O perfil de moléculas sinalizadoras que liberavam mudou para um padrão mais inflamatório e menos regenerativo, e muitos genes associados a sinais de crescimento, seus receptores e potencial regenerativo estavam suprimidos. Mesmo quando esses fibroblastos foram cocultivados com suas próprias AD‑MSCs, a maioria de suas funções — movimento, produção de colágeno e atividade gênica benéfica — permaneceu atenuada em comparação com fibroblastos de pacientes que não haviam sido submetidos à quimioterapia.
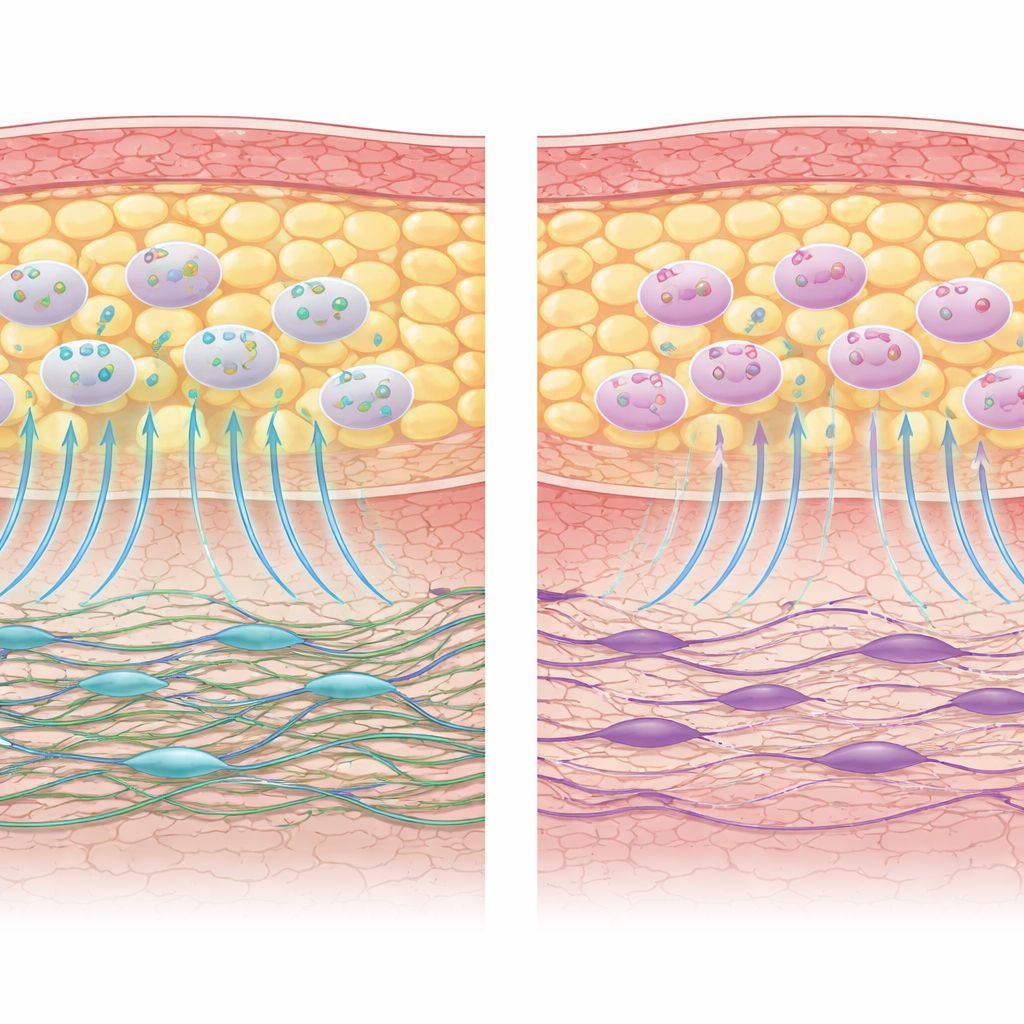
O que isso significa para terapias de cicatrização futuras
Para leigos, a mensagem deste trabalho é que a quimioterapia não parece destruir o banco de células reparadoras derivadas da gordura do corpo, mas deixa os construtores de linha de frente da pele — os fibroblastos — menos capazes de migrar rapidamente para feridas e reconstruir tecido resistente. Como as AD‑MSCs permanecem funcionalmente intactas, elas continuam sendo candidatas promissoras para uso em procedimentos reconstrutivos, cuidados com feridas e enxertos de gordura após o tratamento do câncer. No entanto, o estado prejudicado dos fibroblastos pode limitar o quanto essas células semelhantes a tronco conseguem beneficiar o reparo por si só. Os autores sugerem que terapias futuras podem precisar apoiar ambos os lados da parceria reparadora: preservar ou restaurar a saúde dos fibroblastos enquanto se aproveitam AD‑MSCs robustas, idealmente em modelos mais complexos e semelhantes ao corpo que capturem melhor o ambiente real de cicatrização em sobreviventes de câncer.
Citação: Skoniecka, A., Słonimska, P., Tymińska, A. et al. Impact of neoadjuvant chemotherapy on the functionality of adipose-derived mesenchymal stromal cells and their modulatory effects on fibroblasts in oncology patients. Sci Rep 16, 8614 (2026). https://doi.org/10.1038/s41598-026-39457-9
Palavras-chave: quimioterapia, cicatrização, células-tronco derivadas da gordura, fibroblastos, medicina regenerativa