Clear Sky Science · pt
Descoberta de compostos antivirais potenciais e aceleração da descoberta terapêutica contra o vírus da varíola dos macacos
Por que esta pesquisa importa agora
A varíola dos macacos, hoje frequentemente chamada mpox, passou de uma infecção tropical rara para uma preocupação global, com surtos relatados em vários continentes nos últimos anos. Ao contrário da COVID-19, ainda não existe um medicamento feito especificamente para deter esse vírus. Este estudo usa ferramentas computacionais avançadas para buscar novas pequenas moléculas que possam desarmar o vírus onde ele mais prejudica: sua capacidade de se esconder do nosso sistema imunológico. Se confirmados em laboratório, esses compostos candidatos poderão se tornar o ponto de partida para uma nova classe de medicamentos antivirais.
Como o vírus se esconde das nossas defesas
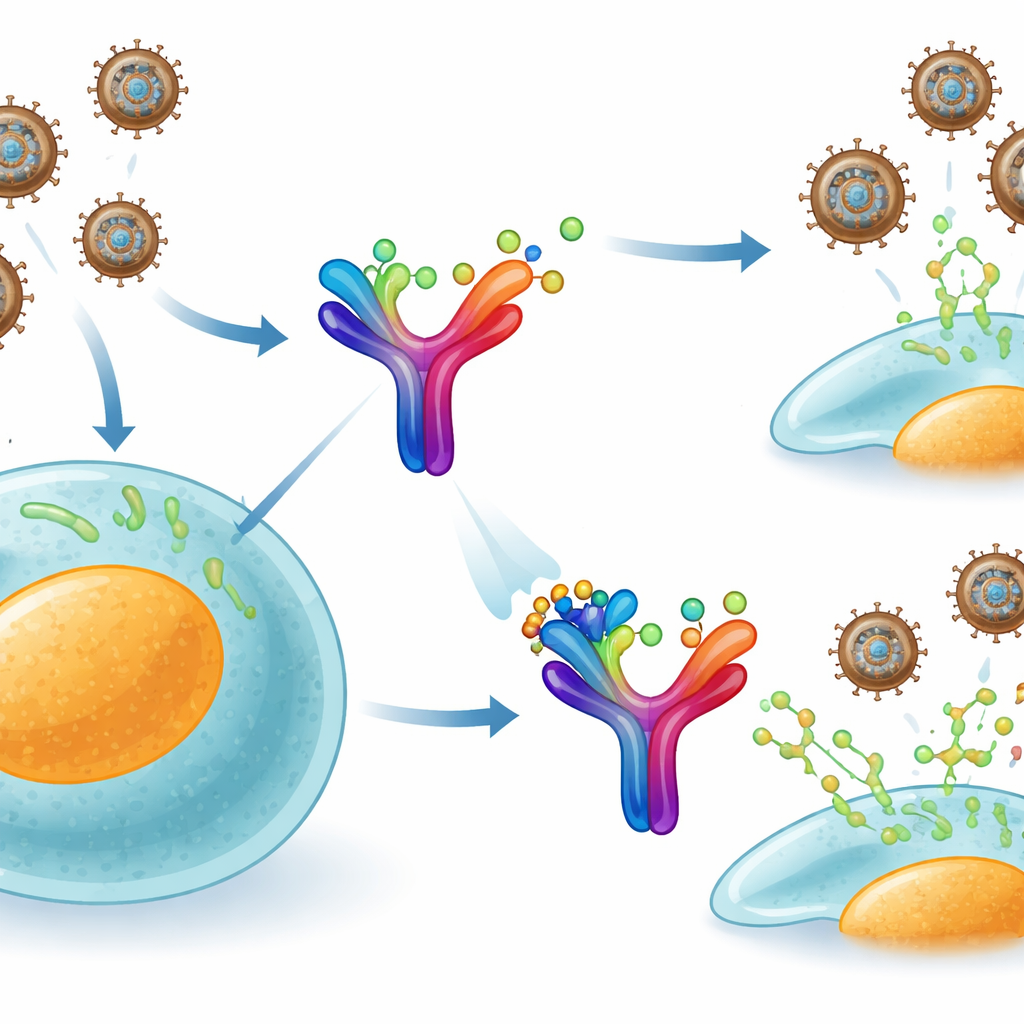
A varíola dos macacos pertence à mesma família mais ampla da varíola, e usa um truque engenhoso para escapar do sistema imune. Nossas células liberam uma proteína sinalizadora chamada interferon-gama, que normalmente alerta as células vizinhas e ativa defesas antivirais. O vírus, porém, produz sua própria proteína secretada, chamada B8R, que flutua fora das células infectadas. A B8R imita de forma muito próxima o nosso próprio receptor de interferon-gama e captura esses sinais imunes antes que alcancem seu alvo verdadeiro. Na prática, ela age como uma esponja, absorvendo as mensagens de alarme do corpo e impedindo uma resposta antiviral completa.
Usando computadores para desenhar tratamentos mais inteligentes
A descoberta tradicional de fármacos pode levar muitos anos e recursos enormes. Aqui, os pesquisadores recorrem ao desenho de fármacos assistido por computador para acelerar o processo. Como não existe uma estrutura 3D experimental da proteína B8R, eles primeiro usaram ferramentas baseadas em AlphaFold para prever sua forma atômica e verificaram cuidadosamente a qualidade desse modelo. Com uma estrutura 3D confiável em mãos, fizeram uma triagem virtual de uma biblioteca química de 5.000 pequenas moléculas. Regras que descrevem o que normalmente torna um composto parecido com um fármaco oral (como tamanho, forma e solubilidade) foram usadas para filtrar candidatos ruins, deixando 2.890 compostos promissores para testes detalhados contra o modelo da proteína B8R.
Encontrando uma “chave” química promissora
O passo seguinte foi ver quais moléculas poderiam se encaixar confortavelmente em um bolso importante na superfície da B8R, onde ela normalmente interage com o interferon-gama. A equipe usou docking molecular, uma técnica que testa bilhões de poses possíveis para uma molécula no bolso da proteína e pontua quão firmemente ela se ligaria. Três candidatos principais emergiram, cada um previsto para formar interações fortes com aminoácidos-chave no bolso. Um composto em particular mostrou a maior energia de ligação e fez vários contatos estabilizadores com resíduos críticos que ajudam a ancorá‑lo no lugar, sugerindo que pode ser especialmente eficaz em bloquear a atividade da B8R.
Observando as moléculas em movimento ao longo do tempo
Proteínas e moléculas de fármacos não são rígidas; elas se movem, flexionam e “respiram” em um ambiente aquoso. Para capturar isso, os pesquisadores realizaram longas simulações de dinâmica molecular — filmes virtuais com duração de centenas de nanosegundos — para ver como cada par proteína–composto se comportava ao longo do tempo. Essas simulações revelaram que o composto de melhor desempenho permaneceu profundamente enterrado no bolso da B8R, com a proteína ajustando-se levemente ao redor dele enquanto se mantinha estruturalmente estável. Em contraste, os outros dois compostos vagaram mais, deslocaram-se para bolsos alternativos ou mostraram flutuações maiores, sugerindo ligações mais fracas ou menos confiáveis. Análises adicionais de flexibilidade, energia e movimentos em larga escala apontaram para o mesmo vencedor: um composto que consistentemente produziu o complexo mais estável e energeticamente favorável.
O que isso pode significar para tratamentos futuros
O estudo não afirma ter descoberto um medicamento pronto, e nenhum experimento em células ou animais foi realizado até o momento. Em vez disso, fornece um ponto de partida robusto e baseado em dados: uma molécula pequena específica que parece idealmente moldada para se encaixar na proteína B8R da varíola dos macacos e potencialmente restaurar o sistema de alarme de interferon do corpo. Ao visar a estratégia de evasão imune do vírus em vez de sua maquinaria de replicação, essa abordagem oferece um ângulo novo para a terapia antiviral. Os autores defendem que seu composto líder agora deve ser testado em laboratório, onde sua capacidade de bloquear a B8R e reduzir a infecção por mpox pode ser medida diretamente. Se esses testes tiverem sucesso, isso pode abrir caminho para um tratamento direcionado que ajude o sistema imunológico a ver e impedir o vírus com mais eficácia.
Citação: Ahmad, F., Navid, A., Irfan, M. et al. Discovery of potential antiviral compounds and accelerating the therapeutic discovery against monkeypox virus. Sci Rep 16, 8306 (2026). https://doi.org/10.1038/s41598-026-39427-1
Palavras-chave: antiviral varíola dos macacos, evasão imune, descoberta de fármacos, modelagem computacional, sinalização de interferon