Clear Sky Science · pt
Otimização de monócitos THP-1-CAR utilizando sinalização CD32a de fagocitose para ativação de células T específica de antígeno
Ensinando Novos Truques ao Sistema Imune
As terapias celulares modernas já reprogramam células do sistema imune para caçar o câncer, mas a maioria depende de células T, que podem ter dificuldades no ambiente hostil dos tumores sólidos. Este estudo volta-se, em vez disso, para outro defensor poderoso — os macrófagos, os “comedores” profissionais do corpo — e investiga como reconfigurá‑los para que não apenas engulam células ou vírus nocivos de forma mais eficiente, mas também recrutem células T para um ataque mais duradouro e direcionado. O trabalho revela regras de projeto para construir macrófagos com receptor quimérico de antígeno (CAR) melhores, que poderiam ser aplicadas tanto a infecções como à COVID‑19 quanto a tumores sólidos de difícil tratamento.
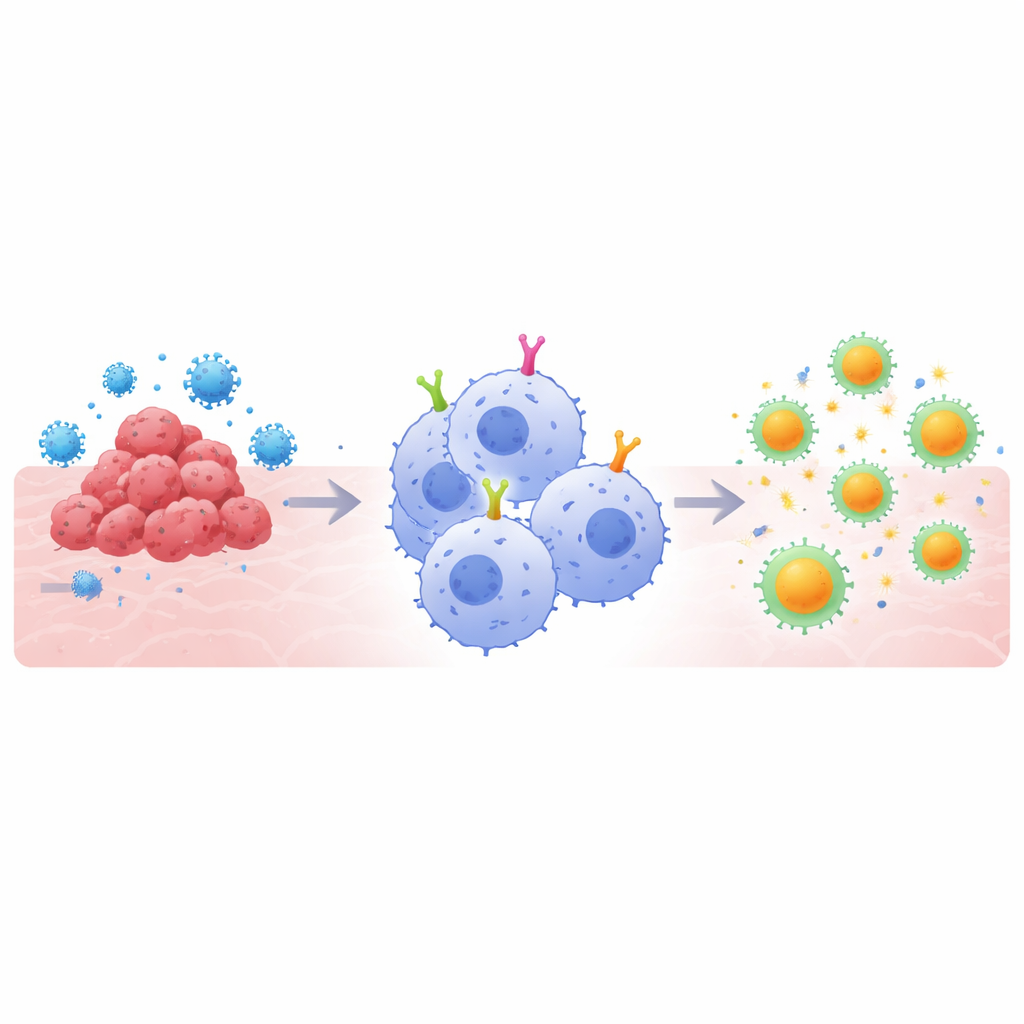
Por que as Células Super‑Comedoras Importam
Terapias baseadas em CAR funcionam equipando células imunes com receptores de superfície feitos sob medida que reconhecem um alvo escolhido, como uma proteína tumoral ou uma espícula viral. As versões em células T transformaram o tratamento de alguns cânceres hematológicos, mas enfrentam obstáculos contra tumores sólidos e em certas infecções. Os macrófagos oferecem uma abordagem diferente: eles naturalmente engolem ameaças e as fragmentam para serem apresentadas às células T, conectando os braços “inato” e “adaptativo” da imunidade. No entanto, a maioria dos projetos de CAR foi originalmente construída para células T, não para macrófagos. Os autores raciocinaram que, para explorar plenamente as forças dos macrófagos, as partes de sinalização internas dos CAR — os segmentos que dizem à célula o que fazer uma vez que um alvo é ligado — precisariam ser ajustadas especificamente para essas células comedoras.
Encontrando a Melhor Fiação Interna
A equipe comparou sistematicamente vários domínios de sinalização interna dentro de CARs introduzidos em uma linhagem de monócitos humana (THP‑1) que pode ser convertida em macrófagos. Eles se concentraram em domínios originados de receptores que normalmente dirigem a fagocitose e a inflamação: CD3ζ (o módulo clássico de célula T), CD32a (um receptor que se liga a alvos cobertos por anticorpos), componentes do CR3 CD11b e CD18 (receptores chave do complemento) e TLR4 (um sensor de perigo microbiano). Usando esferas e pseudovírus revestidos com a proteína spike do SARS‑CoV‑2, mediram quão bem cada desenho de CAR permitia às células engolir alvos, produzir moléculas inflamatórias e, subsequentemente, ativar células T CD8 humanas que já haviam sido expostas ao vírus. Em seguida, transferiram os desenhos mais promissores para CARs direcionados à mesotelina, uma proteína superexpressa em muitos tumores sólidos, para verificar se as mesmas regras valiam em um contexto tumoral.
Construindo Melhores Comedores e Amplificadores de Sinal
Surgiu um padrão claro: CARs baseados em CD32a conduziram de forma consistente uma fagocitose mais forte e mais rápida do que aqueles usando o domínio convencional CD3ζ, apesar de CD3ζ carregar mais dos motivos típicos de ativação. Em outras palavras, o “encaixe” entre o sinal e a maquinaria do macrófago importou mais do que a mera intensidade do sinal. A adição de peças derivadas do CR3 (CD11b ou CD18) sobre CD32a não aumentou ainda mais a capacidade de engolfar na maioria das condições, mas elevou os níveis de citocinas inflamatórias chave, como TNF‑α e IL‑1β. Combinações contendo TLR4 foram além ao impulsionar sinais inflamatórios e o marcador de superfície CD86, associado à capacidade de estimular células T, embora isso viesse com compromissos: níveis mais baixos de CAR na superfície celular e fagocitose um pouco reduzida.
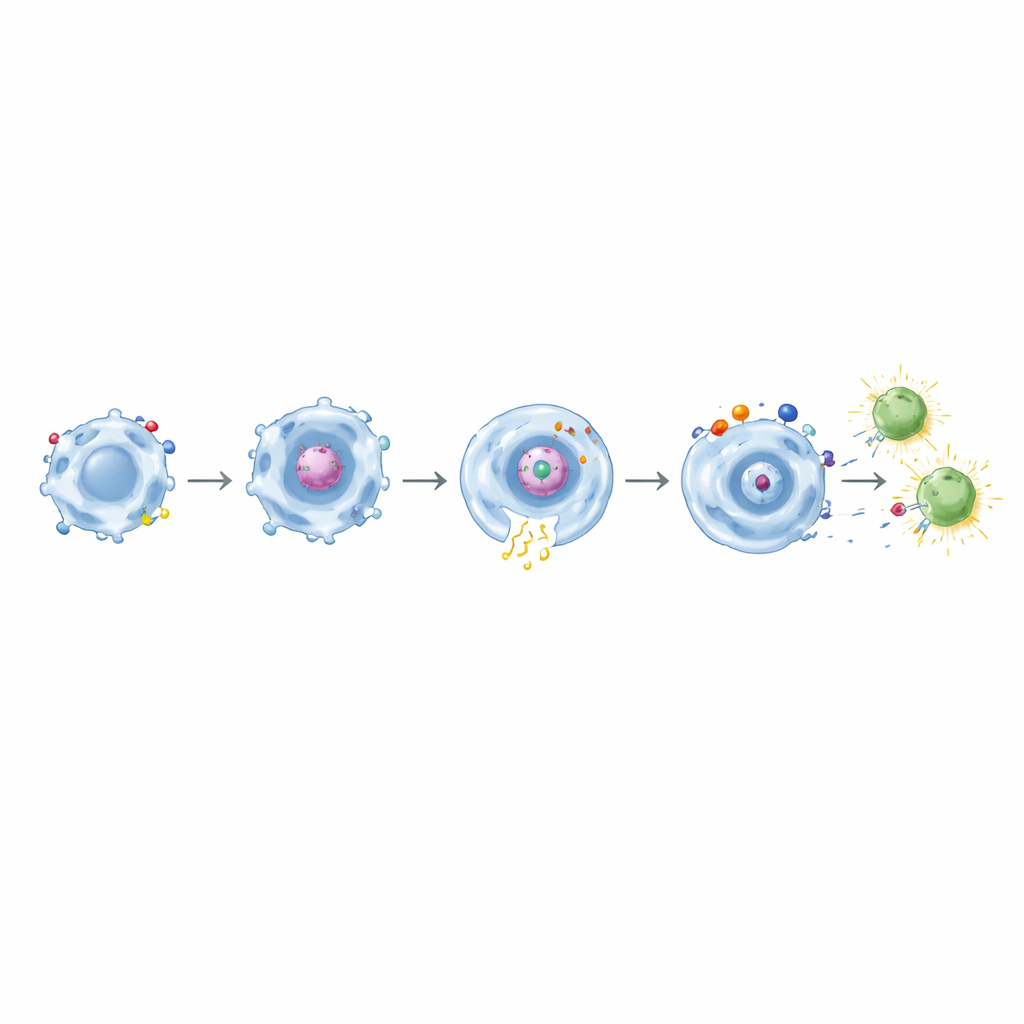
De Comer a Ensinar as Células T
De forma crucial, após macrófagos portando CARs baseados em CD32a engolirem a proteína spike, eles foram capazes de ativar células T CD8 de memória de pessoas previamente vacinadas contra a COVID‑19. Essas células T expressaram marcadores iniciais de ativação e produziram moléculas efetoras como interferon‑γ e TNF‑α. O efeito ficou ainda mais forte com CARs de domínio duplo que emparelhavam CD32a com CD11b, CD18 ou TLR4. Quando desenhos semelhantes direcionados à mesotelina foram testados contra células tumorais geneticamente modificadas, eles novamente mostraram fagocitose precisa e dependente do alvo combinada com sinalização inflamatória aumentada. Entre esses, a combinação CD32a+TLR4 destacou‑se como um poderoso “alarme tecidual”, elevando de forma mais eficaz a secreção de citocinas e CD86 enquanto ainda mantinha a fagocitose tumoral específica.
O Que Isso Pode Significar para Tratamentos Futuros
Para um observador leigo, este estudo mostra que projetar macrófagos não é um problema de tamanho único. Ao trocar e combinar módulos de sinalização interna, os cientistas podem moldar células que ou se concentram na limpeza eficiente de células doentes ou atuam mais como amplificadores imunes que remodelam o ambiente supressor do tumor e recrutam células T. CARs baseados em CD32a emergiram como uma base robusta para tais projetos, superando módulos tradicionais de células T em macrófagos e funcionando tanto contra alvos virais quanto tumorais. Embora esses resultados provenham de modelos de laboratório e precisem ser confirmados em células humanas primárias e em animais, eles fornecem um plano para terapias de próxima geração com CAR macrófagos que podem enfrentar melhor tumores sólidos e infecções persistentes ao unir fagocitose rápida com ativação precisa de células T.
Citação: Hong, J., Lee, S., Kim, Y. et al. Optimization of THP-1-CAR monocytes utilizing CD32a signaling phagocytosis for antigen-specific T cell activation. Sci Rep 16, 8175 (2026). https://doi.org/10.1038/s41598-026-39406-6
Palavras-chave: macrófagos CAR, sinalização CD32a, fagocitose, imunoterapia de tumores sólidos, ativação de células T