Clear Sky Science · pt
Um modelo de física de polímeros do núcleo celular em interfase para simulações radiobiológicas
Por que a forma da nossa “casa” do DNA importa
A radiação é uma espada de dois gumes na medicina: pode matar células cancerosas, mas também pode danificar tecidos saudáveis. No cerne tanto dos riscos quanto dos benefícios está o nosso DNA, compactado dentro do núcleo celular. Este artigo mostra como um modelo 3D detalhado, inspirado na física, dessa “cidade do DNA” nuclear pode ajudar cientistas a prever como a radiação provoca quebras e reparos incorretos dos cromossomos, potencialmente melhorando tratamentos contra o câncer e estimativas de risco por radiação no espaço.
Vendo o genoma como uma estrutura viva
Dentro de cada célula humana, dois metros de DNA são dobrados em um minúsculo núcleo de poucos micrômetros de diâmetro. Essa dobra não é aleatória: cada cromossomo tende a ocupar seu próprio território, que por sua vez é dividido em bairros e domínios em laço. Novas ferramentas experimentais, como microscopia de super-resolução e mapas de contato Hi-C, revelaram esse arranjo 3D intrincado em detalhes notáveis. Ainda assim, a maioria dos modelos de radiação continua a tratar o DNA como um emaranhado simplificado de linhas ou laços idealizados, ignorando essa organização de ordem superior. Os autores propuseram construir um modelo de núcleo inteiro que respeite o que os biólogos aprenderam sobre a arquitetura real da cromatina, mantendo-se rápido o suficiente para ser executado em computadores comuns de laboratório.
Construindo um núcleo virtual com física de polímeros
A equipe modelou os cromossomos como cadeias flexíveis, emprestando ideias da física de polímeros, o mesmo campo usado para entender plásticos e materiais macios. Eles dividiram o problema em três estágios de relaxamento para domar o enorme custo computacional. Primeiro, posicionaram grandes blocos estruturais chamados domínios de cromatina por todo o núcleo, permitindo que se repelam, se estendam ao longo de seus comprimentos e se agrupem em subcompartimentos mais amplos. Segundo, aproximaram o zoom dentro de cada domínio para dispor fibras de cromatina mais finas, incluindo regiões em laço mantidas por proteínas de ligação. Terceiro, permitiram que todas as fibras interagissem livremente novamente dentro do limite nuclear para alcançar uma configuração final realista. Ao dividir o processo dessa forma e adicionar busca hierárquica e truques de computação paralela, reduziram o tempo de execução de um impraticável quatro meses para cerca de três horas por núcleo virtual em uma estação de trabalho de 64 núcleos.
De trilhas de radiação a quebras e reparos do DNA
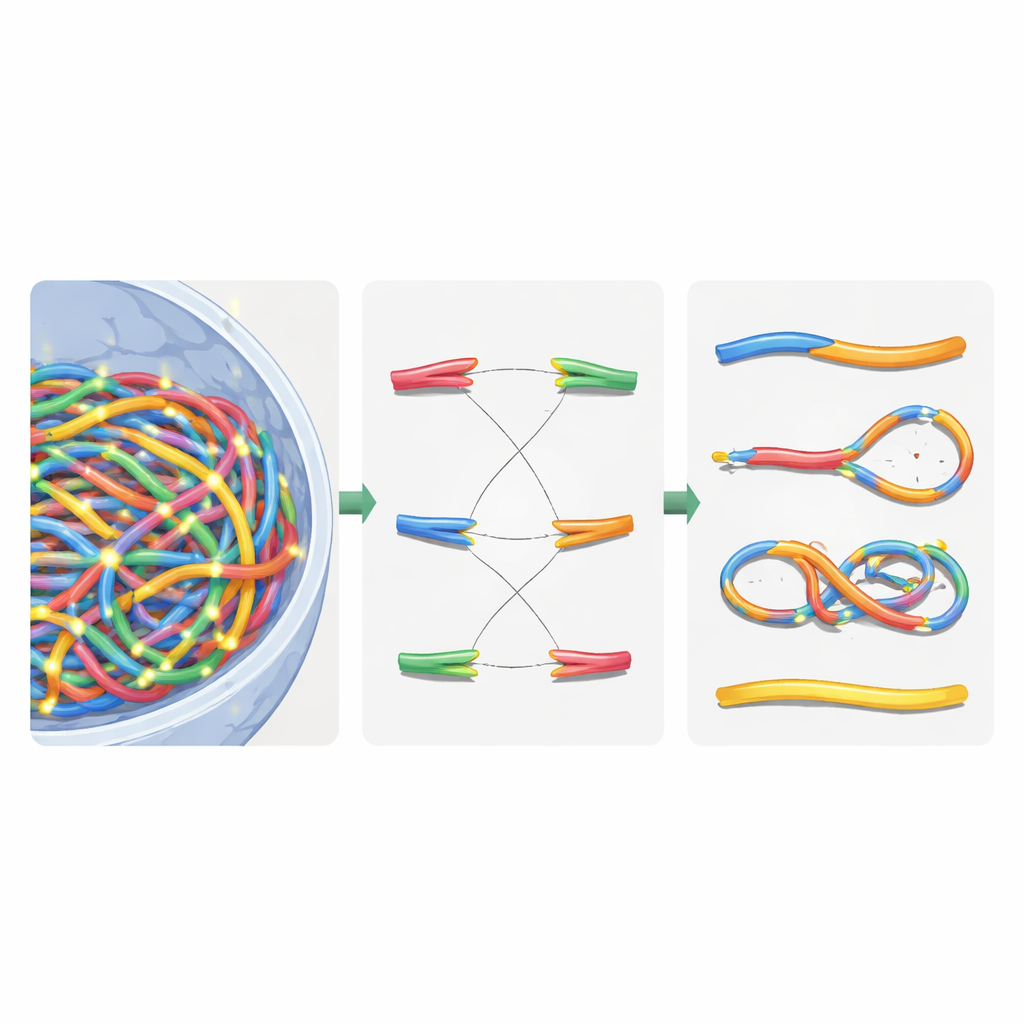
Depois de construir o núcleo virtual, os autores sobrepuseram trilhas de radiação detalhadas geradas por simulações Geant4-DNA. Eles usaram uma busca hierárquica para encontrar, para cada evento de ionização, qual domínio de cromatina, segmento de fibra e finalmente qual nucleotídeo estava mais próximo, sem nunca armazenar as dez bilhões de posições de nucleotídeos na memória. Em vez disso, mantiveram um modelo reutilizável de cromatina e aplicaram transformações de coordenadas inteligentes em tempo real. Ionizações no esqueleto do DNA foram tratadas como quebras de fita, e quebras próximas em fitas opostas viraram quebras de fita dupla. Para imitar a maquinaria de reparo celular, os autores introduziram uma regra de religação com base na distância: extremidades livres de DNA que estejam próximas têm maior probabilidade de se religarem. As decisões de religação foram feitas passo a passo até que todas as extremidades estivessem pareadas ou permanecessem sem reparo, recriando tanto reparos corretos quanto fragmentos religados incorretamente.
Classificando cromossomos quebrados com lógica de rede
Após esse reparo virtual, o núcleo continha uma mistura de cromossomos remontados e fragmentos remanescentes. Para classificar o que havia ocorrido, os autores traduziram o genoma reparado em um grafo não direcionado: segmentos cromossômicos tornaram-se arestas, e suas extremidades e pontos de ruptura tornaram-se nós. Usando um algoritmo padrão de componentes conectados, eles puderam recuperar automaticamente cada novo objeto do tipo cromossomo e contar características-chave como o número de centrômeros (pontos de fixação para a divisão celular) e telômeros (extremidades naturais). A partir disso, identificaram dicêntricos (cromossomos com dois centrômeros), anéis e deleções. Em seguida, compararam suas simulações com experimentos clássicos em células da pele humana expostas a raios gama e partículas alfa, constatando que as aberrações cromossômicas totais foram reproduzidas dentro de cerca de 20% dos valores medidos, uma melhoria substancial em relação a modelos anteriores.
O que isso significa para pacientes e astronautas
De forma simples, este trabalho mostra que “onde” o DNA está no núcleo e “como” ele se dobra influenciam fortemente como os danos por radiação se acumulam em alterações cromossômicas perigosas. Ao combinar arquitetura genômica 3D realista, simulação eficiente baseada em física e leitura baseada em grafos dos cromossomos quebrados, os autores oferecem uma ponte poderosa entre biologia estrutural e radiobiologia. Eles argumentam que refinamentos futuros — como adicionar cronometrias detalhadas de reparo e usar dados de sequenciamento de genoma inteiro — poderiam tornar essa abordagem ainda melhor na previsão do impacto biológico de partículas de alta energia usadas na terapia contra o câncer ou encontradas em viagens espaciais profundas. Em última instância, melhores modelos da “casa” do DNA dentro de nossas células podem ajudar a ajustar tratamentos por radiação mais seguros e eficazes e a aprimorar nossa compreensão dos riscos radiológicos a longo prazo.
Citação: Zhao, M., Huang, G., Xu, Z. et al. A polymer physics model of the interphase cell nucleus for radiobiological simulations. Sci Rep 16, 7913 (2026). https://doi.org/10.1038/s41598-026-39234-8
Palavras-chave: danos ao DNA induzidos por radiação, arquitetura 3D da cromatina, aberrações cromossômicas, modelagem por física de polímeros, terapia com partículas