Clear Sky Science · pt
Deficiência de Dlgap2 perturba a homeostase sináptica ao promover a degradação de Itsn1 mediada por ubiquitina em um modelo com semelhança ao autismo induzido por ácido valproico
Por que um medicamento comum e a conexão neural importam
O ácido valproico é um medicamento usado há muito tempo para epilepsia e transtornos de humor, mas quando tomado durante a gravidez tem sido associado a um risco maior de autismo em crianças. Este estudo aborda uma pergunta premente para famílias e médicos: o que exatamente esse fármaco faz na fiação do cérebro em desenvolvimento? Ao rastrear alterações até moléculas específicas nas sinapses — os pontos de comunicação entre neurônios — os pesquisadores revelam uma nova cadeia de eventos que pode ajudar a explicar comportamentos semelhantes ao autismo e apontar para estratégias terapêuticas futuras. 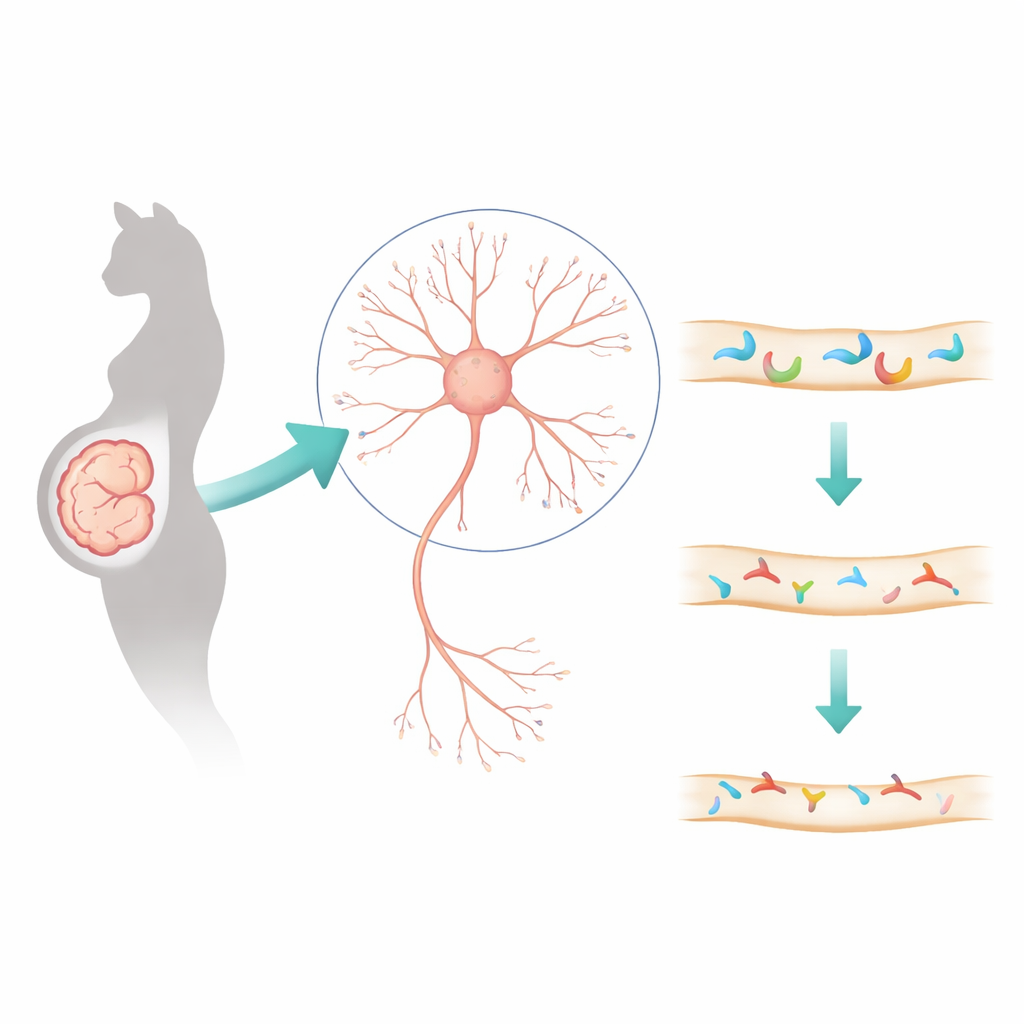
Buscando, entre espécies, pontos vulneráveis compartilhados
Para encontrar pistas confiáveis, a equipe não se baseou em apenas um modelo animal. Compararam cérebros ou tecidos cerebrais semelhantes de organoides corticais humanos, macacos, ratos e camundongos que haviam sido expostos ao ácido valproico antes do nascimento. Usando levantamentos em grande escala de genes e proteínas, identificaram um pequeno conjunto de genes que mudaram em todos esses sistemas e que estavam ligados às sinapses e à mielinização dos axônios. Entre eles, um se destacou: Dlgap2, uma proteína de andaime que ajuda a organizar o lado pós‑sináptico das sinapses excitatórias. Em camundongos expostos ao ácido valproico prenatalmente, os níveis de Dlgap2 caíram no córtex e, mais especificamente, dentro de pequenos compartimentos sinápticos, sugerindo que essa molécula estrutural é uma vítima-chave da exposição ao fármaco.
Das mudanças moleculares às alterações comportamentais
Os autores então perguntaram se a perda de Dlgap2 por si só é suficiente para perturbar a função cerebral. Usaram vírus carregando RNA de fita curta em formato hairpin para reduzir Dlgap2 em neurônios de camundongo em cultura e em camundongos recém‑nascidos. Em cultura, neurônios com Dlgap2 reduzido desenvolveram ramificações mais curtas e tiveram menos pontuações pós‑sinápticas, sinais de conexões enfraquecidas. Em animais vivos, o silenciamento direcionado de Dlgap2 no cérebro produziu comportamentos semelhantes ao autismo: camundongos machos jovens tiveram dificuldade em aprender a localização de uma plataforma oculta em um labirinto aquático e mostraram menor interesse por parceiros sociais e por novidade social em um teste de três câmaras. Essas alterações reproduzem os déficits de aprendizagem e sociais observados em animais expostos ao ácido valproico, fortalecendo a hipótese de que a perda de Dlgap2 não é apenas um efeito colateral, mas um motor das mudanças comportamentais.
Encontrando um parceiro vulnerável na sinapse
Para entender como a perda de Dlgap2 repercute na sinapse, os pesquisadores examinaram mais de perto as proteínas ancoradas na densidade pós‑sináptica, a densa base molecular que recebe sinais químicos. Usando proteômica, descobriram que a redução de Dlgap2 alterou a abundância de centenas de proteínas sinápticas, especialmente aquelas envolvidas na organização das sinapses e na reciclagem de vesículas por endocitose. Uma proteína, Intersectin‑1 (Itsn1), caiu de forma particularmente acentuada. Trabalhos bioquímicos adicionais mostraram que Dlgap2 e Itsn1 residem fisicamente nos mesmos complexos proteicos em frações enriquecidas em sinapses e que ambos aparecem entre genes associados ao autismo. Isso apontou para uma parceria regulatória focalizada entre as duas moléculas dentro de um cenário sináptico muito concorrido. 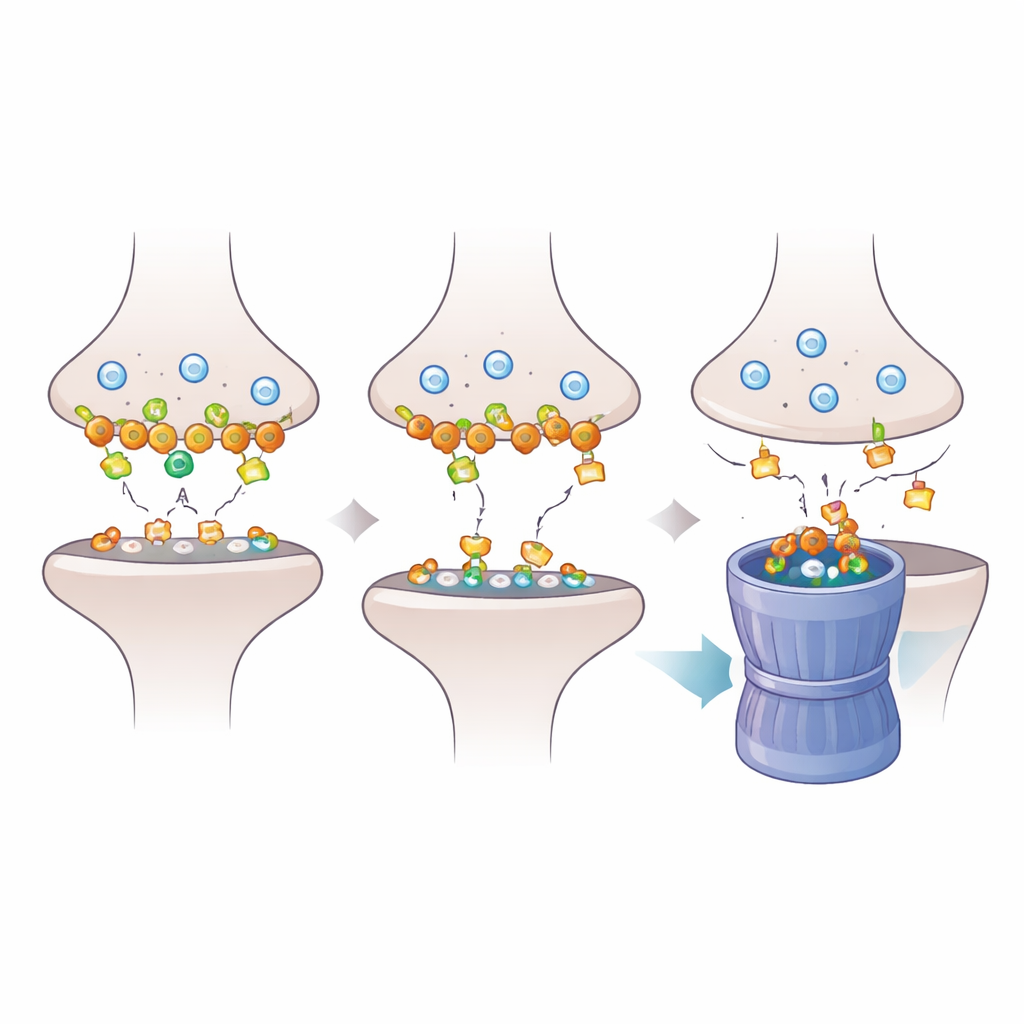
Um caminho oculto de descarte vem à tona
A equipe então investigou por que os níveis de Itsn1 caem quando Dlgap2 está ausente. Observaram que, em compartimentos sinápticos, a redução de Dlgap2 desencadeou uma forma de marcação proteica conhecida como ubiquitinação ligada a K48, que sinaliza proteínas para degradação pelo “triturador” proteassoma da célula. Bloquear esse sistema de descarte com o fármaco MG132 preveniu a perda de Itsn1, indicando que Dlgap2 normalmente protege Itsn1 de ser marcado e destruído. Sem Dlgap2, Itsn1 é cada vez mais marcado, direcionado ao proteassoma e esgotado das sinapses, comprometendo a reciclagem endocítica e o equilíbrio da atividade sináptica. O trabalho sugere que mudanças sutis na velocidade de turnover de proteínas-chave podem desestabilizar sinapses durante o desenvolvimento cerebral.
O que isso significa para o autismo e tratamentos futuros
Em conjunto, o estudo propõe uma ideia simples, porém poderosa, para não especialistas: a exposição pré‑natal ao ácido valproico pode enfraquecer uma proteína estrutural “braçadeira” (Dlgap2) nas sinapses. Quando essa braçadeira se perde, sua parceira (Itsn1) passa a ser alvo excessivo do sistema celular de descarte, levando à reciclagem defeituosa de componentes sinápticos e, em última instância, a circuitos mal conectados e comportamentos semelhantes ao autismo em camundongos. Embora muitos genes e fatores ambientais contribuam para o autismo, esse eixo Dlgap2–Itsn1 oferece uma cadeia molecular concreta desde a exposição pré‑natal a drogas até a função cerebral alterada. A longo prazo, estratégias que preservem essa parceria ou ajustem o maquinário de descarte proteico nas sinapses podem ajudar a proteger cérebros em desenvolvimento de formas semelhantes de perturbação.
Citação: Guo, X., Zhang, L. & Zhuang, K. Dlgap2 deficiency disrupts synaptic homeostasis by promoting ubiquitin-mediated Itsn1 degradation in a valproic acid-induced autism-like model. Sci Rep 16, 8305 (2026). https://doi.org/10.1038/s41598-026-39099-x
Palavras-chave: ácido valproico e gravidez, proteínas de andaime sináptico, mecanismos do espectro do autismo, via do proteassoma ubiquitina, modelos murinos de autismo