Clear Sky Science · pt
O casr do peixe-zebra modula a estrutura e a função cardíaca
Por que os corações de peixes importam para a saúde humana
Nossos corações dependem do cálcio, um mineral simples, para bater corretamente. Quando os sinais de cálcio falham, o resultado pode ser insuficiência cardíaca ou outra doença grave. Este estudo usa pequenos peixes-zebra—peixes de água doce transparentes frequentemente usados em laboratórios—para explorar como um interruptor sensível ao cálcio nas células molda a força e a sobrevivência do coração. Ao desligar um único gene que ajuda as células a detectar o cálcio, os pesquisadores descobriram uma série de problemas na bomba cardíaca, na forma do corpo e até na bexiga natatória cheia de ar do peixe. O trabalho também mostra que o contexto genético mais amplo de um animal pode atenuar ou agravar dramaticamente o impacto de uma mutação nociva, uma lição com claros ecos na medicina humana.
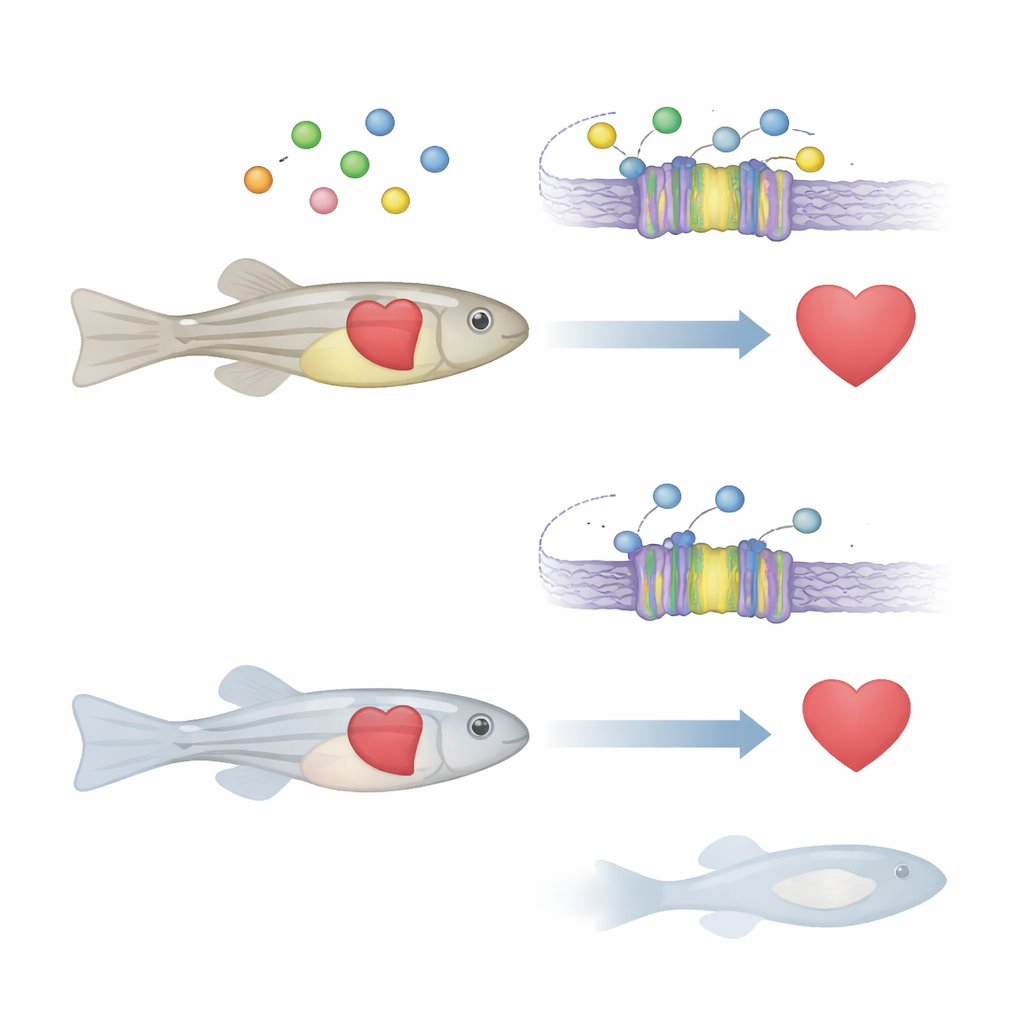
Um “termostato” celular para o cálcio
O cálcio dentro e fora das células age como um sinal universal que controla o movimento muscular, a liberação de hormônios e até quais genes são ativados. Muitos órgãos dependem de uma proteína chamada receptor sensor de cálcio, que funciona como um termostato para os níveis de cálcio. Quando o cálcio extracelular muda, esse receptor ajusta a liberação de hormônios e outros processos para restaurar o equilíbrio. Em pessoas, defeitos nesse receptor já estão ligados a distúrbios ósseos e minerais, e são suspeitos em doenças cardíacas e alguns cânceres. No entanto, exatamente como esse sensor de cálcio influencia o desenvolvimento e a função cardíaca em um organismo inteiro permaneceu incerto.
O que acontece quando o sensor de cálcio é desligado
A equipe concentrou-se na versão desse gene no peixe-zebra, chamada casr, que é fortemente conservada em relação ao homólogo humano. Usando ferramentas modernas de edição genética, eles criaram peixes-zebra nos quais ambas as cópias do casr foram desativadas. A princípio, os peixes jovens pareciam quase normais. Mas aos cinco dias após a fertilização, muitos mutantes não conseguiram inflar a bexiga natatória, um pequeno órgão preenchido por gás que controla a flutuabilidade. Esses peixes afundaram no fundo, nadaram mal, logo desenvolveram curvatura da coluna e todos morreram até duas semanas de idade. Esses sinais externos apontavam para problemas internos sérios afetando mais de um sistema orgânico.
Um coração mais fraco, menor e mais lento
Vídeos em alta velocidade e análise de imagem dos corações batendo revelaram quão profundamente a ausência do sensor de cálcio afetou o desempenho cardíaco. Em larvas de peixe-zebra normais, o ventrículo do coração enche e esvazia em um padrão rítmico e vigoroso. Nos mutantes, o ventrículo era visivelmente menor durante o enchimento, o batimento cardíaco era mais lento e cada batida expelia menos sangue. Medidas de quanto o músculo cardíaco encurta e de quanto a área da câmara de bombeamento varia a cada batida foram ambas reduzidas, indicando contração enfraquecida. O débito cardíaco total—o volume de sangue movido por minuto—caiu acentuadamente. No nível genético, centenas de transcritos mudaram, e redes-chave que controlam o manejo do cálcio e a maquinaria da contração muscular foram reduzidas, ligando a edição do gene tanto à falha molecular quanto mecânica do coração.
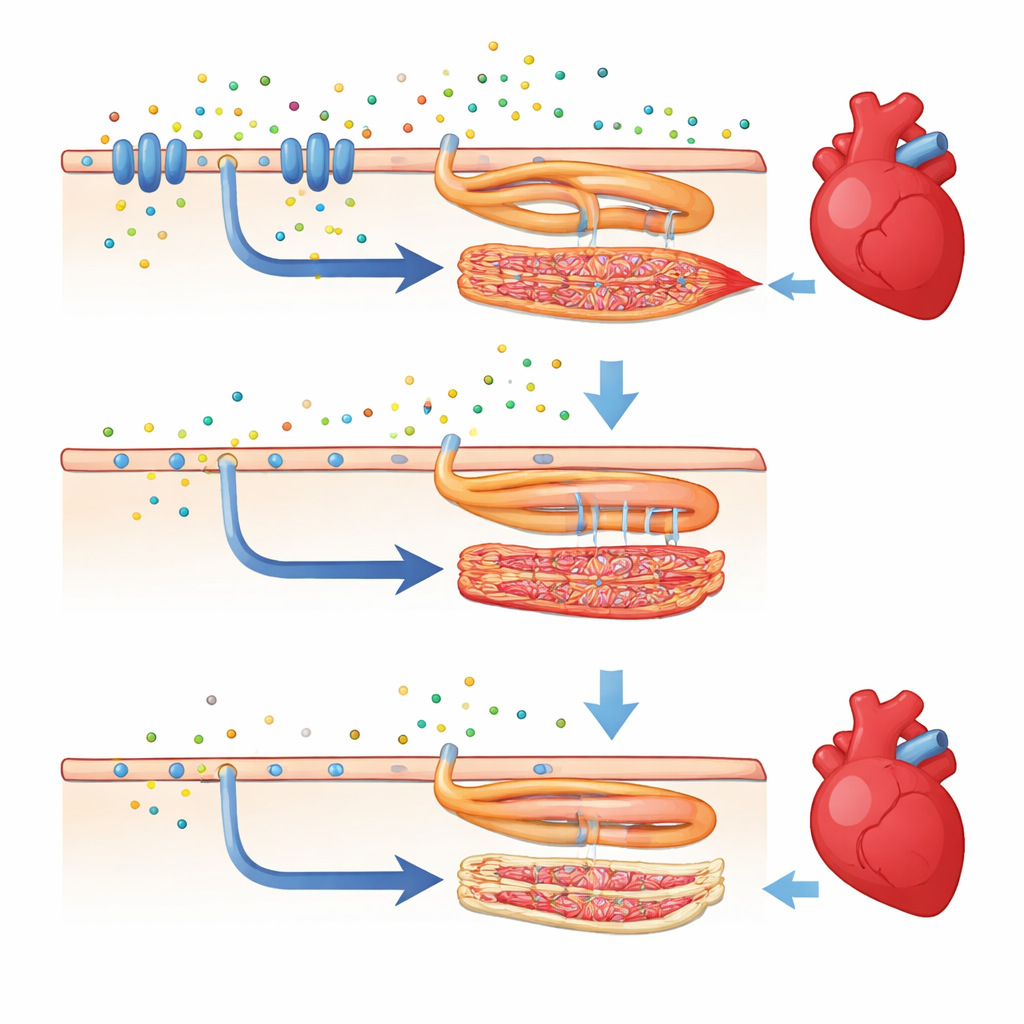
Como genes de fundo podem resgatar um coração doente
Surpreendentemente, a mesma mutação em casr comportou-se de forma muito diferente em outra linhagem comum de peixe-zebra, conhecida como TL (Tupfel long-fin). Quando o nocaute do gene foi transferido para esse novo contexto genético, os peixes conseguiram inflar suas bexigas natatórias, sobreviveram até a idade adulta e exibiram bombeamento cardíaco muito melhor. Seus corações ainda estavam algo comprometidos—a frequência cardíaca permaneceu mais baixa que o normal—mas medidas de quão vigorosamente o ventrículo se contraía e a quantidade de sangue bombeada por minuto quase igualaram as de peixes saudáveis. Nesses animais resgatados, muitos dos genes ligados à sinalização do cálcio e à contração do músculo cardíaco voltaram a níveis intermediários, mais altos do que na linhagem originalmente doente. Isso revela que outros genes espalhados pelo genoma podem amortecer ou intensificar o impacto de uma alteração prejudicial.
Sinais que moldam corações e flutuabilidade
Além do coração, a perda do sensor de cálcio também perturbou grandes sistemas de controle do crescimento no embrião. Genes nas vias de sinalização Wnt e Hedgehog—arquitetos bem conhecidos da formação de órgãos—foram reduzidos nos mutantes. Essas alterações provavelmente contribuem para a falha na inflação da bexiga natatória, que por sua vez pode piorar a sobrevivência ao dificultar a alimentação e a locomoção eficientes dos peixes. Marcadores de diferenciação das células do músculo cardíaco também foram reduzidos, e os ventrículos eram menores, sugerindo que o sensor de cálcio ajuda a orientar como as células do músculo cardíaco crescem e amadurecem.
O que isso significa para entender o risco de doença
Em conjunto, este trabalho mostra que o receptor sensor de cálcio é um guardião crucial tanto da função cardíaca quanto do desenvolvimento adequado de órgãos no peixe-zebra. Quando esse sensor é perdido, os sinais de cálcio falham, o músculo cardíaco contrai-se de forma fraca, a bexiga natatória não funciona e os animais morrem jovens. Ainda assim, o resgate dramático em uma linhagem genética diferente destaca uma mensagem central: o resto do genoma pode modificar fortemente o quão perigosa uma mutação é de fato. Para a saúde humana, isso reforça por que pessoas portadoras de variantes genéticas arriscadas podem experimentar desfechos muito diferentes, e por que entender tanto os genes centrais da doença quanto seu contexto genético é essencial para prever e tratar condições cardíacas.
Citação: Liu, L., Hu, Y., Xie, B. et al. Zebrafish casr modulates cardiac structure and function. Sci Rep 16, 8543 (2026). https://doi.org/10.1038/s41598-026-39063-9
Palavras-chave: sinalização do cálcio, desenvolvimento do coração, modelo peixe-zebra, contexto genético, função cardíaca