Clear Sky Science · pt
Identificação in silico de antagonistas inaláveis de pequenas moléculas para IL-33/ST2 em endótipos de asma grave tipo‑2‑alta
Por que isso importa para a respiração
Para milhões de pessoas com asma grave, mesmo inaladores modernos e injeções avançadas podem deixá‑las sem fôlego e em risco de crises perigosas. Este estudo investiga se drogas conhecidas, no formato mais parecido com comprimidos, poderiam ser reprojetadas para atuar como tratamentos inaláveis que bloqueiam um dos sinais “de alarme” iniciais da asma nos pulmões. Usando apenas simulações computacionais, os pesquisadores procuraram pequenas moléculas que pudessem se encaixar em um receptor-chave envolvido na asma grave mediada por alergia, preparando o terreno para testes laboratoriais futuros, em vez de oferecer um medicamento pronto para uso.
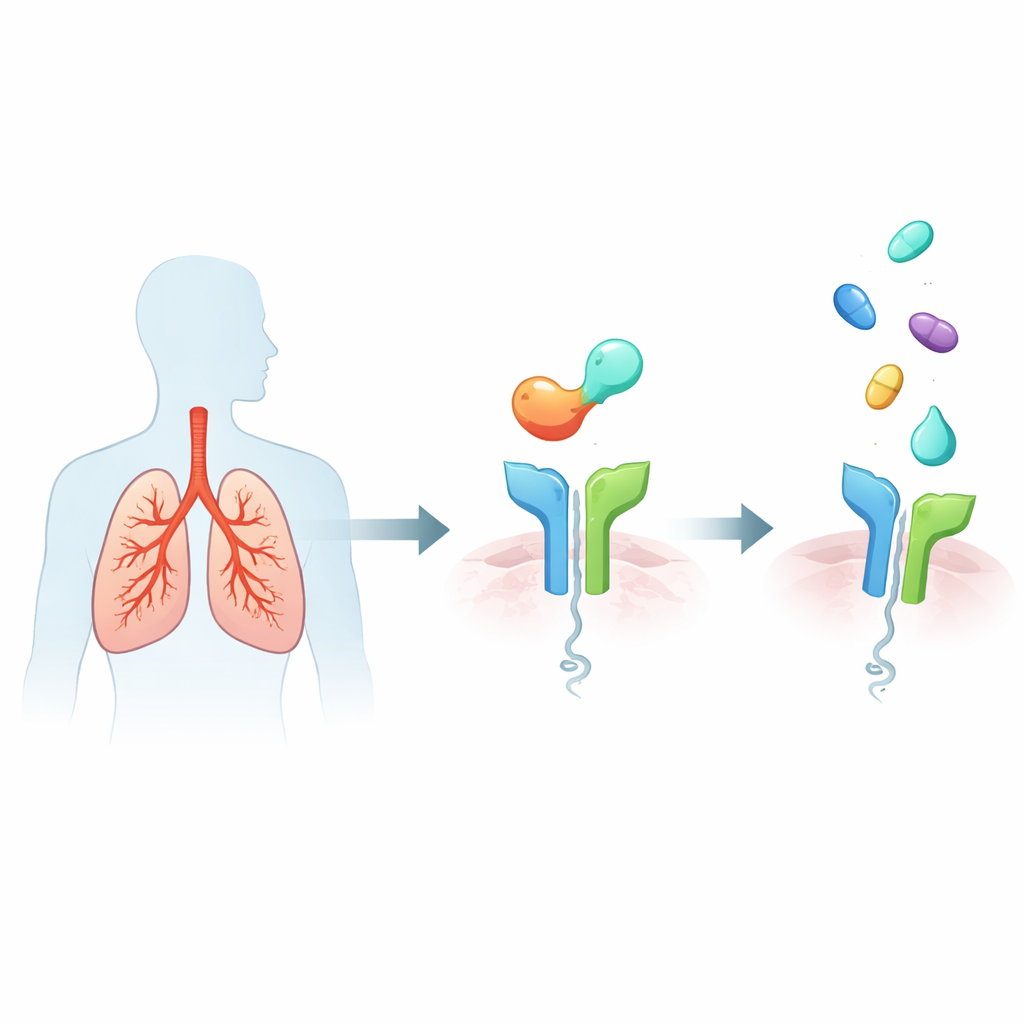
O sistema de alarme dentro dos pulmões asmáticos
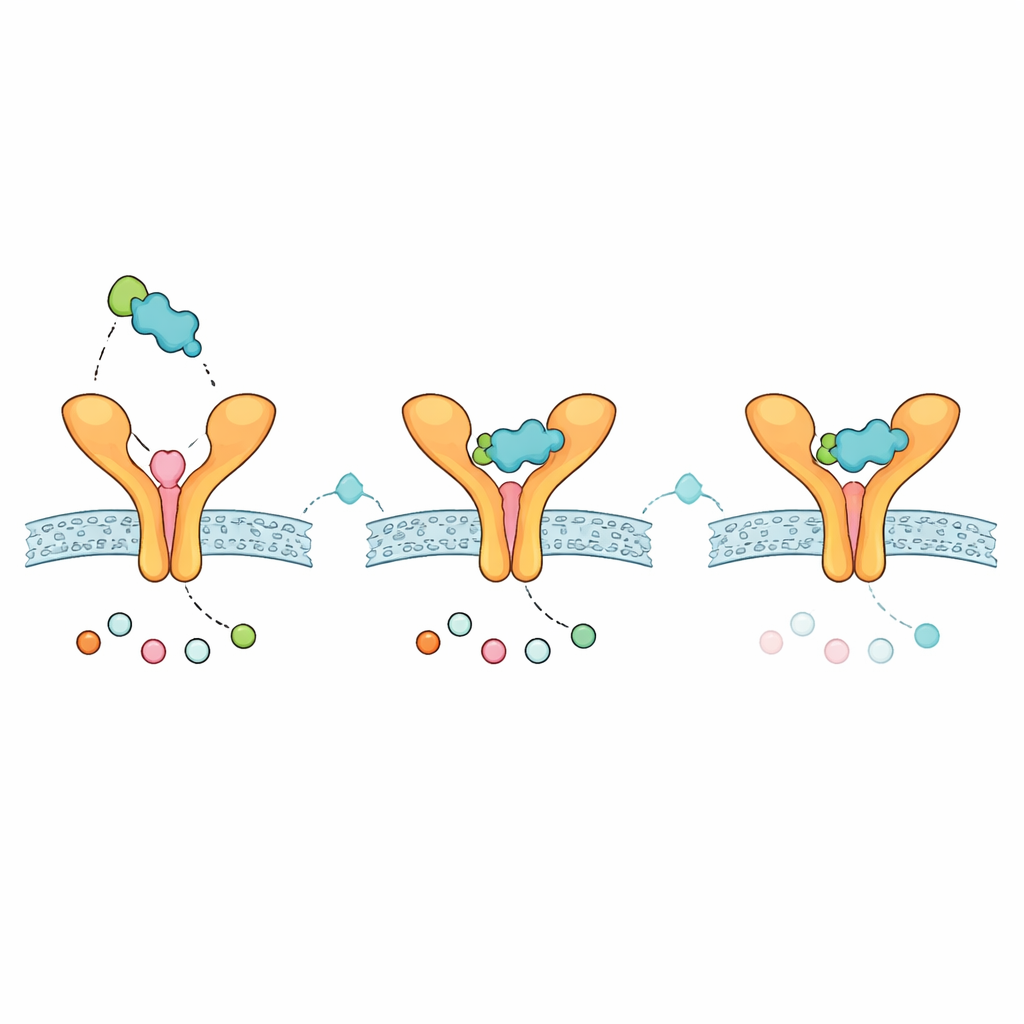
A asma grave tipo‑2‑alta é caracterizada por uma resposta imune hiperativa que enche as vias aéreas de muco e células inflamatórias, estreita os tubos respiratórios e danifica a estrutura pulmonar ao longo do tempo. Um gatilho importante é uma proteína chamada IL‑33, liberada por células do revestimento das vias aéreas sob estresse. A IL‑33 se liga a um receptor chamado ST2 em várias células imunes, que então liberam mensageiros potentes que impulsionam características clássicas da asma, como chiado, exacerbações e remodelamento crônico das vias aéreas. Como maior atividade IL‑33/ST2 está associada a sintomas piores e ataques mais frequentes, o ST2 emergiu como um alvo upstream atraente: bloquear o ST2 pode silenciar muitos dos sinais inflamatórios downstream de uma só vez.
De anticorpos para fármacos no estilo do dia a dia
Várias terapias atuais para asma grave usam anticorpos injetáveis que capturam proteínas inflamatórias no sangue ou bloqueiam seus receptores. Embora eficazes para alguns pacientes, esses fármacos biológicos são caros, precisam ser administrados por injeção e focalizam principalmente sinais mais distais na via. Em contraste, drogas de pequenas moléculas — mais parecidas com comprimidos ou inaladores tradicionais — poderiam ser fabricadas em escala, armazenadas com facilidade e potencialmente entregues diretamente nos pulmões. O desafio é que o ST2 se liga à IL‑33 por meio de uma interface proteína‑proteína ampla, que é mais difícil de ser perturbada por pequenas moléculas do que um bolso profundo e bem delimitado em uma enzima. Os autores, portanto, recorreram a dados estruturais de alta resolução do complexo ST2–IL‑33 e a ferramentas in silico modernas para ver se algum fármaco anti‑inflamatório conhecido poderia, inesperadamente, aderir a parte dessa interface.
Varrendo a superfície do receptor por computador
Usando a estrutura cristalina do ST2 humano ligado à IL‑33, a equipe primeiro removeu a IL‑33 para expor a superfície de ligação do receptor e empregou um programa de identificação de bolsões para apontar a região mais promissora para uma pequena molécula se alojar. Em seguida, selecionaram dez pequenas moléculas clinicamente relevantes já usadas em asma ou doenças imunes relacionadas — como os bloqueadores de leucotrienos Montelucaste e Zafirlucaste, derivados da talidomida que modulam o sistema imune e inibidores de JAK — além de uma molécula previamente reportada focada em ST2 como referência. Com software de docking virtual, cada composto foi posicionado milhares de vezes na superfície do ST2, e as poses de melhor encaixe foram pontuadas pela força de ligação prevista. O Zafirlucaste emergiu como o esqueleto de maior classificação, superando ligeiramente o Montelucaste e o comparador conhecido direcionado ao ST2.
Ajustando uma molécula líder na tela
Como o Zafirlucaste mostrou o balanço mais promissor entre ligação prevista e comportamento geral semelhante ao de fármaco, os autores usaram uma ferramenta de design guiada por IA para criar uma versão modificada dessa molécula. O objetivo foi manter sua afinidade ao ST2 enquanto melhorava o perfil de segurança previsto. O análogo redesenhado apresentou uma pontuação de docking muito similar e foi previsto como menos tóxico in silico. Mapas detalhados de contatos sugeriram que tanto o composto original quanto o modificado tocam vários dos mesmos aminoácidos do ST2 que normalmente contatam a IL‑33, indicando que ocupam partes funcionalmente importantes da interface. Simulações estendidas de dinâmica molecular — meio microssegundo de movimento virtual em água e sal — mostraram que receptor e ligante permaneceram flexíveis, com a pequena molécula amostrando diferentes posições ao longo da superfície em vez de se travar rigidamente no lugar. Cálculos das energias de interação ao longo do tempo apontaram para uma associação significativa, porém dinâmica, consistente com uma molécula sondando uma superfície proteína‑proteína relativamente plana.
Pistas sobre como um futuro inalador poderia se comportar
Para explorar se o Zafirlucaste modificado poderia plausivelmente funcionar como um medicamento, a equipe executou checagens computacionais padrão de absorção, distribuição, metabolismo, excreção e toxicidade. O análogo satisfez regras comuns de “drug‑likeness” oral, mostrou tamanho e lipossolubilidade moderados e foi previsto como incapaz de atravessar o cérebro — características que podem ser favoráveis para um tratamento focado nos pulmões com efeitos colaterais sistêmicos limitados. Estimativas de solubilidade variaram conforme o modelo, implicando que formulação cuidadosa seria necessária, especialmente para vias não orais como a inalação. O composto também foi previsto como capaz de interagir com certas enzimas hepáticas, sugerindo que possíveis interações fármaco‑fármaco precisariam de atenção caso viesse a ser usado junto com outros medicamentos.
O que este trabalho realmente mostra
Em vez de entregar um novo remédio para asma, este estudo demonstra uma estratégia computacional passo a passo para encontrar e refinar pequenas moléculas que possam interferir no sistema de alarme IL‑33/ST2 na superfície das células das vias aéreas. Destaca o Zafirlucaste e um parente otimizado por IA como pontos de partida plausíveis para experimentos laboratoriais, mostrando que podem ocupar partes-chave da interface do ST2 e ter propriedades previstas de segurança e semelhança com fármacos amplamente aceitáveis. Contudo, todas as evidências são virtuais: o trabalho não prova que essas moléculas bloqueiam a ligação da IL‑33 ao ST2, atenuam a sinalização inflamatória ou ajudam pacientes a respirar melhor. Essas respostas exigirão testes bioquímicos, estudos celulares, modelos animais e, eventualmente, ensaios clínicos. Por ora, o estudo oferece um roteiro computacional e uma lista curta de esqueletos candidatos para cientistas que buscam transformar o próprio interruptor de alarme da asma em um alvo de fármaco inalável prático.
Citação: Sun, G., Liu, Q., Yu, M. et al. In Silico identification of inhalable small-molecule IL-33/ST2 antagonists for severe type-2-high asthma endotypes. Sci Rep 16, 7996 (2026). https://doi.org/10.1038/s41598-026-39027-z
Palavras-chave: asma grave, via IL-33 ST2, antagonistas de pequenas moléculas, desenho de fármacos in silico, terapêuticos inaláveis