Clear Sky Science · pt
Modelagem baseada em estrutura revela a base molecular da nova atividade da CYP153A6 em derivados de tolueno
Delegando Trabalhos Químicos Difíceis à Natureza
Químicos e a indústria dependem de reações que introduzem oxigênio em ligações carbono–hidrogênio resistentes—por exemplo, para descontaminar poluentes ou construir precursores para medicamentos e fragrâncias. Fazer isso de forma limpa, sem reagentes agressivos ou resíduos metálicos pesados, é difícil. Este estudo examina um catalisador natural, a enzima CYP153A6 de uma bactéria do solo, e formula uma pergunta simples com grandes implicações: pode essa enzima ser orientada para “elevar” seletivamente compostos semelhantes ao tolueno—componentes comuns de combustíveis e solventes—em produtos mais úteis e ambientalmente amigáveis?
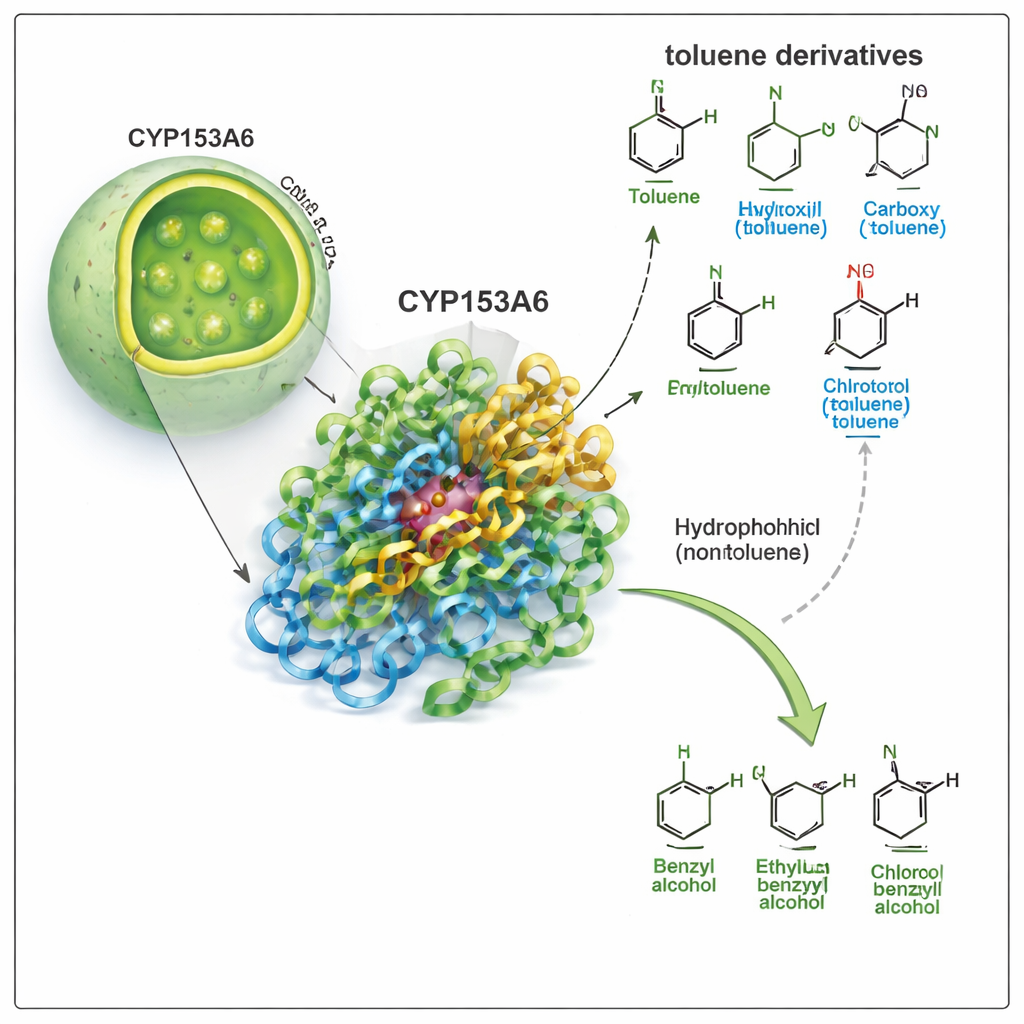
Uma Enzima que Escolhe um Único Ponto
CYP153A6 pertence à grande família dos citocromos P450, os versáteis especialistas naturais em oxidação. Ao contrário de muitos catalisadores industriais, essa enzima funciona em água, em temperatura moderada, e seleciona posições muito específicas numa molécula. Trabalhos anteriores mostraram que CYP153A6 adiciona oxigênio nas extremidades de cadeias hidrocarbonadas simples e em certos compostos aromáticos de origem vegetal. Aqui, os autores investigam se ela também pode atacar a posição “benzílica”—a pequena cadeia lateral ligada a um anel benzênico—no tolueno e em compostos relacionados. Essa transformação converte derivados de tolueno em álcoois benzílicos, blocos de construção valiosos para farmacêuticos, aromas e produtos finos.
Testando Quais Moléculas a Enzima Prefere
A equipe primeiro realizou experimentos de biotransformação usando células de E. coli modificadas que produzem CYP153A6, tanto como células inteiras quanto em extratos celulares. Exporam a enzima a um painel de derivados do tolueno, variando o grupo ligado ao anel aromático (como metil, cloro, metoxi, hidroxila ou nitro) e sua posição (para, meta ou orto). A enzima performou muito bem em compostos apolares ou apenas ligeiramente polares, como p-cimeno, p-xileno, p-metilanisol e p-clorotolueno, convertendo consistentemente o grupo metílico benzílico em um álcool benzílico. De forma marcante, ignorou por completo moléculas mais fortemente polares como p-cresol, p-metil benzil álcool e p-nitrotolueno, apesar de serem estruturalmente semelhantes. Esse padrão sugere que o bolso da enzima é fortemente hidrofóbico e desfavorece grupos polares.
Construindo um Mapa 3D da Máquina Molecular
Como a estrutura tridimensional da CYP153A6 não havia sido resolvida experimentalmente, os pesquisadores construíram um modelo computacional de alta qualidade usando um P450 estreitamente relacionado cuja estrutura é conhecida. Validaram esse modelo verificando sua geometria e rodando longas simulações de dinâmica molecular para ver se a proteína permanecia estável ao longo do tempo — o que ocorreu. As simulações revelaram um sítio ativo enterrado conectado ao exterior por túneis estreitos pelos quais substratos entram e produtos saem. Esses túneis são moldados e regulados por alças flexíveis na superfície da proteína, ajudando a explicar como a enzima pode guiar moléculas hidrofóbicas até o centro reativo do ferro do heme enquanto permite que água e produtos oxidados escapem.
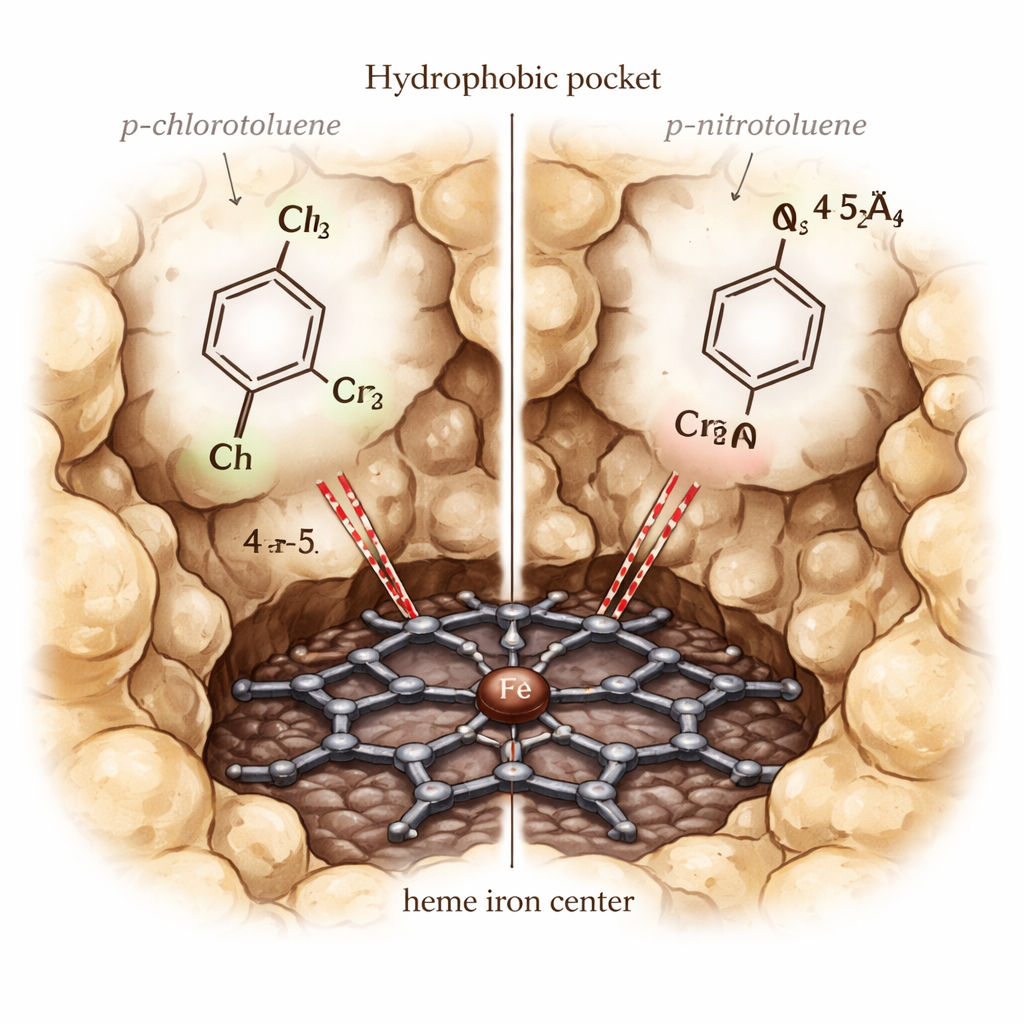
Observando Moléculas se Encaixarem, Moverem e Reagirem
Com o modelo em mãos, os autores simularam como diferentes derivados do tolueno se ligam dentro da CYP153A6. Usaram uma abordagem chamada docking em conjunto (ensemble docking), testando muitas formas sutilmente diferentes da proteína e vários estados eletrônicos do ferro do heme, para identificar quais combinações melhor distinguiam substratos reais de não-substratos. O cenário vencedor usou o ferro em seu estado férrico de repouso e sem moléculas extras de água no bolso, e favoreceu corretamente os substratos conhecidos. Simulações posteriores acompanharam, quadro a quadro, como cada molécula se posicionava em relação ao heme. Bons substratos como p-cimeno e p-xileno permaneceram próximos ao ferro com seu grupo metílico benzílico apontado para ele, e suas energias de ligação previstas foram fortemente favoráveis. Substratos ruins tenderam a se afastar, adotar orientações constrangedoras ou interagir de forma desfavorável com as cadeias laterais predominantemente oleosas que revestem o bolso.
Por Que Um Sósia Reage e Outro Não
Um enigma se destacou: p-clorotolueno é eficientemente oxidado pela CYP153A6, enquanto p-nitrotolueno não é, apesar de ambos se encaixarem no bolso e apresentarem forças de ligação similares nas simulações. Para resolver isso, os autores realizaram cálculos mais detalhados de mecânica quântica/mecânica molecular (QM/MM) no estado altamente reativo “Composto I” da enzima. Esses cálculos mostraram que o grupo nitro retira tanta densidade eletrônica do carbono benzílico que ele se torna muito difícil de oxidar, apesar da proximidade geométrica. Em contraste, o grupo cloro permite melhor comunicação eletrônica entre o heme e o substrato, refletida em maior densidade de spin no anel aromático e no grupo metila e em um alinhamento mais reativo para a etapa crítica de abstração de hidrogênio.
O Que Isso Significa para uma Química Mais Limpa
Em termos cotidianos, a CYP153A6 comporta-se como uma pequena luva oleosa que segura certas moléculas semelhantes a combustíveis na posição exata para que oxigênio seja adicionado em um ponto específico—transformando-as em produtos mais solúveis em água, úteis e, em última instância, mais degradáveis. O estudo mostra que a enzima prefere substituintes não polares e que tanto a forma quanto o fluxo eletrônico determinam se um derivado de tolueno será transformado. Ao esclarecer como CYP153A6 reconhece e ativa essas moléculas, o trabalho traça um roteiro para engenharia de versões aprimoradas que poderiam ajudar a limpar poluentes aromáticos ou fabricar compostos complexos de forma mais sustentável.
Citação: Wei, Y., Donzella, S., Foiadelli, S. et al. Structure-based modeling reveals molecular basis for CYP153A6’s novel activity toward toluene derivatives. Sci Rep 16, 7570 (2026). https://doi.org/10.1038/s41598-026-38986-7
Palavras-chave: biocatálise, citocromo P450, hidroxilação de tolueno, engenharia de enzimas, química verde