Clear Sky Science · pt
Biofábrica transplastômica para a produção de α‑lactoalbumina humana funcional para aplicações nutricionais e terapêuticas
Transformando plantas em fábricas de proteínas do leite
As dietas modernas dependem fortemente de proteínas do leite, mas a criação de vacas em escala global traz custos ambientais e questões éticas. Este estudo explora uma maneira bastante diferente de produzir uma proteína-chave do leite humano — ensinando folhas de plantas a fabricá‑la. O trabalho mostra que plantas de tabaco podem ser reprogramadas para manufaturar α‑lactoalbumina humana, uma proteína importante para a nutrição infantil e com potencial atividade anticâncer, abrindo caminho para ingredientes de fórmulas infantis sem origem animal e novos componentes alimentares com propriedades antitumorais.
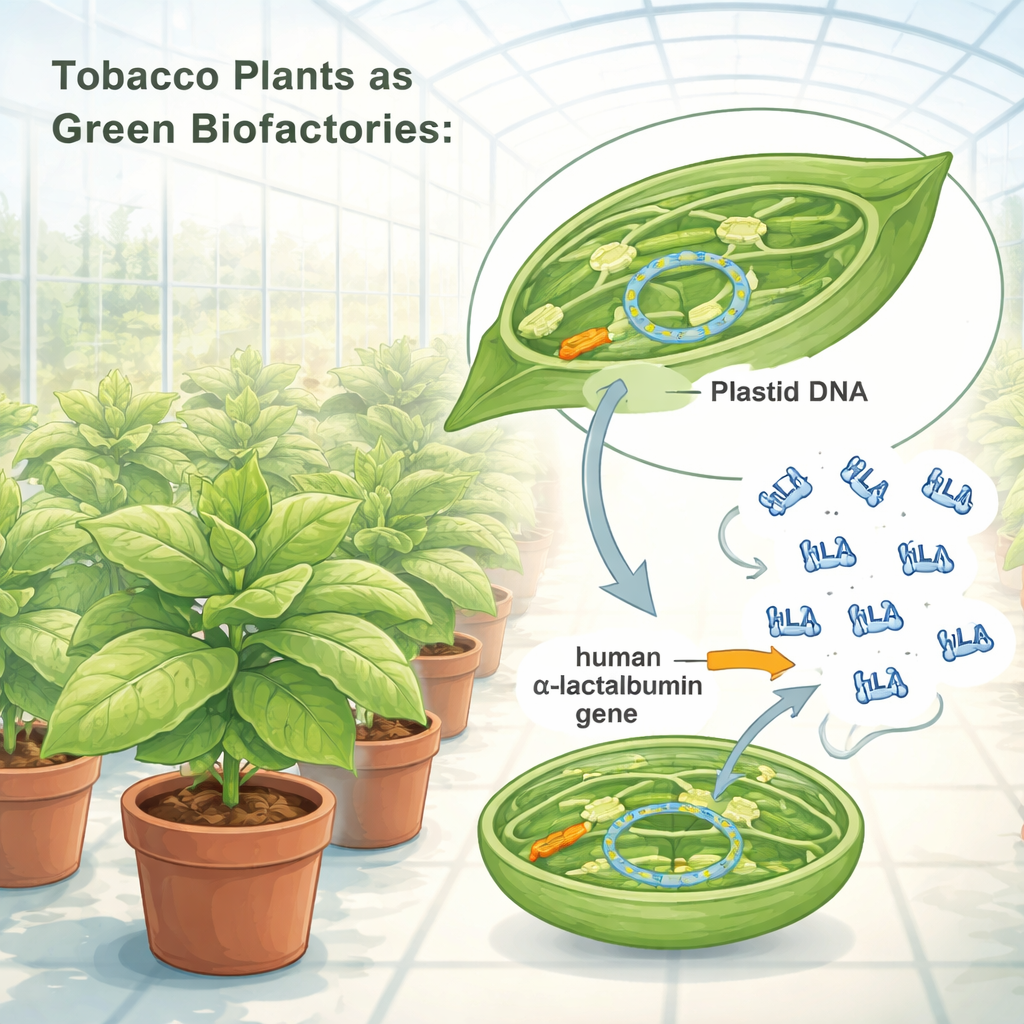
Por que essa proteína do leite é importante
O leite materno é mais que alimento; é um coquetel bem ajustado de proteínas, gorduras e açúcares que muda conforme as necessidades do bebê. Uma de suas proteínas mais importantes é a α‑lactoalbumina, que auxilia a síntese de lactose, o principal açúcar do leite e fonte crítica de energia para lactentes. A α‑lactoalbumina é rica em aminoácidos essenciais, incluindo triptofano, precursor do neurotransmissor serotonina, e tem sido associada a maior resistência ao estresse e potencial proteção contra certos tipos de câncer. Por ser de fácil digestão, ter sabor suave e permanecer estável em ampla faixa de acidez, é amplamente usada em fórmulas infantis e bebidas nutricionais — e a demanda está em crescimento.
O problema com a pecuária tradicional
Depender de vacas para fornecer proteínas do leite tem desvantagens. O setor pecuário é responsável por uma parcela significativa das emissões globais de gases de efeito estufa, e grandes operações leiteiras demandam vastas áreas de terra, água e ração. Além disso, o manejo das fazendas pode introduzir preocupações sobre hormônios, antibióticos e patógenos na cadeia do leite. Essas pressões impulsionaram o interesse por abordagens de “agricultura celular”, nas quais proteínas do leite são fabricadas por microrganismos ou células cultivadas em vez de animais. No entanto, muitos desses sistemas ainda são caros, difíceis de escalar ou produzem proteínas que não são idênticas às versões humanas. Plantas, especialmente os cloroplastos das folhas — as pequenas fábricas verdes que conduzem a fotossíntese — oferecem uma plataforma alternativa promissora.
Reprogramando cloroplastos como biofábricas
Os pesquisadores redesenharam as instruções genéticas da α‑lactoalbumina humana para que os cloroplastos do tabaco pudessem lê‑las de forma eficiente. Inseriram esse gene otimizado no DNA dos cloroplastos, usando um “cassete gênico” composto por fortes elementos regulatórios vegetais que funcionam como interruptores potentes. Utilizando um método de bombardeio com partículas, eles entregaram esse cassete nas células foliares do tabaco e então selecionaram plântulas cujos cloroplastos haviam adotado completamente o novo gene. Testes genéticos confirmaram que todas as cópias do DNA cloroplastidial nessas plantas passaram a conter o roteiro da proteína humana. As plantas modificadas cresceram normalmente em condições de estufa, produziram sementes e não mostraram penalidades visíveis em tamanho, forma ou fertilidade, sugerindo que a carga adicional de proteína não prejudicou a saúde vegetal.
Comprovando que a proteína produzida pela planta funciona
Em seguida, a equipe perguntou se a α‑lactoalbumina produzida na planta se comportava como a proteína humana real. Eles extraíram proteínas solúveis das folhas, purificaram a α‑lactoalbumina e examinaram sua estrutura usando uma técnica que revela como as proteínas se dobram. A “impressão digital” espectral da proteína derivada da planta quase coincidiu com a da α‑lactoalbumina humana comercial, indicando dobramento semelhante. Funcionalmente, a proteína vegetal ativou a enzima sintetizadora de lactose quase tão bem quanto a versão nativa, promovendo a formação de lactose a cerca de 93% da taxa da proteína padrão. Notavelmente, a α‑lactoalbumina acumulou‑se em cerca de 23% de toda a proteína solúvel nas folhas — um dos níveis mais altos relatados para proteínas humanas produzidas em cloroplastos vegetais — sugerindo que esse sistema pode fornecer rendimentos relevantes para a indústria.
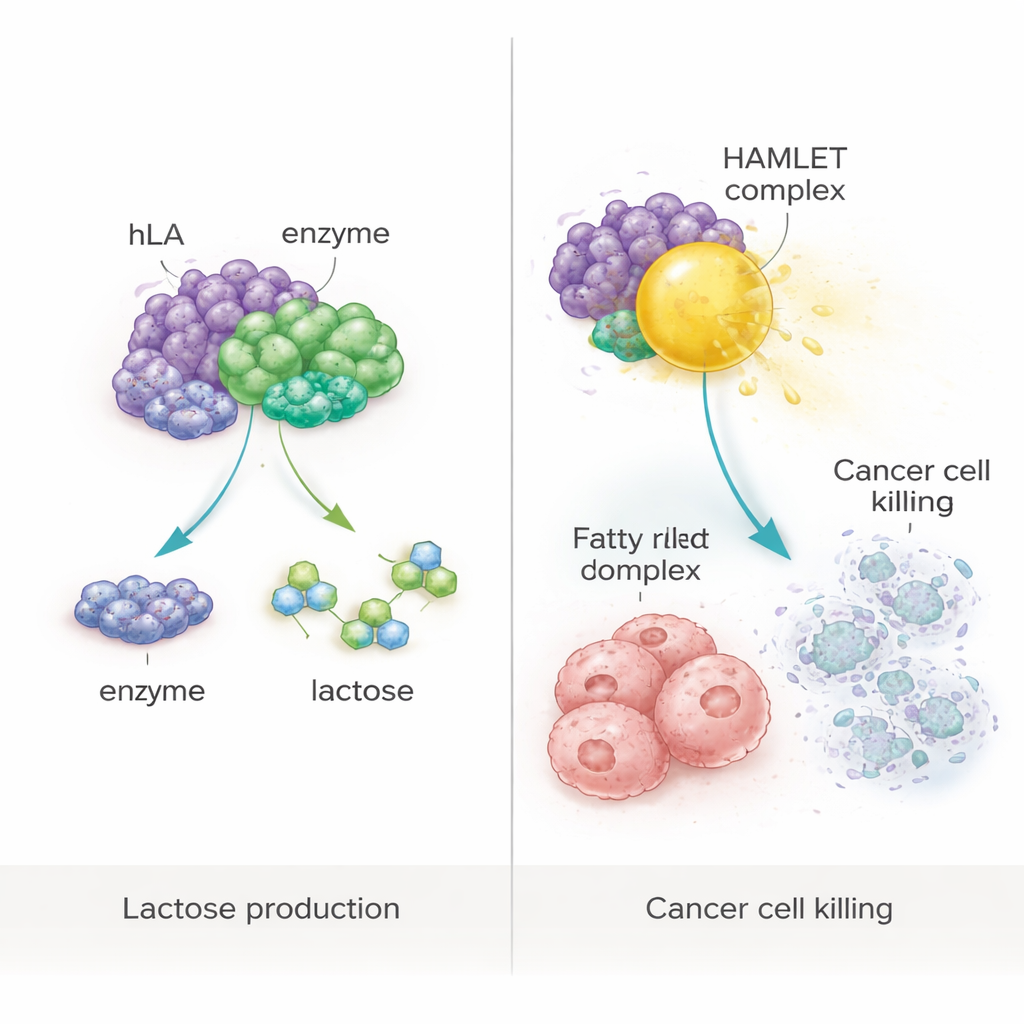
Da nutrição a complexos anticâncer
O estudo também testou uma ideia mais ambiciosa: usar a proteína produzida na planta como bloco de construção para um complexo anti‑câncer conhecido como HAMLET, formado quando a α‑lactoalbumina se liga fortemente ao ácido oleico, um ácido graxo comum. Ao aquecer suavemente a proteína purificada com ácido oleico sob condições controladas, os pesquisadores criaram um complexo semelhante ao HAMLET. Quando aplicado a células humanas de câncer colorretal (WiDr) e de mama (MCF‑7) em cultura, esse complexo reduziu drasticamente a sobrevivência celular para menos de 10%. Análises subsequentes mostraram que a maior parte das células afetadas estava em apoptose, uma forma de morte celular programada, em vez de rompimento descontrolado. Importante, nem a proteína isolada, nem o ácido graxo isolado, nem extratos de plantas não modificadas provocaram morte celular significativa, confirmando que o efeito citotóxico dependia do complexo específico.
O que isso pode significar para alimentos e medicamentos futuros
Em conjunto, o trabalho demonstra que cloroplastos vegetais podem produzir de forma confiável grandes quantidades de uma proteína do leite humano que é tanto nutricionalmente relevante quanto terapeuticamente ativa. Para um público não especializado, isso significa que futuras fórmulas infantis, alimentos funcionais ou suplementos poderiam um dia ser produzidos usando proteínas cultivadas em folhas em vez de extraídas de vacas, reduzindo o impacto ambiental enquanto se aproximam da biologia humana. Ao mesmo tempo, a mesma proteína de origem vegetal pode ser convertida em laboratório em um complexo anticâncer direcionado, sugerindo cadeias produtivas baseadas em plantas para biofármacos acessíveis. Embora sejam necessárias mais pesquisas para confirmar a segurança e o desempenho em animais e humanos — e para transferir essa tecnologia para culturas comestíveis — o estudo oferece um vislumbre convincente de plantas atuando como mini‑fábricas para a próxima geração de nutrição e medicina.
Citação: Ehsasatvatan, M., Kohnehrouz, B.B. Transplastomic biofactory for the production of functional human α-lactalbumin for nutritional and therapeutic applications. Sci Rep 16, 7359 (2026). https://doi.org/10.1038/s41598-026-38965-y
Palavras-chave: proteínas do leite produzidas em plantas, biofábrica de cloroplastos, alfa‑lactoalbumina humana, alternativas lácteas sustentáveis, terapia contra o câncer HAMLET