Clear Sky Science · pt
A2-pancortinas interagem com Bcl-xL e WAVE1 para promover sítios de contato mitocôndria-Retículo Endoplasmático (MERCs) e exacerbar a elevação do cálcio mitocondrial para mediar a morte celular no AVC
Por que conexões minúsculas no cérebro importam no AVC neonatal
O AVC costuma ser visto como uma doença de adultos, mas quando atinge recém-nascidos pode danificar silenciosamente o cérebro em desenvolvimento e causar problemas ao longo da vida. Este estudo investiga o que ocorre no interior das células nervosas durante essa crise. Os autores focam em uma família pouco conhecida de proteínas chamadas pancortinas e mostram como duas variantes do desenvolvimento agem como “amplificadores” perigosos, estreitando as conexões entre estruturas celulares-chave e impulsionando uma inundação de cálcio que pode empurrar os neurônios jovens rumo à morte.
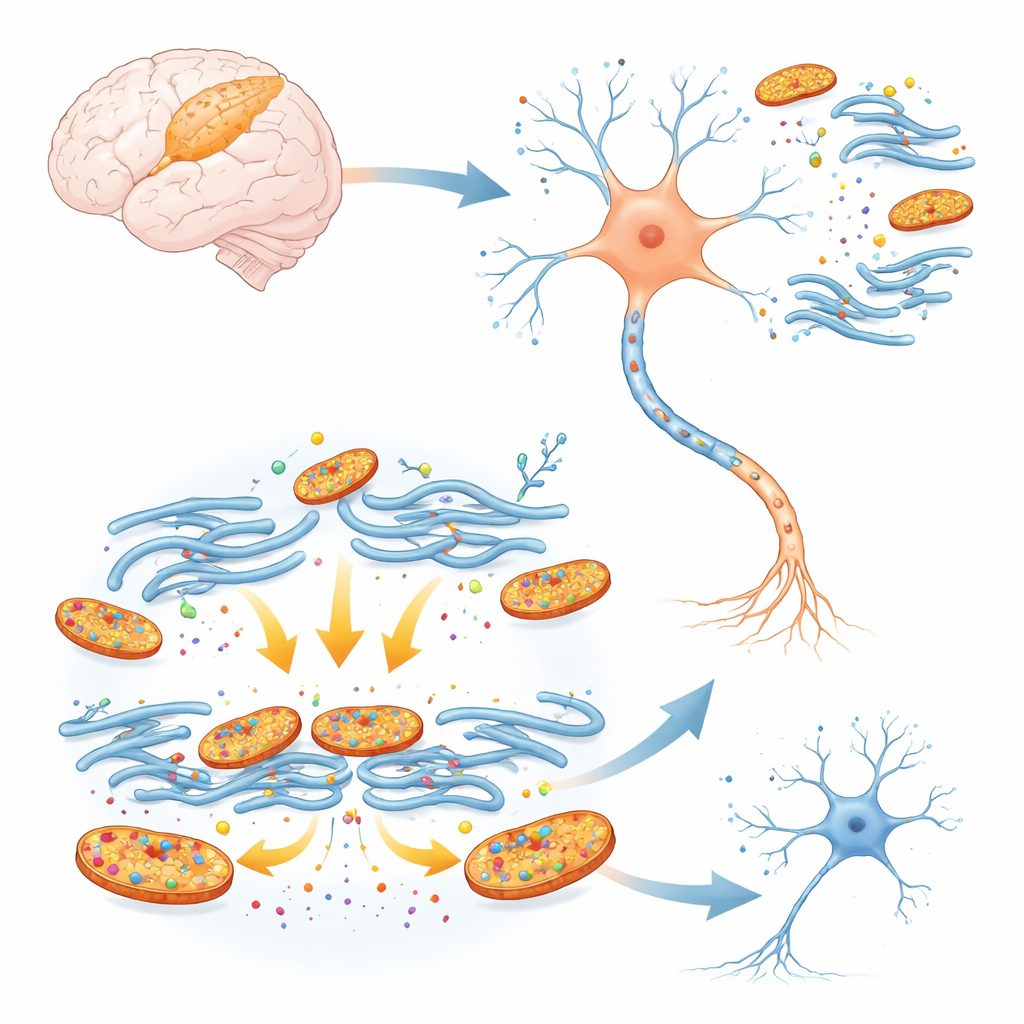
Responsáveis ocultos no cérebro neonatal
As pancortinas são proteínas com função de andaime que ajudam a moldar o cérebro em crescimento. Duas formas, chamadas A2-pancortinas, são abundantes durante o desenvolvimento inicial e depois diminuem amplamente à medida que o cérebro madura. Como cérebros recém-nascidos são especialmente vulneráveis à perda de oxigênio, os pesquisadores questionaram se essas proteínas do início da vida poderiam agravar o dano quando o fluxo sanguíneo ao córtex é brevemente interrompido, como ocorre no AVC neonatal. Em neurônios corticais de camundongo em cultura, eles usaram ferramentas genéticas para reduzir todos os níveis de pancortina e então expuseram as células a uma falta de oxigênio e glicose que imita o AVC. Neurônios com redução de pancortina tiveram muito mais chance de sobreviver, sugerindo que essas proteínas, em vez de proteger as células jovens, ajudam a impulsioná-las ao dano sob estresse.
De modelos de AVC em camundongo a tecido cerebral resgatado
Para verificar se esse papel nocivo também aparece em um cérebro vivo, a equipe desenvolveu camundongos que especificamente não expressam as formas A2-pancortinas do desenvolvimento. Camundongos jovens de duas semanas com nocaute e seus companheiros normais foram então submetidos ao bloqueio de uma artéria cerebral importante, um modelo padrão de AVC isquêmico. Após um dia, ambos os grupos mostraram lesão em regiões cerebrais profundas, mas o córtex dos camundongos sem A2-pancortinas teve cerca de metade do dano observado em animais normais. De forma marcante, esse efeito protetor desapareceu em animais de cinco semanas, quando variantes adultas de pancortina predominam. Esses resultados dependentes da idade apontam as A2-pancortinas como fatores pró-morte chave no córtex neonatal, ligando um programa de desenvolvimento à vulnerabilidade ao AVC.
Zonas de contato perigosas dentro dos neurônios
No interior das células, as mitocôndrias produtoras de energia ficam próximas ao retículo endoplasmático (RE), uma rede membranosa dobrada que armazena cálcio. Onde as duas membranas se aproximam, os chamados sítios de contato mitocôndria–RE atuam como túneis microscópicos pelos quais o cálcio pode passar. Transferências moderadas sustentam a produção de energia, mas o excesso pode sobrecarregar as mitocôndrias e desencadear a morte celular. Os pesquisadores descobriram que as A2-pancortinas, junto com dois parceiros — Bcl-xL e WAVE1 — se organizam em um complexo tripartido que se localiza nesses sítios de contato. Quando forçaram as células a produzir A2-pancortinas extras juntamente com esses parceiros, mitocôndrias e RE passaram a se tocar com mais frequência e mais firmeza, conforme relatado por um sensor fluorescente dividido especializado. Uma proteína de ancoragem chamada GRP75 juntou-se a esse complexo, ajudando a estabilizar as zonas de contato.
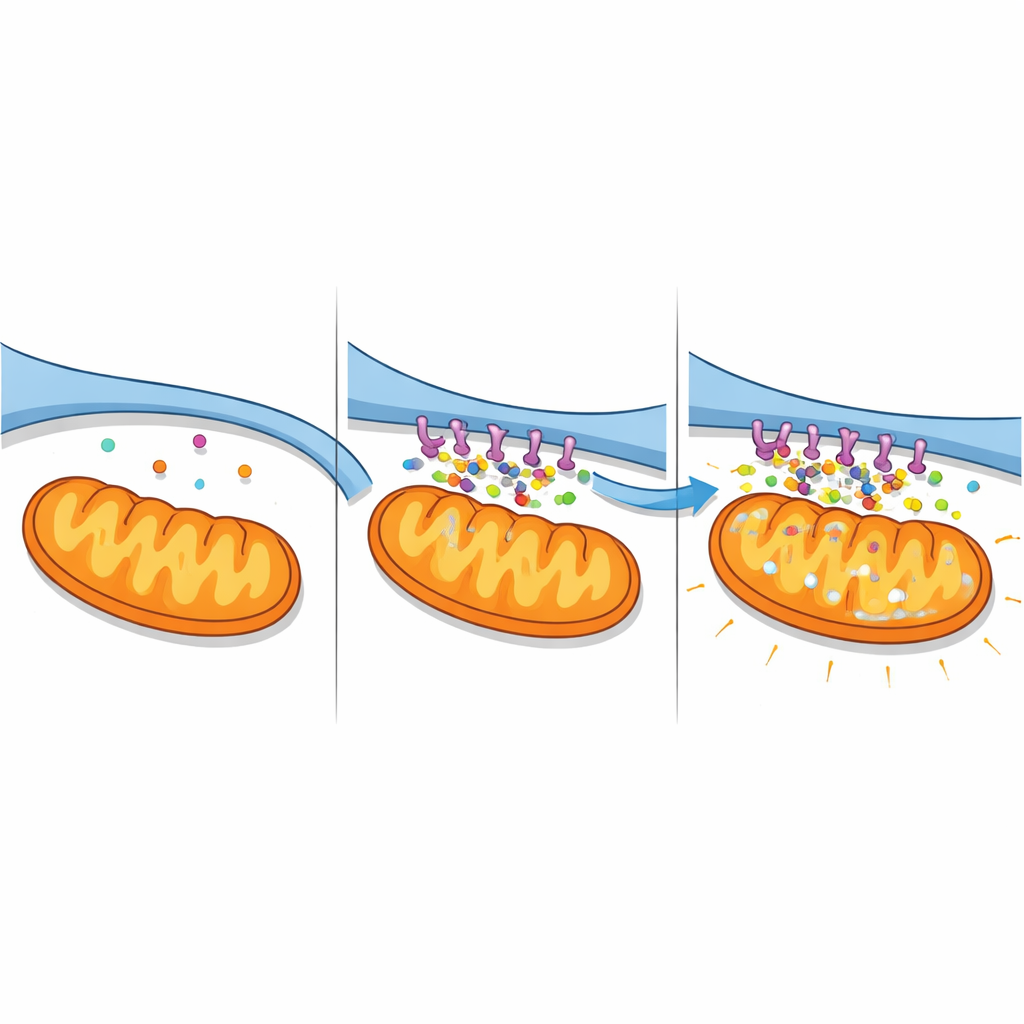
Inundações de cálcio e usinas de energia em colapso
Os contatos reforçados tiveram consequências sérias para o equilíbrio do cálcio. Usando indicadores fluorescentes que reportam separadamente o cálcio no citosol, no RE e nas mitocôndrias, os autores observaram as alterações ao longo do tempo. Células expressando o complexo A2-pancortina mostraram um aumento contínuo do cálcio dentro das mitocôndrias e no fluido circundante, juntamente com uma queda nas reservas do RE, assinatura de uma transferência massiva do RE para as mitocôndrias. Bloquear um canal chave de liberação de cálcio na superfície do RE (IP3R) impediu em grande parte essas mudanças, confirmando que o complexo amplifica uma via específica do RE para a mitocôndria. Em células do tipo nervoso expostas à privação de oxigênio e glicose semelhante ao AVC, a redução de pancortinas teve o efeito oposto: a sobrecarga de cálcio foi atenuada e as reservas do RE foram melhor preservadas. Juntos, esses achados revelam as A2-pancortinas como organizadoras de uma “superestrada” de cálcio que se torna letal sob estresse isquêmico.
O que isso significa para proteger cérebros recém-nascidos
Para não especialistas, a mensagem principal é que este trabalho identifica um novo interruptor molecular que ajuda a decidir se neurônios jovens vivem ou morrem após um AVC. Ao apertar as junções microscópicas entre membranas armazenadoras de cálcio e as usinas de energia celulares, as A2-pancortinas fazem com que as mitocôndrias engasguem com o excesso de cálcio e falhem. Remover essas proteínas em camundongos jovens suaviza o impacto do AVC experimental, sugerindo que drogas ou terapias baseadas em genes destinadas a interromper complexos de A2-pancortina — ou afrouxar os sítios de contato que reforçam — poderiam algum dia reduzir a lesão cerebral em recém-nascidos afetados. Embora tais tratamentos permaneçam prospectos futuros, o estudo mapeia uma via clara e testável desde proteínas do desenvolvimento até sobrecarga de cálcio e perda neuronal no AVC neonatal.
Citação: Yang, Q., Wang, CC., Matsuyama, T. et al. A2-pancortins interact with Bcl-xL and WAVE1 to promote mitochondria-ER contact sites (MERCs) and exacerbate mitochondrial calcium elevation to mediate cell death in stroke. Sci Rep 16, 8467 (2026). https://doi.org/10.1038/s41598-026-38928-3
Palavras-chave: AVC neonatal, sítios de contato mitocôndria-Retículo Endoplasmático, sobrecarga de cálcio, proteínas pancortina, morte neuronal