Clear Sky Science · pt
Perfil da microbiota intestinal e vias metabólicas em pacientes transplantados de coração infectados e não infectados antes e depois da cirurgia
Por que seu intestino importa após receber um novo coração
O transplante de coração pode dar a pessoas com insuficiência cardíaca grave uma segunda chance de vida, mas as infecções nas semanas seguintes à cirurgia continuam sendo uma ameaça importante. Este estudo faz uma pergunta aparentemente simples, porém de grande alcance: como a comunidade de micróbios que vive em nossos intestinos — a microbiota intestinal — muda no entorno do transplante cardíaco e essas mudanças podem ajudar a explicar quem desenvolve infecções e quem não desenvolve?
O minúsculo ecossistema dentro dos pacientes transplantados
Nossos intestinos abrigam trilhões de bactérias que ajudam a digerir os alimentos, treinar o sistema imunológico e conter germes invasores. A cirurgia, medicamentos imunossupressores potentes e antibióticos de amplo espectro podem abalar esse ecossistema frágil. Para acompanhar o que acontece em pacientes submetidos a transplante de coração, pesquisadores na China acompanharam 20 adultos que receberam corações doados. Eles coletaram amostras de fezes cerca de uma semana antes da cirurgia e novamente 30 dias depois, e então usaram sequenciamento de DNA para catalogar quais bactérias estavam presentes e ferramentas computacionais para prever o que esses micróbios poderiam estar fazendo metabolicamente.
Quatro grupos de pacientes, quatro padrões microbianos
A equipe dividiu os pacientes em quatro grupos: com e sem infecções antes da cirurgia, e com e sem infecções no primeiro mês após o procedimento. Antes do transplante, a diversidade geral e a estrutura da microbiota intestinal eram surpreendentemente semelhantes independentemente da presença prévia de infecção. Pessoas sem infecção pré-operatória eram majoritariamente colonizadas por um gênero familiar chamado Bacteroides, frequentemente associado à estabilidade intestinal. Em contraste, pacientes infectados apresentavam uma mistura que incluía o potencialmente nocivo Enterococcus casseliflavus ao lado de bactérias muitas vezes consideradas benéficas, como Limosilactobacillus e Weissella cibaria, sugerindo uma comunidade intestinal em equilíbrio delicado e oscilante.
Depois da cirurgia: uma bifurcação no caminho microbiano
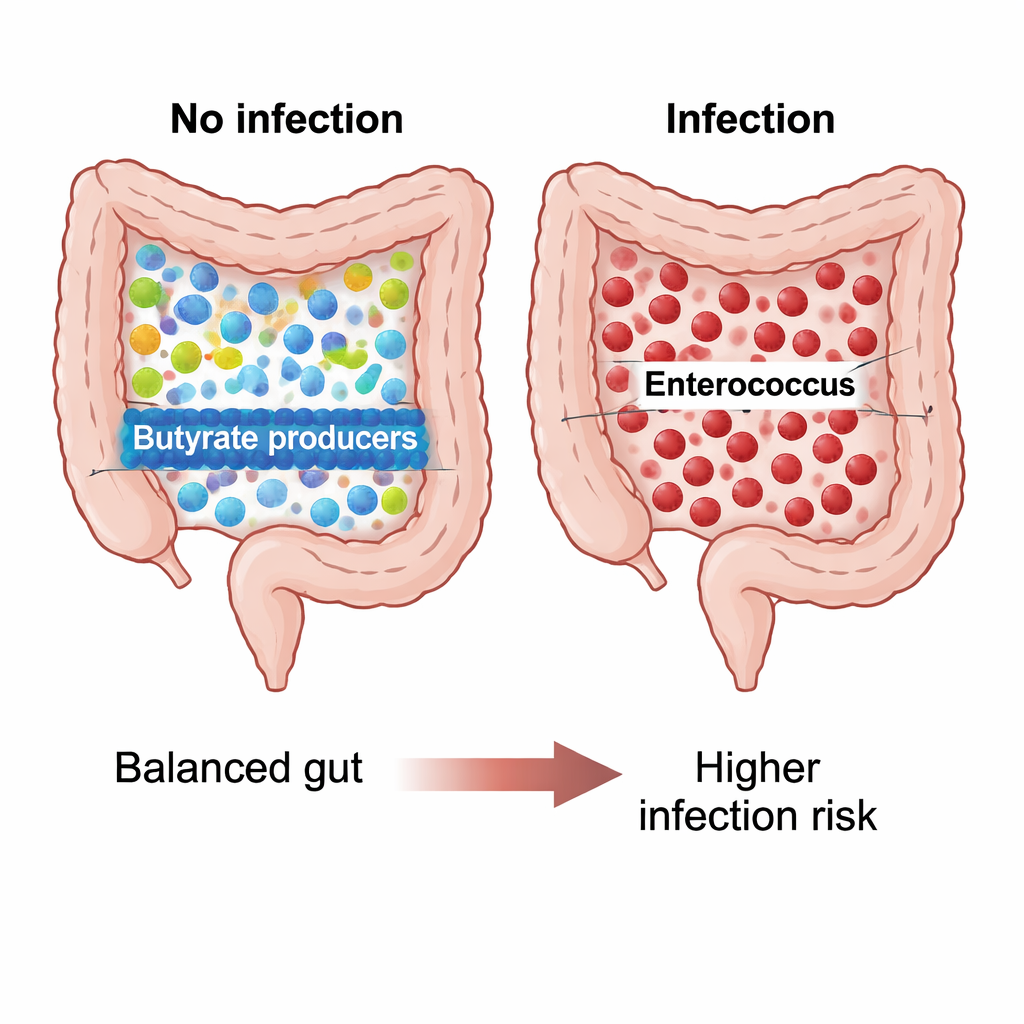
Aos 30 dias após a operação, a microbiota dos pacientes que evitaram infecção formou um padrão reconhecível, enquanto aqueles que desenvolveram infecções apresentaram um quadro bem diferente. Pacientes não infectados mostraram comunidades microbianas mais ricas e homogêneas, com muitos membros do gênero Blautia e bactérias relacionadas que produzem butirato, um ácido graxo de cadeia curta conhecido por nutrir as células intestinais e apoiar a estabilidade imunológica. Seus ecossistemas intestinais pareciam diversos e equilibrados. Nos pacientes que sofreram infecções, porém, a diversidade caiu e a comunidade foi dominada por Enterococcus faecium, uma bactéria resistente frequentemente associada a infecções hospitalares e conhecida por resistência a antibióticos. Análises estatísticas mostraram que os microrganismos desse grupo infectado se agrupavam à parte dos demais, apontando para um caso claro de perturbação microbiana pós-cirúrgica, ou disbiose.
Química microbiana ligada à proteção ou risco
Os pesquisadores também investigaram que tipos de funções químicas esses micróbios poderiam desempenhar. Usando software preditivo, eles encontraram que, no grupo pós-operatório não infectado, Blautia estava associada a vias que degradam um composto chamado L-1,2-propanodiol, um intermediário na fermentação de fibras que alimenta a produção de ácidos graxos benéficos como o propionato. Nos pacientes infectados, esse potencial metabólico previsto era marcadamente menor, consistente com uma comunidade intestinal menos capaz de produzir moléculas protetoras. Antes da cirurgia, Enterococcus casseliflavus em pacientes infectados estava ligado a rotas fermentativas incomuns que podem refletir um ambiente microbiano estressado e com alta demanda energética, embora isso precise de confirmação laboratorial direta.
O que isso significa para pacientes e equipes de cuidado
Para quem enfrenta um transplante de coração, esses achados sugerem que o intestino não é apenas um espectador; ele pode ajudar a moldar o risco de infecções perigosas. O estudo aponta para uma mudança dinâmica da dominância de Bacteroides antes da cirurgia para, após o procedimento, uma enriquecimento protetor por Blautia ou uma proliferação prejudicial de Enterococcus, dependendo de como se desenrola o período de recuperação inicial. O estresse relacionado à infecção e o uso intenso de antibióticos parecem empurrar a comunidade intestinal para um estado de baixa diversidade dominado por Enterococcus, observado em pacientes infectados. Os autores propõem uma estratégia de “duplo alvo”: favorecer o retorno de bactérias produtoras de butirato — possivelmente por meio da dieta ou probióticos selecionados com cuidado — enquanto monitoram de perto os níveis de Enterococcus. Embora sejam necessários estudos maiores e de maior duração, este trabalho abre a possibilidade de que, no futuro, o ajuste da microbiota intestinal passe a fazer parte rotineira dos cuidados para proteger pacientes de infecções potencialmente fatais.
Citação: Han, J., Hua, L., Yang, B. et al. Gut microbiota and metabolic pathway profiles in infected and non-infected heart transplant patients before and after surgery. Sci Rep 16, 7697 (2026). https://doi.org/10.1038/s41598-026-38911-y
Palavras-chave: transplante de coração, microbiota intestinal, infecção pós-operatória, antibióticos, bactérias produtoras de butirato