Clear Sky Science · pt
Desempenho cinético aprimorado e estabilidade da catalase imobilizada em caulinita funcionalizada com epóxi
Transformando uma Argila Natural em um Limpa‑pro
O peróxido de hidrogênio é amplamente usado para desinfetar, branquear e tratar água, mas o peróxido residual em correntes de resíduos industriais pode danificar células vivas e o meio ambiente. A natureza já fornece uma ferramenta poderosa de limpeza: a enzima catalase, que decompõe o peróxido de hidrogênio em água e oxigênio inofensivos. Contudo, enzimas livres são frágeis e difíceis de reutilizar. Este estudo mostra como um mineral de argila comum, a caulinita, pode ser modificado de forma suave para que a catalase se fixe fortemente a ele, tornando‑se uma "superfície de limpeza" mais resistente e reutilizável que pode ajudar a tornar processos industriais e o tratamento de águas residuais mais seguros e sustentáveis. 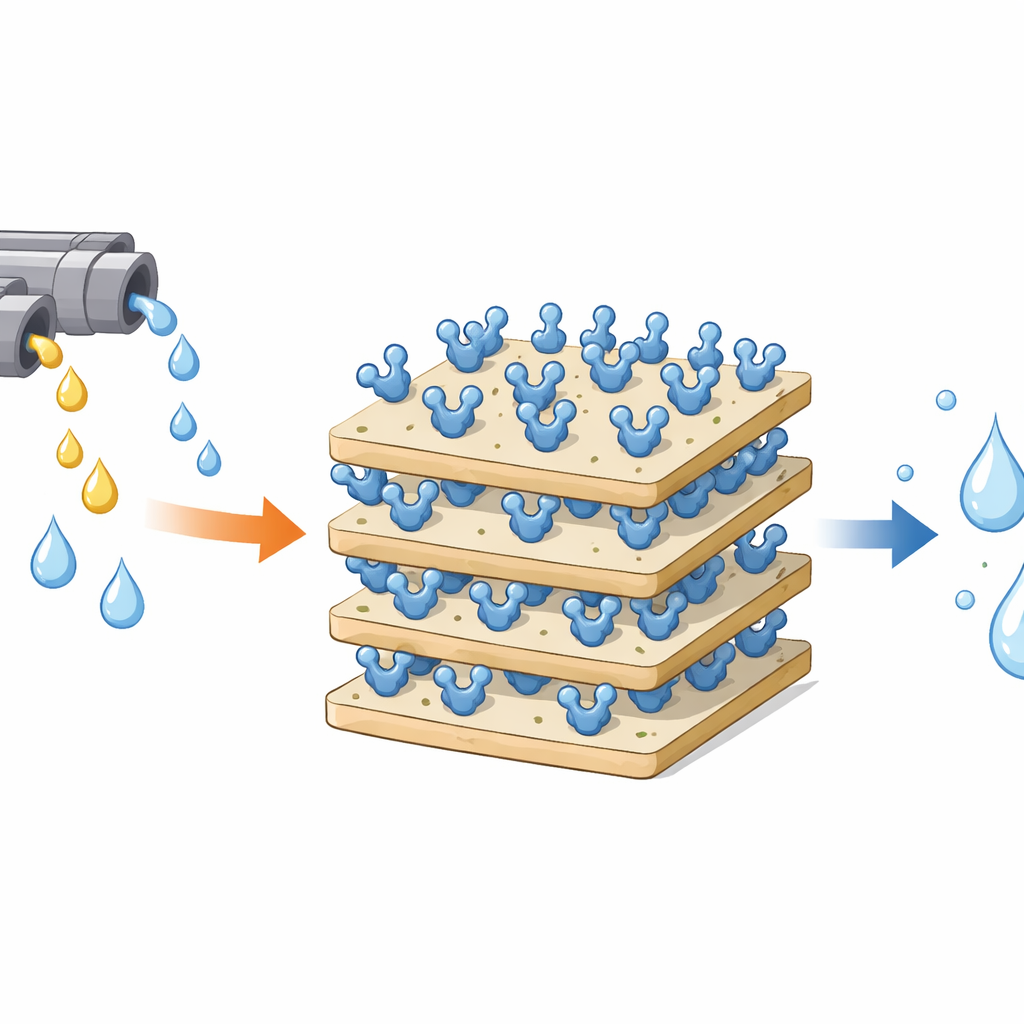
Um Mineral Comum com Potencial Oculto
A caulinita é uma argila branca barata e amplamente disponível, usada em papel, cerâmica e até na medicina. Possui uma estrutura em camadas que é mecanicamente resistente e quimicamente estável, mas sua superfície é relativamente inerte, de modo que enzimas não se prendem bem e tendem a ser lavadas. Tentativas anteriores de fixar catalase em caulinita simples basearam‑se principalmente em forças de atração fracas. Esses sistemas conseguiam reter alguma enzima, mas apresentavam baixa carga, lavagem fácil e perda de atividade ao longo do tempo. Os autores supuseram que, se pudessem introduzir mais sítios reativos na caulinita sem destruir sua estrutura, a argila poderia atuar como uma plataforma robusta e duradoura para a catalase.
Adicionando um Revestimento Pegajoso porém Suave
Para melhorar a caulinita, os pesquisadores revestiram sua superfície com uma pequena molécula chamada GPTMS, um tipo de silano que carrega um grupo epóxi. Em misturas água‑álcool sob condições levemente ácidas, o GPTMS primeiro se converte em grupos silanol que podem se ligar aos hidroxilas naturais da argila, formando uma camada orgânica fina e durável. As partes epóxi permanecem intactas e projetam‑se da superfície como anéis reativos minúsculos. Um conjunto de técnicas confirmou essa transformação: espectros de infravermelho mostraram novas vibrações relacionadas a carbono–hidrogênio e ao epóxi; imagens em microscopia eletrônica revelaram que a argila inicialmente compacta em placas tornou‑se mais aberta e porosa; análise térmica detectou perda de massa extra em temperaturas moderadas devido à camada orgânica recentemente anexada; e espectroscopia de superfície mostrou muito mais carbono na argila modificada, preservando ao mesmo tempo a estrutura mineral subjacente.
Ancorando a Enzima na Argila
Quando a catalase foi misturada com essa caulinita portadora de epóxi, a enzima rapidamente se ligou à superfície. Na primeira hora, a maior parte dos sítios de ligação já estava ocupada, e o equilíbrio foi essencialmente alcançado em quatro horas. A argila modificada pôde reter cerca de 300 miligramas de catalase por grama de suporte — muito acima dos sistemas à base de caulinita anteriores. A equipe descobriu que pH neutro e temperaturas moderadas (por volta da ambiente a corporal) eram melhores para a carga, refletindo um equilíbrio entre a estabilidade da enzima e a reatividade dos grupos amino da proteína com os anéis epóxi na superfície. Em nível molecular, grupos nucleofílicos na catalase atacam os anéis epóxi tensionados, formando múltiplas ligações fortes. Essa fixação em múltiplos pontos limita movimentos prejudiciais ao mesmo tempo que mantém o centro ativo acessível. 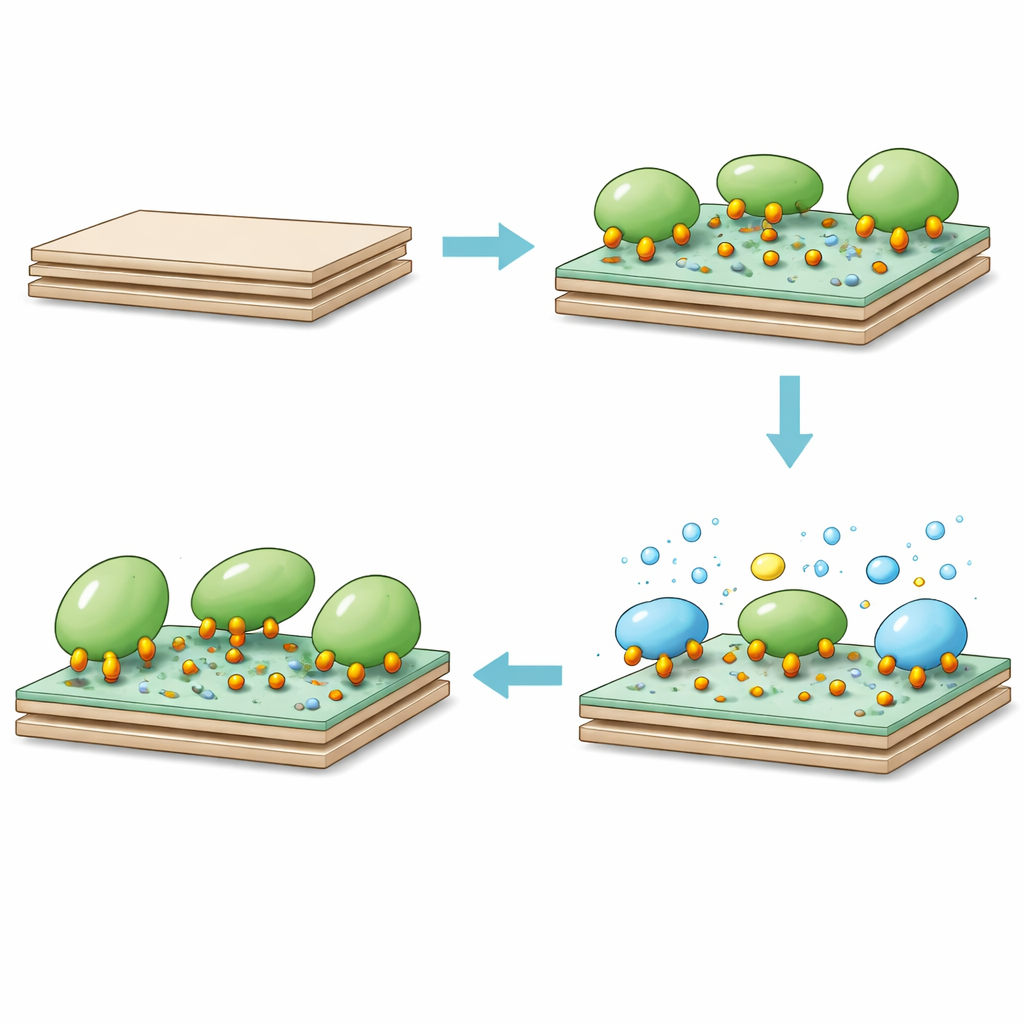
Ação Mais Rápida, Mais Resistente e de Maior Duração
Fixar a catalase na argila modificada alterou seu comportamento em relação ao peróxido de hidrogênio. A enzima imobilizada mostrou uma "demanda" aparente por substrato muito menor do que a enzima livre, o que significa que ela pode atuar de forma eficiente mesmo quando os níveis de peróxido são modestos. Embora a taxa máxima de reação tenha diminuído um pouco — provavelmente porque a difusão através da camada sólida e a flexibilidade reduzida da enzima retardam o processo — a eficiência catalítica global na verdade aumentou em cerca de 80%. Igualmente importante, a catalase imobilizada suportou repetidos usos e armazenamento prolongado muito melhor do que a forma livre. Manteve alta atividade após muitos ciclos de reação e preservou uma fração muito maior de sua potência inicial após semanas em armazenamento frio. O próprio suporte de argila também pôde ser regenerado e reutilizado várias vezes para recargas de enzima com apenas perda gradual de capacidade.
Por Que Isso Importa no Dia a Dia
Em termos simples, o estudo transforma uma argila familiar e de baixo custo em um suporte inteligente e reutilizável para uma enzima natural desintoxicante. Ao engenheirar cuidadosamente a superfície da argila com uma fina camada rica em epóxi, os pesquisadores criaram uma plataforma que prende firmemente a catalase, ajuda‑a a reconhecer seu alvo com mais facilidade e a protege de danos. Isso significa que podemos, potencialmente, limpar correntes industriais carregadas de peróxido, apoiar processos avançados de oxidação ou projetar tratamentos mais seguros na indústria alimentícia e farmacêutica usando quantidades menores de enzima por períodos mais longos. O trabalho mostra como o ajuste da interface entre minerais e proteínas pode desbloquear novas ferramentas duráveis para tecnologias mais verdes.
Citação: Erol, K., Veyisoğlu, A., Tatar, D. et al. Enhanced kinetic performance and stability of catalase immobilized on epoxy-functionalized kaolinite. Sci Rep 16, 8196 (2026). https://doi.org/10.1038/s41598-026-38910-z
Palavras-chave: imobilização de enzimas, catalase, argila caulinita, tratamento de efluentes, superfície funcionalizada com epóxi