Clear Sky Science · pt
Expressão alterada do eixo CD26/ADA na inflamação mediada pelo sistema imune na mononucleose infecciosa
Por que esse vírus infantil importa
Muitos pais conhecem a mononucleose infecciosa, frequentemente chamada de “mono”, como uma doença ruim, porém geralmente temporária, caracterizada por febre, dor de garganta e linfonodos aumentados. No entanto, em um pequeno número de crianças, a infecção pode tornar‑se grave e causar danos a órgãos como o fígado. Este estudo investiga, em detalhes, como o sistema imune das crianças reage ao vírus Epstein–Barr, a principal causa da mono, e foca em um par de parceiros minúsculos na superfície celular — CD26 e uma enzima chamada ADA — que podem ajudar a explicar por que algumas respostas imunes se tornam perigosamente intensas.
Os defensores do corpo em excesso
Quando o vírus Epstein–Barr entra no organismo, ele infecta principalmente certos glóbulos brancos e desencadeia uma forte reação imune. Neste estudo, os médicos compararam sangue de 30 crianças com mono aguda a 30 crianças saudáveis. Eles descobriram que as crianças doentes apresentavam muito mais glóbulos brancos no total, especialmente um subconjunto chamado células T CD8, especializadas em matar células infectadas. Ao mesmo tempo, outro grupo importante de auxiliares, as células T CD4, estava relativamente reduzido, de modo que o equilíbrio habitual entre células de “ataque” e de “apoio” foi invertido. Níveis de proteínas que combatem infecções no sangue, incluindo várias moléculas sinalizadoras que aumentam ou diminuem a inflamação, também estavam mais elevados, mostrando que o sistema imune estava totalmente ativado.
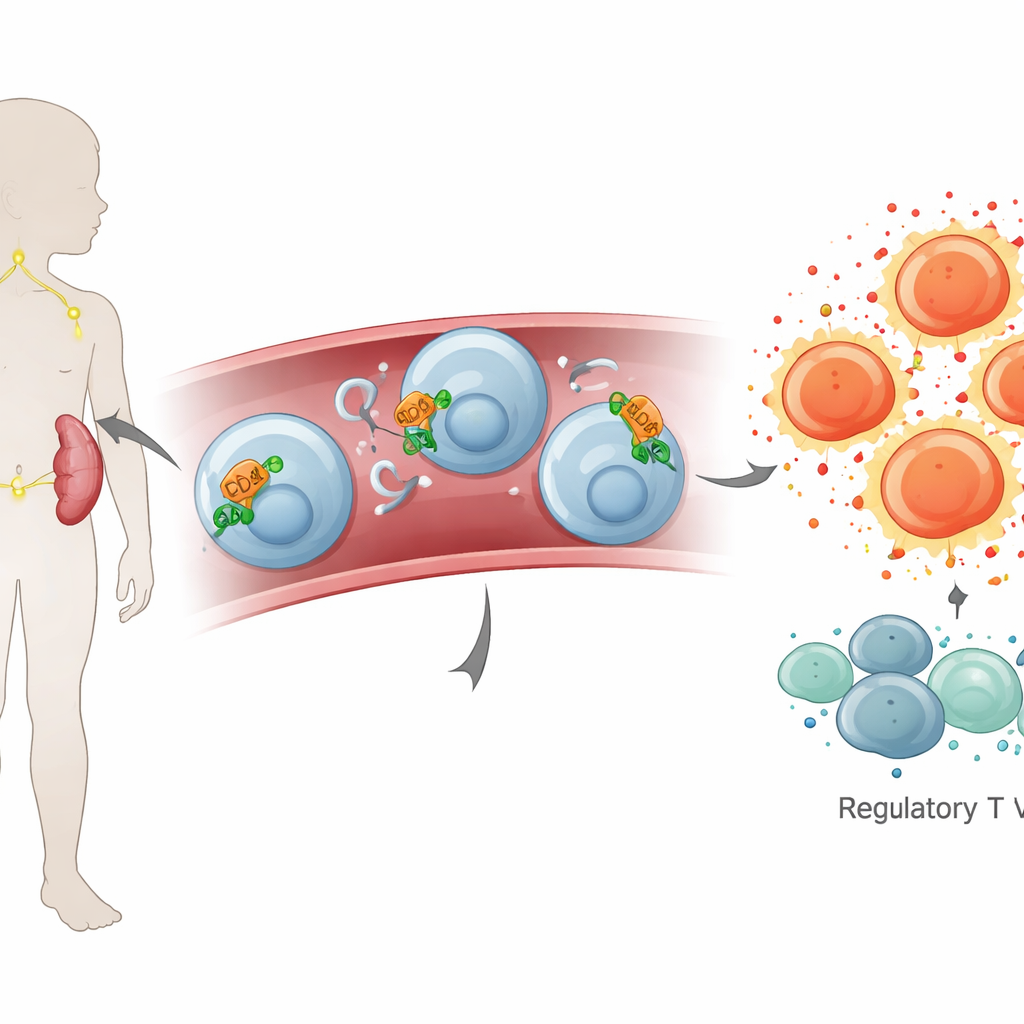
Um olhar atento num pequeno interruptor de controle
Os pesquisadores então se concentraram em CD26 e ADA, duas moléculas que se situam no cruzamento entre a ativação celular e a sinalização química fora das células. Usando testes genéticos em células sanguíneas, eles verificaram que crianças com mono apresentavam níveis mais altos das instruções para CD26 e ADA (mRNA), sugerindo que as células imunes estavam se preparando para produzir mais dessas proteínas. Testes sanguíneos confirmaram que a atividade da ADA em si estava aumentada. Curiosamente, a quantidade circulante da proteína CD26 no plasma não diferiu muito entre crianças doentes e saudáveis, o que sugere que, na mono, essa molécula pode permanecer principalmente aderida às superfícies celulares em vez de flutuar livremente.
Deslocamento do equilíbrio entre ataque e contenção
Para entender como esse interruptor de controle se comportava em diferentes células imunes, a equipe usou citometria de fluxo, um método que conta e caracteriza células uma a uma. Nas células T CD8, as que se expandem dramaticamente durante a mono, o CD26 era mais comum, independentemente de as células carregarem outro marcador chamado CD39, associado a um poderoso sistema de freio químico. Esse padrão sugere que nessas células “assassinas”, o CD26 pode ajudar a superar sinais químicos locais que normalmente amorteceriam sua atividade, sustentando um ataque forte às células infectadas pelo vírus. Ao mesmo tempo, entre as células T CD4 que usualmente ajudam a coordenar respostas imunes, o quadro foi mais misto. Células que expressavam tanto CD4 quanto CD39 — frequentemente associadas a papéis regulatórios e calmantes — foram relativamente mais frequentes, o que pode ajudar a explicar níveis elevados de sinais atenuantes como a citocina IL‑10.
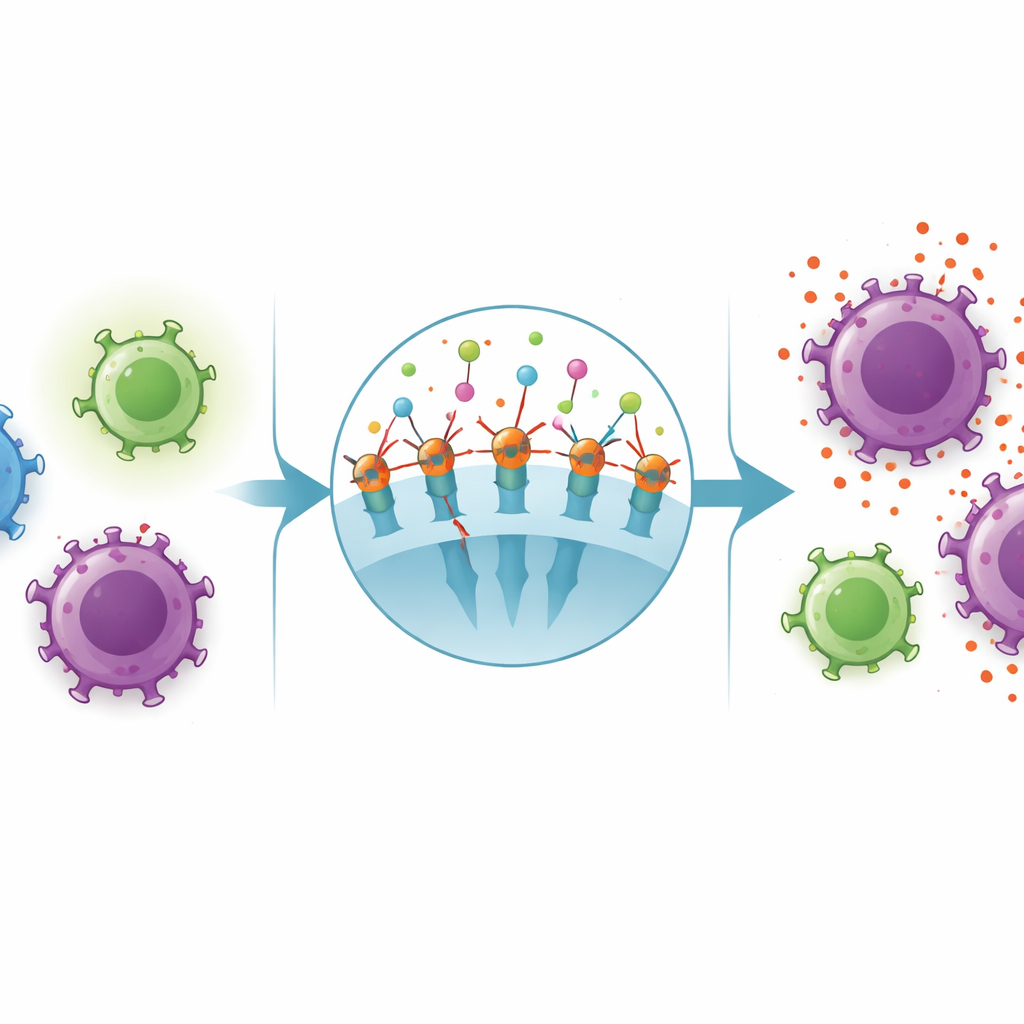
Quando a regulação enfraquece
Contudo, dentro da população de CD4 que não expressa CD39 e é tipicamente composta por células auxiliares ativas, a fração de células exibindo CD26 foi, na verdade, menor em crianças com mono do que em pares saudáveis. Essa perda de CD26 nas células auxiliares pode reduzir sua capacidade de proliferar e coordenar respostas equilibradas, mesmo enquanto as células CD8 são impulsionadas para uma atividade mais intensa. O estudo também mostrou que a quantidade de CD26 no plasma acompanhou os níveis de ADA e de interferon‑gama, um potente sinal inflamatório, e se relacionou inversamente com a participação de células T CD4 e com a razão CD4‑para‑CD8. Em conjunto, esses padrões apontam o “eixo” CD26/ADA como fortemente conectado à intensidade com que o sistema imune responde durante a infecção.
O que isso significa para crianças doentes
Para famílias e clínicos, esses achados oferecem um retrato mais claro do motivo pelo qual um vírus comum pode, às vezes, causar doença preocupante. Na mono aguda, os sistemas imunes das crianças parecem depender fortemente de células T CD8 armadas com atividade extra do par CD26–ADA, impulsionando um forte ataque antiviral que corre o risco de extrapolar e danificar tecidos. Ao mesmo tempo, certas células auxiliares e regulatórias perdem ou redesenham seus padrões de CD26, potencialmente enfraquecendo os freios que normalmente mantêm a inflamação sob controle. Embora mais estudos sejam necessários — especialmente em casos muito graves — este trabalho sugere que medir e, eventualmente, modular o eixo CD26/ADA pode um dia ajudar os médicos a avaliar a gravidade da doença ou a conceber tratamentos que acalmem incêndios imunes prejudiciais sem desligar completamente as defesas do corpo.
Citação: Shi, T., Shi, W., Tian, J. et al. Altered expression of the CD26/ADA axis in immune-mediated inflammation of infectious mononucleosis. Sci Rep 16, 9316 (2026). https://doi.org/10.1038/s41598-026-38891-z
Palavras-chave: mononucleose infecciosa, vírus Epstein-Barr, células T, regulação imune, via da adenosina