Clear Sky Science · pt
Avaliando a relação evolutiva da proteína de ligação à TATA (TBP) com vários padrões de dobramento de domínios proteicos usando máquina de vetores de suporte (SVM)
Como uma proteína “interruptora” do DNA se conecta a muitas outras
A proteína de ligação à caixa TATA, ou TBP, é uma operária das nossas células: ela ajuda a ativar genes ao agarrar o DNA em muitos promotores. Este estudo faz uma pergunta aparentemente simples, mas com grandes implicações: existem outras proteínas, com funções muito diferentes, que silenciosamente compartilham a forma subjacente da TBP? Ao combinar comparação de estruturas 3D, análise de sequência e ferramentas modernas de aprendizado de máquina, os autores traçam laços familiares ocultos entre a TBP e proteínas envolvidas em metabolismo, química de neurotransmissores e até vias relacionadas ao câncer.
Uma proteína-chave no controle gênico
A TBP fica na porta de entrada da expressão gênica em organismos que vão de leveduras a humanos. Ela reconhece uma sequência curta de DNA chamada caixa TATA e dobra o DNA para ajudar a montar a grande maquinaria de transcrição que copia genes em RNA. Como essa etapa é tão central, o dobramento — o arranjo tridimensional — do núcleo da TBP é altamente conservado ao longo da evolução. Os autores concentram-se numa estrutura de TBP bem estudada conhecida como 1tba e a usam como sonda para buscar outras proteínas que possam compartilhar seu projeto arquitetônico, mesmo que suas sequências de aminoácidos e funções cotidianas pareçam muito diferentes à primeira vista.
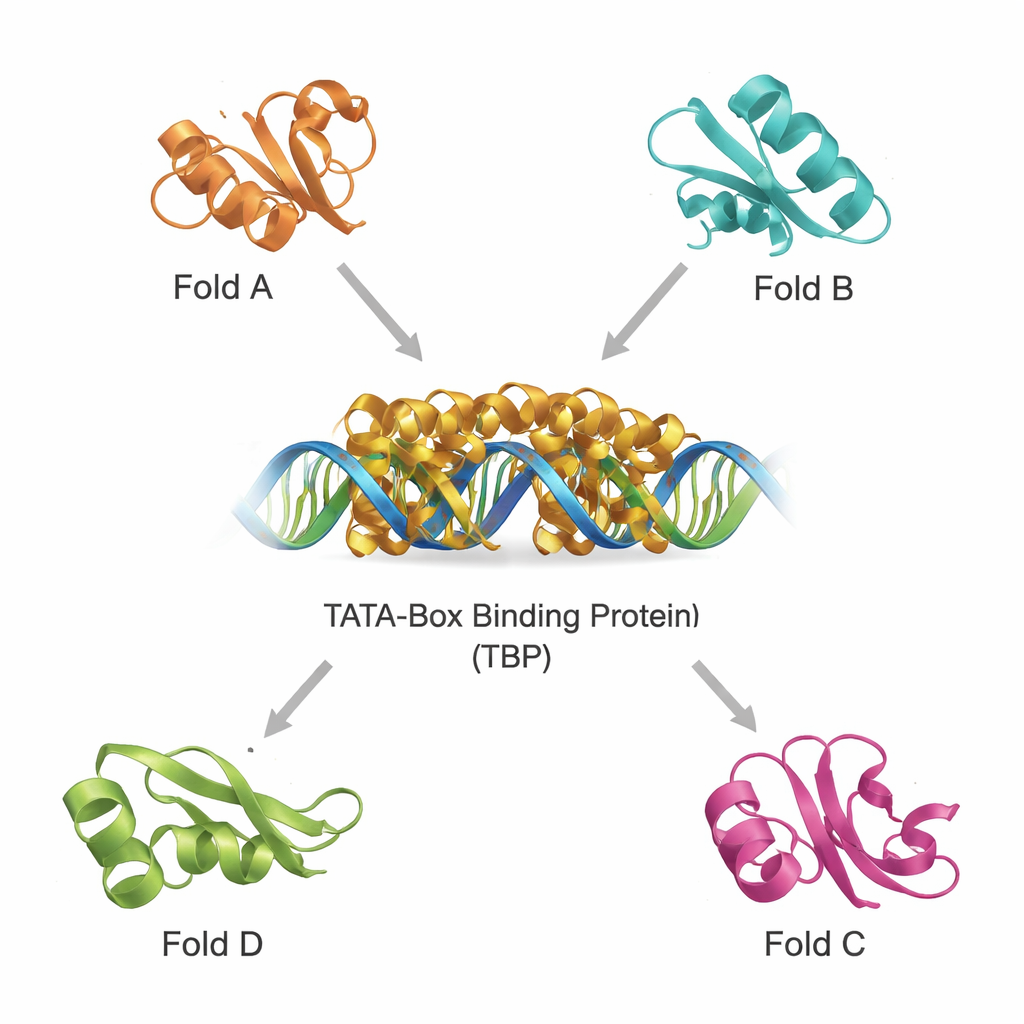
Encontrando primos estruturais em um universo proteico lotado
Bancos de dados modernos contêm centenas de milhares de estruturas de proteínas, tornando possível vasculhar por parentes distantes pela forma 3D em vez de apenas pela sequência. Usando duas ferramentas potentes, DALI e TOP‑search, a equipe primeiro extraiu proteínas cujos dobramentos se assemelhavam ao da TBP. Em seguida, classificaram esses candidatos com um catálogo evolutivo de domínios e os reduziram a um pequeno conjunto de exemplos estruturalmente semelhantes, mas funcionalmente diversos. Entre eles estão uma enzima que produz glutamina importante no metabolismo, um domínio encontrado em várias enzimas que lidam com tRNA, uma enzima com um dobramento característico em “hot‑dog” envolvida na química de ácidos graxos, e proteínas que ajudam a fabricar tetraidrobiopterina, uma molécula crucial para a função cerebral. Superpor suas estruturas à da TBP mostrou que, apesar das diferentes funções, elas compartilham motivos centrais reconhecíveis.
Ensinando máquinas a reconhecer famílias proteicas ocultas
Para ir além da inspeção caso a caso, os autores construíram modelos de aprendizado de máquina que pudessem automaticamente sinalizar dobramentos semelhantes aos da TBP. Eles reuniram grandes conjuntos de sequências de proteínas conhecidas por pertencer à TBP ou a cada um dos dobramentos relacionados, junto com um amplo conjunto de “fundo” de proteínas não relacionadas. Cada proteína foi convertida em resumos numéricos simples: com que frequência cada aminoácido aparece e com que frequência cada par possível de aminoácidos ocorre na sequência. Esses perfis alimentaram máquinas de vetores de suporte (SVMs) e modelos de floresta aleatória, que aprenderam a separar um tipo de dobramento de todos os outros. Usando validação cruzada rigorosa, os modelos alcançaram precisão muito alta — frequentemente acima de 95% — mesmo quando treinados apenas em partes das sequências correspondentes a regiões conservadas.
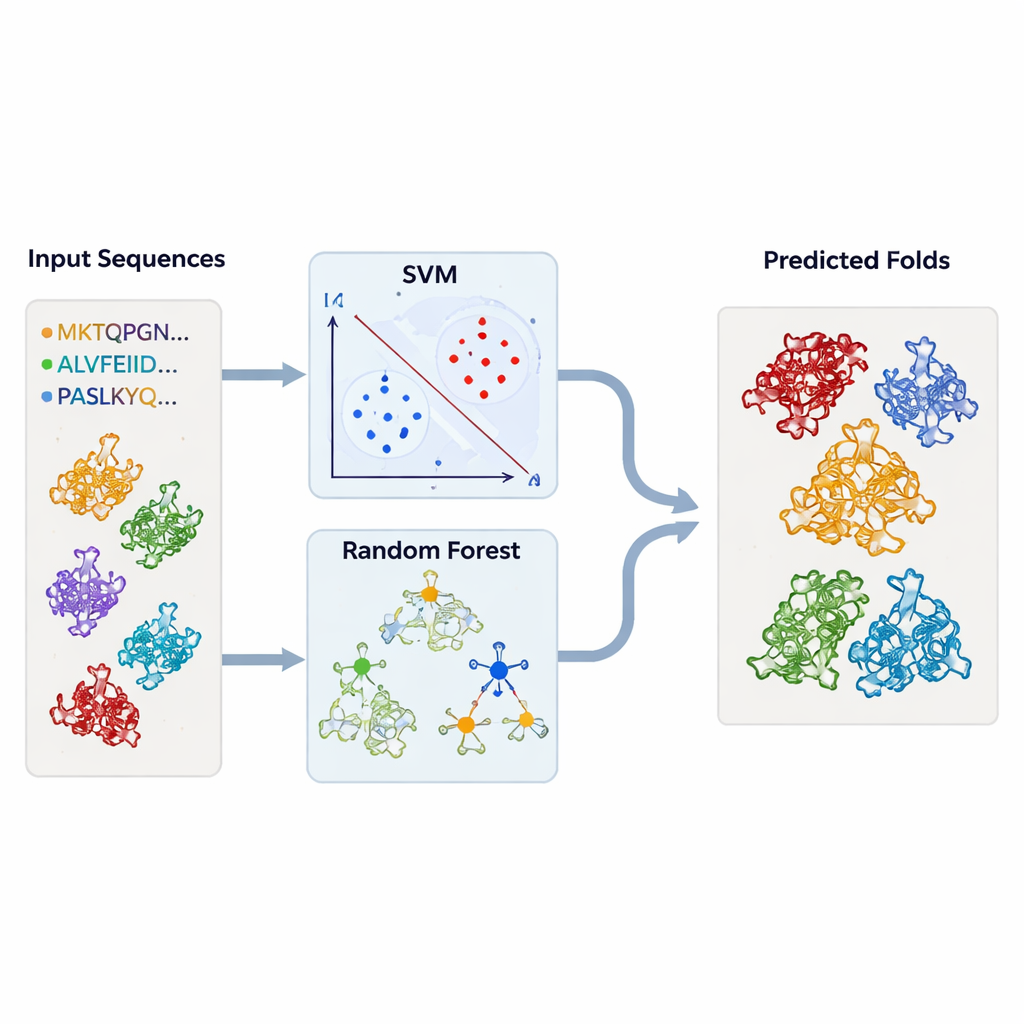
Testando os modelos em milhares de estruturas desconhecidas
Com esses classificadores treinados, a equipe voltou aos bancos de dados estruturais. Eles submeteram milhares de cadeias proteicas — recuperadas do DALI e do TOP‑search — a seus modelos para ver quais exibiam as marcas estatísticas de dobramentos semelhantes à TBP ou aos dobramentos relacionados. As abordagens SVM e de floresta aleatória concordaram em grande parte e identificaram muitos candidatos que as ferramentas estruturais também haviam sinalizado como similares. Em alguns casos, enzimas com atividades aparentemente não relacionadas ainda assim se agruparam fortemente com a TBP ou entre si, reforçando a ideia de que a evolução pode reaproveitar a mesma estrutura subjacente para muitos papéis bioquímicos diferentes.
Por que essas conexões ocultas importam
O estudo conclui que a TBP compartilha ancestralidade estrutural profunda com várias famílias de enzimas, incluindo proteínas semelhantes à glutamina sintetase e domínios de edição de enzimas de processamento de tRNA. Mesmo quando as sequências divergem e as funções se distanciam, essas proteínas preservam motivos arquitetônicos comuns, sugerindo descendência de um ancestral compartilhado. Para um público não especializado, a mensagem-chave é que a natureza tende a reciclar projetos bem‑sucedidos: um dobramento pode ser adaptado repetidamente para resolver problemas muito diferentes, desde ligar genes até ajustar metabolismo e química cerebral. Ao combinar comparação de estruturas 3D com aprendizado de máquina, os autores fornecem um conjunto de ferramentas prático para descobrir tais relações, ajudando biólogos a prever o que proteínas não caracterizadas podem fazer e apontando desenvolvedores de fármacos para novos alvos guiados pela evolução em vias relevantes para doenças.
Citação: Selvaraj, M.K., Kaur, J. Evaluating the evolutionary relationship of TATA binding protein (TBP) with various folding patterns of protein domains using support vector machine (SVM). Sci Rep 16, 7696 (2026). https://doi.org/10.1038/s41598-026-38883-z
Palavras-chave: proteína de ligação à caixa TATA, evolução de proteínas, aprendizado de máquina, estrutura de proteínas, máquina de vetores de suporte