Clear Sky Science · pt
Medições de densidade de massa em célula única usando centrifugação por gradiente em microcanais
Por que pesar células minúsculas importa
Cada célula viva é mais do que um saco de moléculas; seu peso e sua compacidade contam uma história sobre seu estado de saúde. Mudanças sutis na densidade de empacotamento de uma célula podem sinalizar se ela está crescendo, morrendo, combatendo uma infecção ou se tornando cancerosa. Ainda assim, apesar desse potencial, medir a densidade de massa de milhares de células individuais tem sido lento, tecnicamente exigente e caro. Este artigo apresenta uma forma nova e muito mais simples de “pesar” células únicas observando como elas flutuam ou afundam em um líquido controlado dentro de um canal de vidro finíssimo girado em uma centrífuga.
Uma nova variação de um truque antigo de laboratório
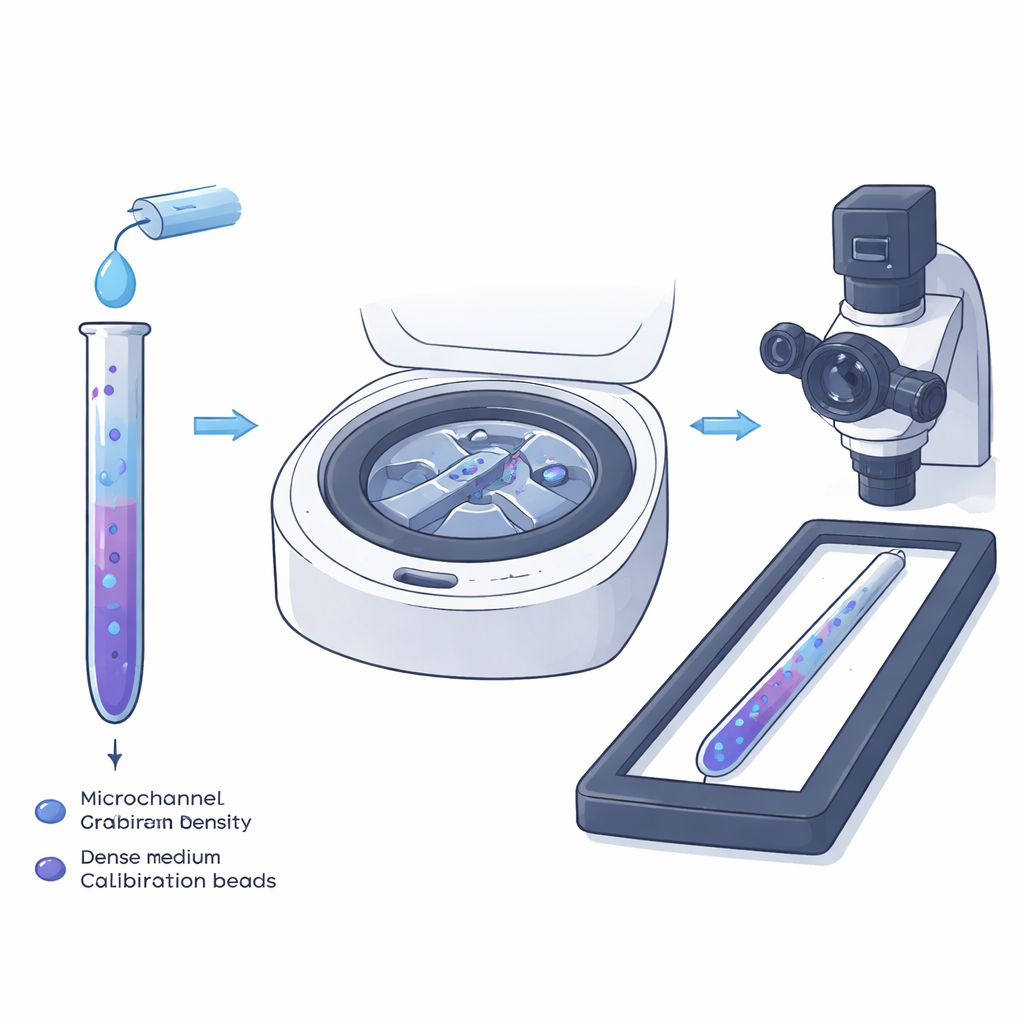
A centrifugação em gradiente de densidade tradicional há muito é usada em tubos para separar misturas de células: quando giradas, as células se assentam no ponto do líquido por camadas onde sua própria densidade corresponde à do fluido ao redor. Os autores miniaturizam essa ideia em um microcanal estreito para que células individuais, não apenas camadas, possam ser medidas diretamente ao microscópio. Eles preenchem o canal primeiro com um líquido leve contendo as células e depois com um líquido mais denso contendo pequenas partículas plásticas cujas densidades são precisamente conhecidas. Quando esses dois líquidos se encontram e fluem no canal minúsculo, formam naturalmente um gradiente de densidade suave e unidimensional ao longo de seu comprimento.
Criando uma rampa suave de densidade
Dentro de canais tão finos, o fluido flui devagar e de forma laminar, sem turbulência. Nessas condições, o perfil parabólico do fluxo mistura o líquido leve e o pesado o suficiente para criar uma transição gradual, em vez de uma fronteira abrupta, entre eles. A equipe estudou esse processo tanto experimentalmente, usando uma tinta fluorescente, quanto por simulações computacionais. Eles descobriram que um gradiente de densidade quase linear, estendendo-se por vários milímetros, pode ser formado em questão de segundos. A altura do canal mostrou‑se crucial: canais rasos mantêm o gradiente estável e impedem o balanço causado pela gravidade do líquido mais denso, o que borraria a relação entre posição e densidade e introduziria erros nas medidas finais das células.
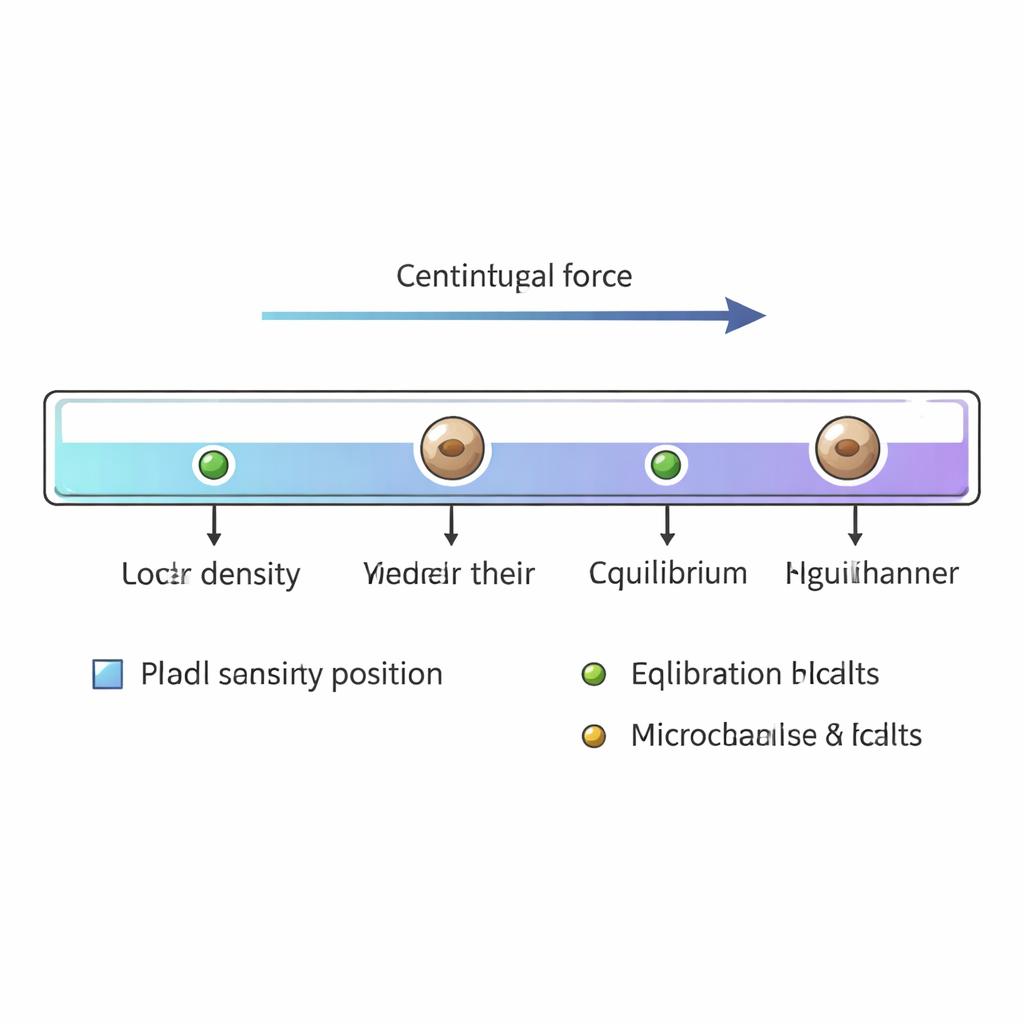
Girando as células até seu ponto de equilíbrio
Uma vez preenchido o canal, suas extremidades são seladas e ele é colocado em uma pequena centrífuga. Girando a cerca de 12.000 rotações por minuto, células e microesferas de calibração movem‑se ao longo do canal até que a força centrífuga seja exatamente equilibrada pela flutuabilidade correspondente à sua densidade particular. Maiores que cerca de três micrômetros de diâmetro, células de levedura atingem esse equilíbrio em menos de 20 segundos. Após aproximadamente um minuto e meio de centrifugação, o canal é removido e escaneado em um microscópio padrão. Os pesquisadores registram as posições de milhares de células individuais de levedura e das esferas de referência, e então convertem cada posição ao longo do gradiente em um valor de densidade de massa usando as densidades conhecidas das esferas como pontos de ancoragem.
Lendo a saúde celular a partir de diferenças minúsculas
Usando essa abordagem, os autores mediram as densidades de mais de 20.000 células de levedura em múltiplos canais. A incerteza típica da medida para uma única célula foi de cerca de 3,3 quilogramas por metro cúbico — pequena o bastante para resolver diferenças biológicas reais, que em suas amostras foram aproximadamente duas vezes maiores. Ao longo de várias horas, observaram que a população principal de levedura manteve uma densidade estável, enquanto uma segunda população, mais densa e ligeiramente menor, apareceu gradualmente. Esse grupo mais denso provavelmente consistia de células mortas ou danificadas que haviam incorporado o fluido mais pesado, tornando‑as mais compactas. Os valores medidos concordaram bem com resultados de técnicas muito mais complexas e lentas, como ressonadores de microcanais suspensos, métodos ópticos e levitação magnética.
Do protótipo de laboratório ao biomarcador prático
O estudo mostra que uma combinação simples de microcanais de vidro, centrífugas comerciais e microscópios padrão pode fornecer medições de densidade de célula única em alta vazão, a taxas de aproximadamente 16.000 células por hora. Embora ainda não seja sensível o suficiente para detectar as menores mudanças induzidas por fármacos, já é potente o bastante para distinguir diferentes tipos celulares ou células vivas de mortas com base no quão compactas são. Ao tornar o “pesar” preciso de células mais acessível e econômico, esse método de gradiente em microcanais pode ajudar a transformar a densidade de massa celular em um biomarcador rotineiro para monitorar doenças, avaliar terapias e explorar como as células regulam sua composição interna.
Citação: Soller, R., Augustsson, P. & Barnkob, R. Single-cell mass-density measurements using microchannel gradient centrifugation. Sci Rep 16, 6501 (2026). https://doi.org/10.1038/s41598-026-38872-2
Palavras-chave: densidade de célula única, microfluídica, centrifugação, células de levedura, biomarcadores celulares