Clear Sky Science · pt
Dinâmica conformacional e análises de energia livre de ligação revelam um inibidor flavonoide estável da polimerase NS5 do vírus da dengue
Por que um vírus transmitido por mosquitos precisa de ajuda de origem vegetal
A febre da dengue explodiu em todo o mundo nos últimos anos, adoecendo milhões e matando milhares. Ainda assim, carecemos de um comprimido antiviral amplamente eficaz e acessível para tratar as pessoas após a infecção. Este estudo investiga uma pergunta aparentemente simples, mas de grande alcance: compostos naturais de plantas podem ser transformados em “chaves” moleculares precisas que emperram uma das máquinas mais importantes do vírus da dengue?
O motor viral que os cientistas querem desligar
O vírus da dengue sobrevive copiando seu material genético dentro de nossas células. Para isso, depende de uma proteína-chave chamada NS5, que funciona como um minúsculo motor de cópia do RNA do vírus. Se a NS5 deixar de funcionar, o vírus não consegue produzir novos genomas e a infecção estagna. Portanto, desenvolvedores de fármacos veem a NS5 — especialmente sua região que copia RNA, conhecida como polimerase dependente de RNA — como um alvo principal para novos medicamentos. Diversos compostos sintéticos e extratos vegetais já demonstraram que a NS5 pode ser bloqueada, mas muitos desses candidatos iniciais ligam-se fracamente, são instáveis ou levantam preocupações sobre segurança e biodisponibilidade.
Procurando agulhas químicas promissoras no palheiro das plantas
Os pesquisadores concentraram-se em flavonoides, uma grande família de compostos vegetais presentes em alimentos como frutas vermelhas, chá e ervas, conhecidas há muito por efeitos antivirais e anti-inflamatórios. A partir de um banco de dados curado de metabólitos secundários de plantas, selecionaram 326 flavonoides e prepararam modelos tridimensionais tanto da enzima NS5 do vírus quanto de cada molécula candidata. Usando um processo de acoplamento computacional em etapas, perguntaram: quais formas se encaixam melhor em uma região “porta dos fundos” específica da NS5 chamada bolso N — um sítio alostérico que pode desligar a enzima quando ocupado e que tende a mutar menos que o sítio ativo principal?
Em cada etapa dessa triagem virtual, compostos que se encaixavam mal ou pareciam improváveis de se comportar como fármacos reais no organismo foram descartados. As moléculas remanescentes foram então avaliadas não apenas pelo ajuste geométrico, mas também pela força de ligação estimada usando um método que aproxima as energias envolvidas quando um composto se liga à NS5 em condições aquosas semelhantes às celulares. Esse processo reduziu o número para um punhado de flavonoides principais, com um candidato, rotulado PSCdb01560, destacando-se por sua energia livre de ligação prevista particularmente favorável.
Observando moléculas se moverem em um microscópio virtual
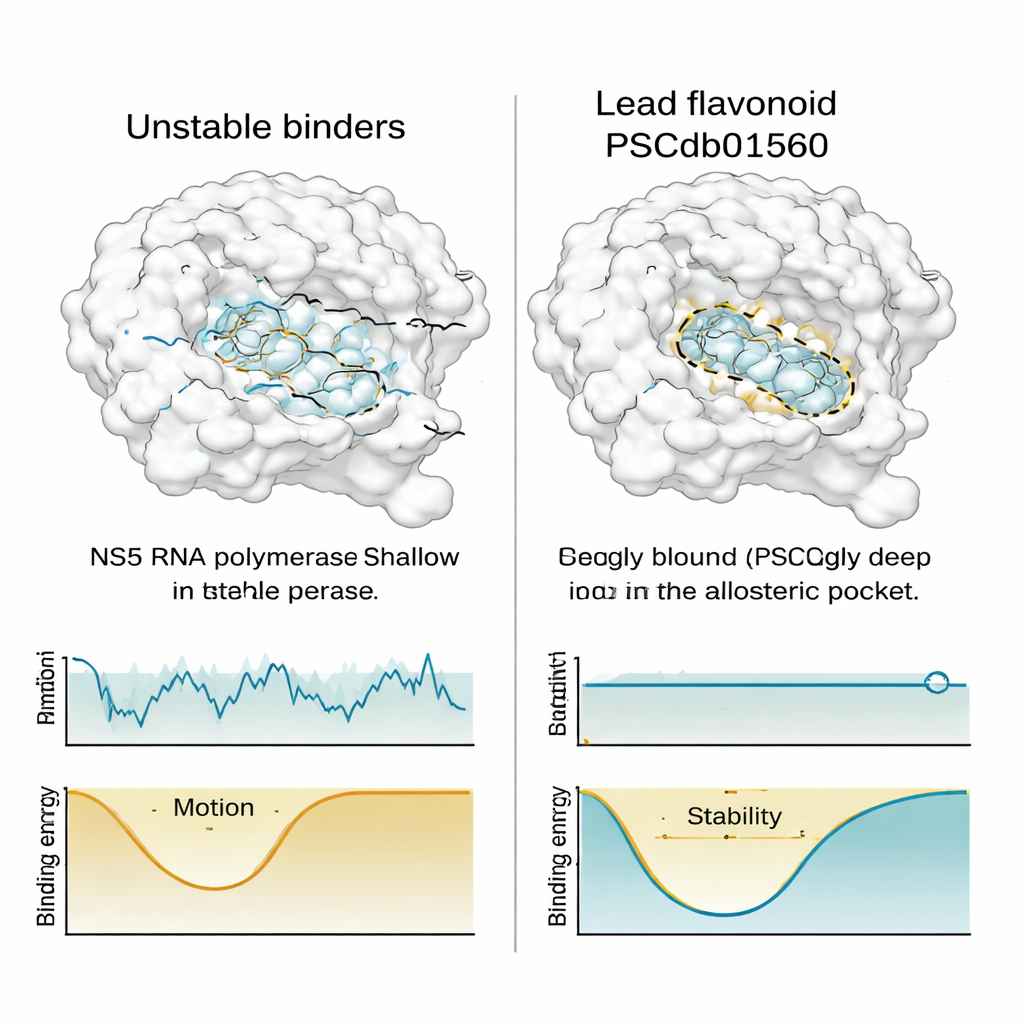
Encaixar-se bem em uma imagem estática não é suficiente; um medicamento útil também precisa permanecer no lugar quando tudo se agita na vida real. Para testar isso, a equipe executou longas e detalhadas simulações de dinâmica molecular — filmes computacionais equivalentes a meio microssegundo — para a NS5 emparelhada com os melhores flavonoides e com um inibidor de referência conhecido. Eles rastrearam quanto a proteína e cada composto oscilaram, quão compacto permaneceu o complexo, quão exposto ele ficou à água circundante e com que frequência contatos químicos-chave se formaram e se romperam. O PSCdb01560 mostrou comportamento notavelmente estável: permaneceu profundamente alojado no bolso N, moveu-se muito pouco em comparação com moléculas concorrentes e pareceu estabilizar a forma geral da NS5 em vez de perturbá‑la.
Em contraste, dois outros flavonoides que inicialmente pareciam promissores começaram a derivar dentro do bolso ou tornaram-se mais expostos ao solvente com o tempo — sinais de ligação mais fraca e menos confiável. Quando os pesquisadores mapearam a “paisagem de energia livre” de cada complexo — uma forma de visualizar quais conformações são termodinamicamente favorecidas — encontraram que o PSCdb01560 ocupava um vale energético profundo e bem definido, enquanto os compostos menos estáveis pulavam entre vários compartimentos mais rasos. Ao comparar os instantâneos de menor energia com as poses originais do acoplamento, a posição do PSCdb01560 mal mudou, ressaltando sua fidelidade conformacional.
Números que indicam força em nível de fármaco
Por fim, a equipe usou um arcabouço de cálculo de energia para estimar quão fortemente cada flavonoide se ligaria após todo o movimento simulado ser levado em conta. O PSCdb01560 atingiu uma energia livre de ligação mais favorável do que o composto de referência estabelecido, impulsionada por uma combinação de complementaridade de forma, interações elétricas atraentes e contatos hidrofóbicos dentro do bolso. Esse padrão — afinidade computacional forte, posicionamento estável ao longo do tempo, flexibilidade interna limitada e engajamento de resíduos cruciais da NS5 compartilhados entre cepas da dengue — destaca o PSCdb01560 como um ponto de partida particularmente convincente para o desenho de fármacos.
O que isso pode significar para futuros tratamentos contra a dengue
Esses resultados ainda não entregam um comprimido contra a dengue, mas reduzem significativamente a busca. O trabalho identifica um arcabouço flavonoide de origem vegetal que, no computador, supera vários concorrentes e até um inibidor de referência conhecido, tanto em estabilidade quanto em força de ligação prevista. Os próximos passos são experimentais: testar se o PSCdb01560 realmente bloqueia a NS5 em tubos de ensaio, impede a replicação do vírus da dengue em células infectadas e se mostra seguro em modelos animais. Se esses obstáculos forem superados, químicos poderão otimizar esse flavonoide até torná-lo um antiviral clinicamente útil. Por enquanto, o estudo oferece uma mensagem otimista: a própria biblioteca química da natureza ainda contém ferramentas promissoras para desarmar uma das ameaças transmitidas por mosquitos que mais cresce no mundo.
Citação: Alsaady, I.M., Gattan, H.S., Aljahdali, S.M. et al. Conformational dynamics and binding free energy analyses unveil a stable flavonoid inhibitor of dengue virus NS5 polymerase. Sci Rep 16, 7761 (2026). https://doi.org/10.1038/s41598-026-38864-2
Palavras-chave: vírus da dengue, polimerase NS5, inibidor flavonoide, descoberta de antivirais, acoplamento molecular