Clear Sky Science · pt
Determinantes ao nível dos resíduos da estabilidade térmica da endolisina extremofílica Ts2631
Por que vírus termófilos importam para futuros antibióticos
À medida que a resistência a antibióticos aumenta, os cientistas correm para encontrar novas formas de eliminar bactérias perigosas. Uma abordagem promissora toma emprestado armas de vírus que infectam bactérias, chamados bacteriófagos. Esses vírus produzem enzimas, conhecidas como endolisinas, que abrem furos nas paredes celulares bacterianas. O estudo discutido aqui foca numa endolisina notavelmente resistente ao calor, Ts2631, de um vírus que vive em fontes termais islandesas. Ao descobrir quais blocos construtores individuais dessa proteína a tornam tão estável em temperaturas próximas ao ponto de ebulição, os pesquisadores esperam projetar enzimas antibacterianas mais robustas e duradouras para medicina e biotecnologia. 
Uma ferramenta viral forjada em fontes termais ferventes
Ts2631 provém de um bacteriófago que infecta a bactéria termófila Thermus scotoductus, que prospera em águas que alcançam bem acima de 60 °C. A enzima Ts2631 corta uma ligação específica no peptidoglicano, a malha resistente que envolve as células bacterianas. O que diferencia Ts2631 é sua termostabilidade extrema: ela permanece dobrada até aproximadamente 100–105 °C, dependendo da solução. Isso está muito acima das temperaturas nas quais a maioria das proteínas se desmonta. Os autores compararam Ts2631 com sua prima mais bem estudada de um vírus de temperatura moderada, a lisozima T7, para entender que truques estruturais a natureza usou para manter Ts2631 intacta sob condições tão severas.
Loops mais curtos e uma mistura diferente de blocos construtores
Proteínas são cadeias de 20 tipos de aminoácidos, dobradas em formas intrincadas. Quando os pesquisadores sobrepuseram as estruturas 3D de Ts2631 e da lisozima T7, constataram que a arquitetura geral é muito semelhante: ambas têm um núcleo compacto de hélices e fitas. A principal diferença reside nas regiões de loop flexíveis que conectam esses elementos. Em Ts2631, esses loops são mais curtos e mostram menor flexibilidade, enquanto a lisozima T7 possui loops mais longos e frouxos. Ts2631 também carrega mais de certos aminoácidos frequentemente associados à resistência ao calor: a rígida prolina; resíduos aromáticos como tirosina e triptofano; e a arginina carregada positivamente. Ao mesmo tempo, tem menos resíduos de serina, ácido aspártico e ácido glutâmico, que podem tornar proteínas mais vulneráveis em altas temperaturas. Esse padrão se mantém não apenas em comparação com a lisozima T7, mas também quando Ts2631 é comparada a centenas de milhares de proteínas virais e a muitos milhões de proteínas bacterianas.
Trocando aminoácidos individuais para testar sua importância
Para avançar de correlações para causa e efeito, a equipe substituiu sistematicamente 55 aminoácidos individuais em Ts2631 e mediu como cada mutação afetou a temperatura de fusão (Tm) e a capacidade da enzima de degradar paredes celulares bacterianas. Algumas alterações ao redor do sítio ativo que contém zinco foram especialmente prejudiciais. Quando modificaram três resíduos que coordenam o zinco (H30, H131 e C139), a Tm da proteína caiu em até cerca de 20 °C, e a atividade foi perdida. Duas tirosinas conservadas (Y60 e Y69) também contribuíram para a estabilidade. Surpreendentemente, remover uma ligação dissulfeto — um tipo de ligação covalente entre cisteínas C80 e C90 — na verdade elevou a temperatura de fusão, embora tenha destruído a atividade. Isso mostra que ser muito estável em tubo de ensaio nem sempre significa que a proteína funcionará melhor em condições reais. 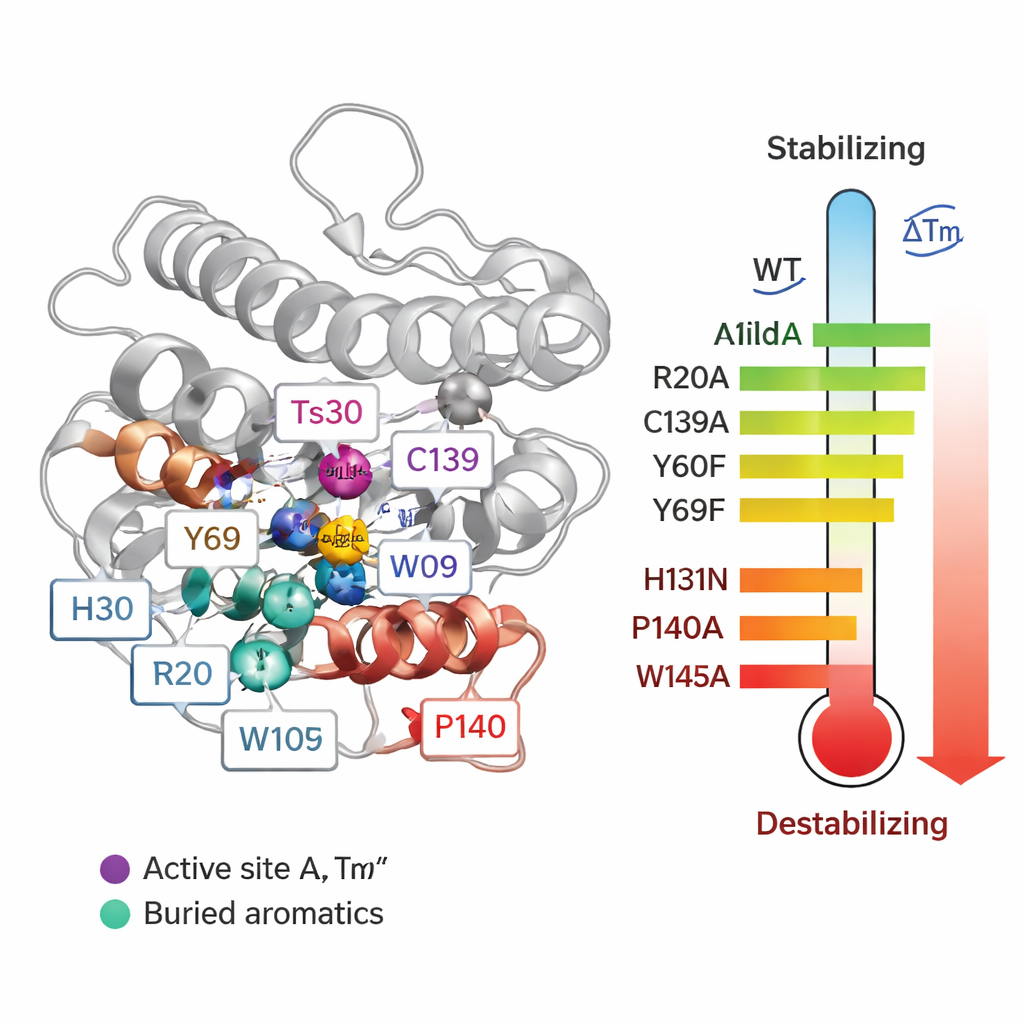
“Âncoras” aromáticas ocultas e uma pega-chave na parede bacteriana
Os resultados mais marcantes vieram da mutação de resíduos de prolina e triptofano. Alterar uma única prolina (P140), localizada bem ao lado da cisteína ligadora de zinco C139, reduziu a Tm em mais de 21 °C e enfraqueceu a atividade após aquecimento, porque a mutação perturbou a geometria especial de ligação necessária para a coordenação adequada do metal. Vários triptofanos profundamente enterrados (W102, W109 e especialmente W145) também se mostraram críticos: substituí-los por alanina causou quedas de Tm de 14–24 °C e tornou a enzima muito mais sensível ao calor durante testes de atividade. Esses resíduos aromáticos atuam como âncoras internas que travam o núcleo da proteína no lugar. Entre as argininas, a maioria teve pouco efeito na estabilidade, mas R20 revelou-se essencial para agarrar o peptidoglicano. Quando R20 foi substituído, a enzima se ligou mal à parede celular bacteriana e perdeu atividade ao aquecimento, revelando que alguns resíduos contribuem mais para a função do que para a simples robustez térmica.
De enzimas de fontes termais a antibacterianos mais resistentes
Em conjunto, o estudo mostra que a resistência térmica extraordinária de Ts2631 se apoia em um punhado de aminoácidos bem posicionados, em vez de um fortalecimento uniforme de toda a proteína. Resíduos que ligam zinco, uma prolina conservada próxima ao sítio ativo e cadeias laterais aromáticas enterradas formam um núcleo estabilizador, enquanto algumas características clássicas de estabilização, como pontes dissulfeto ou pontes salinas, importam menos aqui do que o esperado. Para o campo mais amplo, este trabalho sugere que endolisinas mesofílicas (de temperatura moderada) podem ser tornadas mais duráveis ao se trocar cuidadosamente posições selecionadas por triptofano ou prolina sem sacrificar a atividade antibacteriana. Em outras palavras, ao aprender como a natureza constrói enzimas que resistem a temperaturas próximas à ebulição, os cientistas obtêm um roteiro prático para projetar antibióticos à base de proteínas mais confiáveis e de vida útil prolongada.
Citação: Cieminska, K., Kaczorowska, AK., Kozlowski, L.P. et al. Residue-level determinants of the thermal stability of the extremophilic Ts2631 endolysin. Sci Rep 16, 7630 (2026). https://doi.org/10.1038/s41598-026-38786-z
Palavras-chave: endolisina termoestável, enzimas de bacteriófagos, termostabilidade de proteínas, resistência a antibióticos, engenharia de proteínas