Clear Sky Science · pt
Síntese química de novos derivados aminopirimidin-4-il-1H-pirazol como inibidores da tirosina quinase do baço (SYK)
Por que bloquear uma única enzima pode ajudar a combater o câncer e a inflamação
Nosso sistema imunológico depende de mensagens internas rápidas para dizer às células quando atacar invasores e quando recuar. Quando esses sinais falham, podem alimentar doenças autoimunes e o câncer. Este estudo explora uma via promissora para silenciar esses sinais defeituosos projetando pequenas moléculas semelhantes a fármacos que bloqueiam seletivamente uma enzima chave, a tirosina quinase do baço (SYK), que está perto do centro de muitas reações imunes.
Um interruptor de sinal no núcleo de muitas doenças
SYK age como um interruptor mestre dentro de certas células imunes. Quando ativada, ajuda a impulsionar a inflamação, a produção de anticorpos e o crescimento celular. Em contextos saudáveis isso é útil para combater infecções. Mas em condições como artrite reumatoide, asma e diversos cânceres sanguíneos e sólidos, a atividade de SYK pode ficar excessiva, mantendo as células imunes ligadas e apoiando a sobrevivência tumoral. Por esse papel central, pesquisadores em todo o mundo tentam desenvolver medicamentos que bloqueiem SYK com potência suficiente para ser eficaz, mas com precisão para evitar atingir muitas outras enzimas e causar efeitos colaterais.
Construindo uma família de pequenas moléculas sob medida
Os autores criaram uma nova série de moléculas relacionadas construídas em torno de um arcabouço químico comum chamado aminopirimidin-4-il-1H-pirazol. A partir de blocos de construção simples, eles montaram essas peças passo a passo e então modificaram uma porção da estrutura para produzir nove candidatos finais. Cada molécula foi cuidadosamente verificada usando métodos analíticos padrão para confirmar que sua estrutura e pureza estavam conforme o esperado. Essa abordagem modular permitiu à equipe sondar como mudanças sutis em forma e flexibilidade afetam a interação desses compostos com SYK.
Observando como os compostos agarram seu alvo
Antes de ir ao banco de laboratório, os pesquisadores usaram simulações computacionais para ver quão firmemente cada molécula poderia se fixar ao SYK. Cálculos de docking estimaram quão bem os compostos se encaixam no bolso de ligação da enzima, destacando um candidato, rotulado 44, como especialmente promissor. Simulações mais detalhadas de dinâmica molecular, nas quais o complexo proteína–fármaco é acompanhado ao longo de centenas de nanosegundos, mostraram que o 44 forma uma parceria particularmente estável com SYK. A proteína permaneceu compacta, contatos-chave se mantiveram no lugar, e o sistema assentou em uma única conformação de baixa energia com muitas ligações de hidrogênio fortes, especialmente envolvendo aminoácidos como triptofano e serina que ajudam a acomodar a molécula.
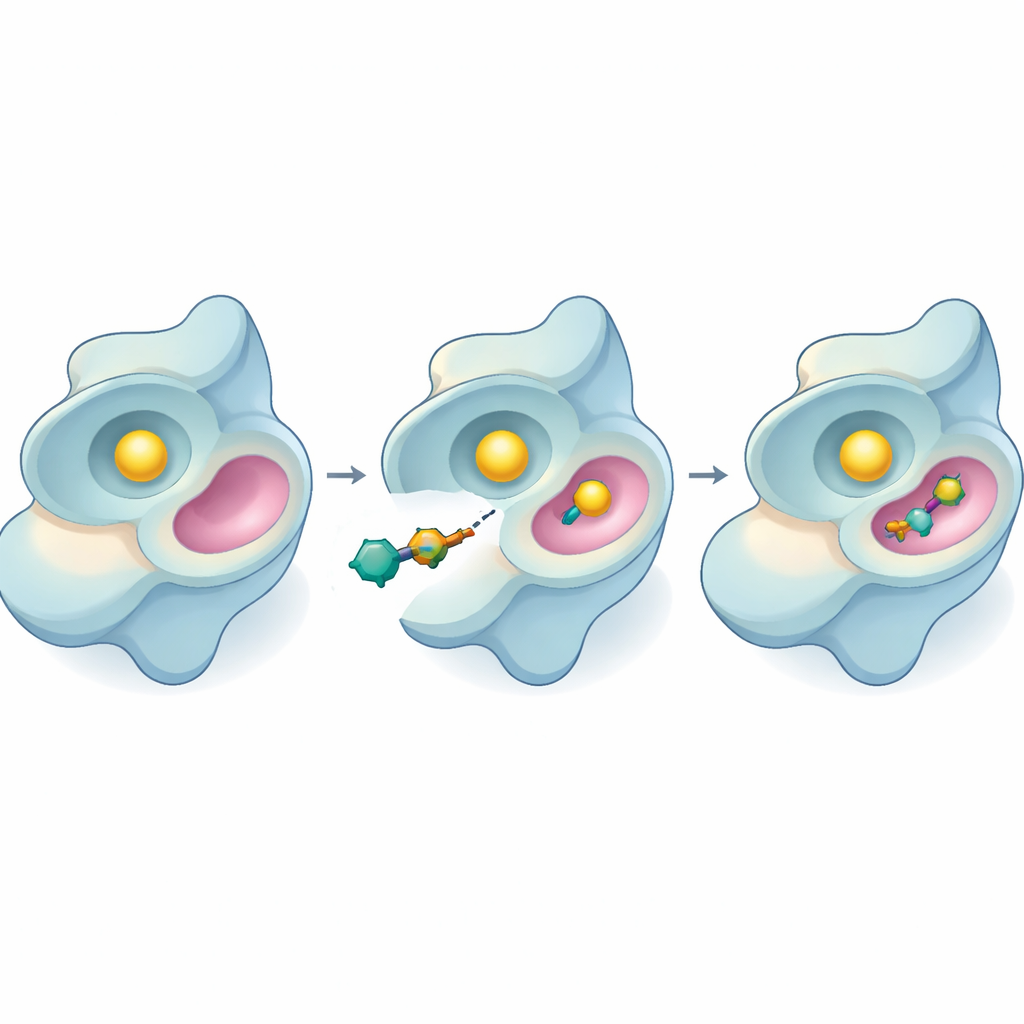
Submetendo os novos inibidores ao teste
A equipe então passou para experimentos de laboratório usando um ensaio baseado em luz que mede quão ativamente o SYK consome sua molécula de combustível, o ATP. Vários dos novos compostos retardaram a enzima, mas o 44 destacou-se novamente. Ele inibiu SYK em concentrações muito baixas e tornou-se mais eficaz quanto mais tempo permanecia com a enzima. Variando a quantidade de substrato presente, os pesquisadores puderam inferir como o 44 atua: em vez de competir diretamente com o ATP no sítio ativo principal, parece ligar-se em um sítio diferente, alostérico, e alterar o comportamento da enzima à distância. Isso é importante porque inibidores alostéricos frequentemente mantêm seu efeito mesmo quando os níveis de ATP são altos ou quando mutações alteram o sítio primário.
O que isso pode significar para tratamentos futuros
Tomados em conjunto, os modelos computacionais e as medidas de laboratório pintam um quadro consistente: a molécula 44 liga-se fortemente ao SYK, mantém a enzima em um estado estável e menos flexível, e interrompe sua atividade por um mecanismo indireto e não competitivo. Para não especialistas, isso significa que os pesquisadores identificaram uma chave química afinada que se encaixa em uma fechadura crítica para muitas doenças dirigidas pelo sistema imune, sem simplesmente bloquear a entrada principal. Embora ainda reste muito trabalho — especialmente testes em células, animais e em painéis mais amplos de enzimas relacionadas — este arcabouço oferece um ponto de partida promissor para futuros fármacos destinados a domar a inflamação nociva e retardar certos cânceres ao mirar em SYK.
Citação: Rajasheker, K.V., Pallavi, M.S., Singh, P. et al. Chemical synthesis of novel aminopyrimidin-4-yl-1H-pyrazole derivatives as spleen tyrosine kinase (SYK) inhibitors. Sci Rep 16, 8323 (2026). https://doi.org/10.1038/s41598-026-38719-w
Palavras-chave: tirosina quinase do baço, inibidores de quinase, terapias contra o câncer, doença autoimune, fármacos alostéricos