Clear Sky Science · pt
Transferência de prótons induzida por luz em água com estruturas diferentes: uma abordagem por RPE para resolver um problema clássico
Por que as Jornadas Ocultas dos Prótons Importam
Cada vez que você respira, pensa ou converte a luz solar em energia útil em uma célula solar, partículas minúsculas com carga positiva chamadas prótons estão em movimento. Como esses prótons viajam através da água é um enigma de séculos, formulado pela primeira vez pelo cientista Theodor Grotthuss em 1806. Este novo estudo usa uma combinação engenhosa de luz e medições magnéticas para observar prótons se movendo em águas com estruturas diferentes, desde soluções salinas e congestionadas até misturas vítreas e geladas e até mesmo dentro de uma proteína de membrana. O trabalho oferece uma maneira renovada de testar ideias clássicas sobre o movimento de prótons e de sondar ambientes que são difíceis de estudar por outros métodos.
Uma Nova Forma de Observar o Movimento dos Prótons
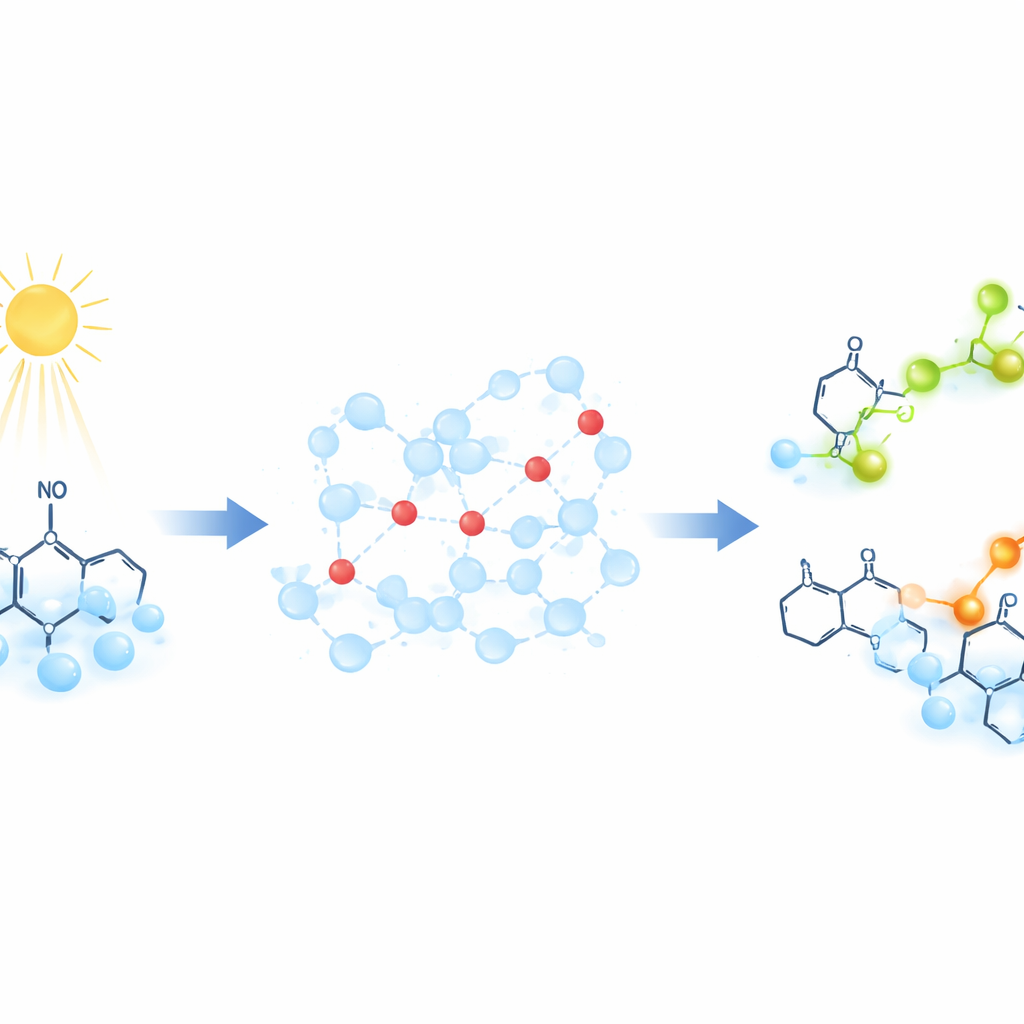
Em vez de seguir os prótons diretamente, os pesquisadores usam moléculas “sonda” especiais que mudam sua assinatura magnética quando capturam um próton. Essas sondas são radicais orgânicos estáveis cujo elétron desemparelhado produz um sinal bem definido em ressonância paramagnética eletrônica (RPE), uma técnica que detecta como elétrons desemparelhados respondem a um campo magnético. Para lançar o movimento de prótons sob demanda, a equipe incide luz sobre um composto chamado 2‑nitrobenzaldeído. Essa reação acionada pela luz libera um surto de prótons em menos de um bilionésimo de segundo, reduzindo subitamente o pH da solução. À medida que os prótons se espalham pela água e se ligam às sondas, o sinal de RPE desloca‑se de forma dependente do tempo, permitindo aos cientistas acompanhar quão rápido ocorre a transferência de prótons.
Como os Vizinhos da Água Freiam ou Aceleram o Fluxo
A água raramente existe sozinha; geralmente está cheia de sais dissolvidos ou outras moléculas que reorganizam sutilmente sua rede de ligações de hidrogênio. A equipe testou como esses aditivos afetam o movimento de prótons comparando água pura com soluções contendo cloreto de potássio, ureia ou cloridrato de guanidínio, todas em concentrações altas. Ajustando as mudanças no sinal de RPE a modelos cinéticos simples, eles extraíram taxas aparentes de transferência de prótons. Descobriram que em 6 molar de cloridrato de guanidínio a transferência de prótons foi cerca de 40 vezes mais lenta do que na água pura, enquanto 8 molar de ureia causou apenas uma desaceleração moderada, e o cloreto de potássio produziu efeitos intermediários. Como a taxa com que os prótons reagem com as sondas é limitada por como eles se movem através da rede de ligações de hidrogênio, essas diferenças apontam para mudanças substanciais em como a água é estruturada ao redor dos íons e moléculas adicionados.
Movimento de Prótons em Gelo Vítreo e Dentro de Proteínas
O método não se limita à água líquida comum. Os autores também estudaram uma mistura água–glicerol resfriada a 160 kelvin, onde ela forma um vidro rígido. A difusão livre de moléculas está essencialmente congelada, ainda assim o sinal de RPE mostrou que as sondas estavam sendo protonadas após a exposição à luz. Isso sugere que a transferência de prótons pode prosseguir sem difusão clássica, possivelmente por tunelamento quântico ao longo de uma cadeia de ligações de hidrogênio, ecoando refinamentos modernos da ideia de Grotthuss. Para explorar a relevância biológica, a equipe ligou um radical sensível ao pH a um sítio específico da proteína de membrana bacteriorrodopsina, na fronteira entre a proteína e a água circundante. Quando dispararam a liberação de prótons com luz, observaram uma resposta de RPE dependente do tempo desse sítio marcado, demonstrando que sua abordagem pode monitorar a entrega de prótons a uma posição definida na superfície de uma proteína.
Conectando Estrutura, Água e Rodovias de Prótons
Para entender melhor por que a sonda ligada à proteína se comportou de maneira muito semelhante à de uma em água de volume, os pesquisadores realizaram simulações computacionais da bacteriorrodopsina em uma membrana e de um pequeno peptídeo em solução. Eles calcularam como as moléculas de água envolvem o grupo nitroxílico do rótulo de spin e encontraram padrões locais de hidratação quase idênticos em ambos os casos, com apenas um leve blindagem pelo ambiente de membrana. Isso significa que, pelo menos para o sítio estudado, os prótons têm acesso através de uma camada de água que se assemelha de perto à água líquida comum. Os autores também mostram que suas sondas podem ser usadas em experimentos de RPE com resolução temporal, abrindo a porta para rastrear simultaneamente o movimento de prótons e elétrons em reações onde os dois estão fortemente acoplados.
O Que Este Trabalho Nos Diz em Termos Simples
Essencialmente, este estudo transforma a luz em um tiro de partida nítido para o movimento de prótons e então usa sondas magnéticas sensíveis para observar com que rapidez esses prótons alcançam diferentes alvos. Ao comparar soluções salinas simples, desnaturantes densos, misturas vítreas e uma proteína de membrana, os pesquisadores demonstram que o fluxo de prótons é fortemente moldado por como as moléculas de água estão dispostas e pelo ambiente ao redor. Sua abordagem não apenas apoia a ideia de que os prótons saltam ao longo de redes de ligações de hidrogênio, mas também revela que esse salto pode persistir mesmo quando o movimento molecular comum está quase congelado. Este novo conjunto de ferramentas pode ajudar cientistas a dissecar como os prótons se movem em enzimas, sistemas de conversão de energia e materiais inovadores, aproximando‑nos do controle desses portadores de carga minúsculos, mas poderosos.
Citação: Barbon, A., Savitsky, A., Grigoriev, I. et al. Photoinduced proton transfer in differently structured water: an EPR approach to solving a classic problem. Sci Rep 16, 7983 (2026). https://doi.org/10.1038/s41598-026-38650-0
Palavras-chave: transferência de prótons, estrutura da água, ressonância paramagnética eletrônica, rede de ligações de hidrogênio, bacteriorrodopsina